网址:http://m.1010jiajiao.com/timu3_id_146653[举报]
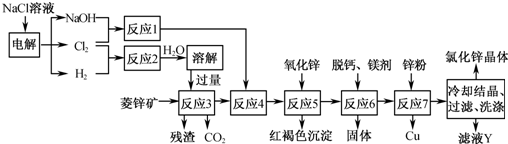
(1)在反应3前要将菱锌矿研磨,其目的是
(2)反应4将Fe2+氧化为Fe3+,该反应的离子方程式为
(3)加入氧化锌调节pH=4.5,反应5的离子方程式为
(4)锌粉不在反应4之前加入的原因是
(5)若用石墨作电极电解滤液Y,则可以得到参与本流程反应的物质有
 一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”.如2Fe3++Cu=2Fe2++Cu2+,可拆写为氧化反应式:Cu→Cu2++2e-,还原反应式:2Fe3++2e-→2Fe2+.并由此实现了化学能与电能的相互转化.据此,回答下列问题:
一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”.如2Fe3++Cu=2Fe2++Cu2+,可拆写为氧化反应式:Cu→Cu2++2e-,还原反应式:2Fe3++2e-→2Fe2+.并由此实现了化学能与电能的相互转化.据此,回答下列问题:(1)将反应Zn+2H+═Zn2++H2↑拆写为两个“半反应式”:其中,氧化反应式为:
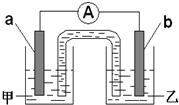
(2)由题(1)反应,设计成原电池如图所示:若电极a为Zn,电极b可选择材料:
(3)由反应2H2+O2
| ||
(4)以惰性材料为电极,电解100mL pH=6的硫酸铜溶液,当电解池内溶液的pH为1时,电极上析出的铜的质量为
(7分)请按要求完成下列反应的式子。
(1)银锌纽扣电池(总反应:Ag2O+Zn= 2Ag+ZnO,电解质溶液:氢氧化钾)的正极反应:______________________________________________________
(2)电解以下溶液:
A. 当电解质溶液为硝酸银溶液、阳极材料为银、阴极材料为铜的阳极反应:______________________________________________________
B. 当电解质溶液为氯化钠溶液、阳极阴极材料均为石墨的阴极反应:
______________________________________________________
C. 将A中的阳极材料改为石墨,其它条件不变时的电解总反应:
______________________________________________________
(3)请你任选一种离子,这种离子既能电离又能水解,分别写出其电离与水解的离子方程式:
电离:______________________________________________________
水解:______________________________________________________
(4)已知每分解1g NH4NO3晶体放出0.53 kJ(298K,101KPa)热量,同时生成笑气(N2O)与液体水。请根据上述信息写出NH4NO3晶体分解的热化学方程式:______________________________________________________
查看习题详情和答案>>
一个完整的氧化还原反应方程式可以拆开,写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”。如2Fe3++Cu===2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e-===Cu2+,还原反应式:2Fe3++2e-=== 2Fe2+。据此,回答下列问题:
⑴将反应Zn+2H+ === Zn2++H2↑拆写为两个“半反应式”:
氧化反应式: ,还原反应式: 。
⑵将反应3NO2+H2O == 2H++2NO3—+NO拆写为两个“半反应式”:
氧化反应式: ,还原反应式: 。
⑶已知某反应的两个“半反应式”为:CH4+10 OH--8e-===CO32-+7H2O,O2+2H2O+4e-=== 4OH—,则氧化还原反应方程式为 。
查看习题详情和答案>>