摘要:25.已知IOH是两性化合物.根据它的性质试回答: (1)写出IOH的两性电离的方程式: (2)完成下列化学方程式: ①.IOH+NaOH: ②.IOH+HCl: ③.IOH+H2S: ④.IOH+KMnO4+H2SO4:
网址:http://m.1010jiajiao.com/timu3_id_146583[举报]
有A、B、C、D、E五种短周期元素,已知A是构成化合物种类最多的元素,其原子最外层电子数是次外层电子数的2倍;E的最高正价和最低负价代数和为4;C与E同主族;B与D同主族;D+与氖原子具有相同的电子层结构;B元素原子的电子层数与族序数相等.试回答:
(1)元素符号:A
(2)写出C在元素周期表中的位置
(3)C、D、E原子半径由大到小的顺序是:
(4)写出AC2的电子式: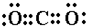
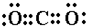 ; B、C、D所形成的化合物的电子式
; B、C、D所形成的化合物的电子式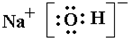
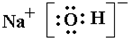 ,并写出所含化学键的类型
,并写出所含化学键的类型
(5)写出A和D两种元素的最高价氧化物发生氧化还原反应的化学方程式:
查看习题详情和答案>>
(1)元素符号:A
C
C
;BH
H
;ES
S
;(2)写出C在元素周期表中的位置
第二周期第ⅥA族
第二周期第ⅥA族
;(3)C、D、E原子半径由大到小的顺序是:
Na>S>O
Na>S>O
;(用元素符号表示)(4)写出AC2的电子式:
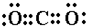
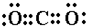
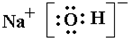
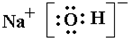
离子键、极性共价键
离子键、极性共价键
;(5)写出A和D两种元素的最高价氧化物发生氧化还原反应的化学方程式:
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2CO2=2Na2CO3+O2
.