摘要:38.科学兴趣小组的同学们对蛋壳的成分开展了有关探究.同学们的实验过程如下: ①将一定量的蛋壳放入容器中,②往其中加入适量的稀盐酸.观察到有较多的气泡产生,③--,④得出结论:蛋壳的主要成分是碳酸盐. (1)请补全第③步的实验内容与现象 . (2)为了测定蛋壳中碳酸钙的质量分数.同学们用蛋壳与足量的稀盐酸充分反应.得到有关数据如下表:(CO2的密度为2克/升) 蛋壳的质量(克) 加入稀盐酸质量(克) 收集到CO2气体体积(升) 7.5 100 1.1 假设二氧化碳全部是由蛋壳中的碳酸钙与盐酸反应产生.小星计算这些蛋壳中碳酸钙的质量分数的过程如下: 解:设该蛋壳中碳酸钙的质量为x CaCO3+2HCl===CaCl2+H2O+CO2↑ 100 28 x 100:28= x:1.1升 x =3.93克.蛋壳中碳酸钙的质量分数==0.524 小星的计算过程中存在明显错误.请你通过列式进行计算.
网址:http://m.1010jiajiao.com/timu3_id_1320621[举报]
 某校八年级物理兴趣小组的同学们对噪声的控制进行了探究.他们从发现比提出问题,做出猜想和假设,设计实验,通过观察、实验和调查走访等途径来收集数据,发现控制噪声污染已经引起社会的高度重视,在市区的主要干道设立噪声监测及分贝数显示装置,以加强每个公民控制噪声的环保意识,控制噪声方面已经采取了许多有效的措施:①将噪声严重的工厂迁出市区;②未装消音设备的机车不得驶入市区;③在市区内不安装高音喇叭,车辆尽量少鸣喇叭; ④积极搞好城市绿化; ⑤采用多孔建筑材料加强隔音;⑥在嘈杂的环境中工作的人们带上耳罩、耳塞等.
某校八年级物理兴趣小组的同学们对噪声的控制进行了探究.他们从发现比提出问题,做出猜想和假设,设计实验,通过观察、实验和调查走访等途径来收集数据,发现控制噪声污染已经引起社会的高度重视,在市区的主要干道设立噪声监测及分贝数显示装置,以加强每个公民控制噪声的环保意识,控制噪声方面已经采取了许多有效的措施:①将噪声严重的工厂迁出市区;②未装消音设备的机车不得驶入市区;③在市区内不安装高音喇叭,车辆尽量少鸣喇叭; ④积极搞好城市绿化; ⑤采用多孔建筑材料加强隔音;⑥在嘈杂的环境中工作的人们带上耳罩、耳塞等.(1)由上述兴趣小组提供的材料分析论证,可以得出减弱噪声的三条途径:其中
①②③
①②③
是在声源处减弱噪声,④⑤
④⑤
是在传播过程中减弱噪声,⑥
⑥
是在人耳处减弱噪声.(填序号)(2)如图所示,它是一种什么装置?
(3)这种装备反映声音的什么特征?显示数字的单位是什么?
(4)在教室里上课,室外常有噪声干扰,请你向学校提出两种减少学校噪声干扰的合理化建议:
①
关闭门窗,拉上窗帘
关闭门窗,拉上窗帘
;②
可在校园内、外广泛植树
可在校园内、外广泛植树
.学过电学知识后,物理兴趣小组的同学们对身边的有关现象产生了浓厚的探究欲望:
(1)图示是一种调节Mp3音量兼开关的调节器,小明拆开后发现它实际上是一个旋钮型
(2)在物理课外活动中,小刚把两种不同的金属片A、B插入橙子,制成“水果电池”,并用电压表测量水果电池的电压为0.8V,如下图所示,试在图中画出此时电压表指针的位置,金属片A是“水果电池”的

查看习题详情和答案>>
(1)图示是一种调节Mp3音量兼开关的调节器,小明拆开后发现它实际上是一个旋钮型
变阻器
变阻器
.当顺时针转动旋钮触片时,Mp3的音量变大,是将接线柱BC
BC
接入电路.(2)在物理课外活动中,小刚把两种不同的金属片A、B插入橙子,制成“水果电池”,并用电压表测量水果电池的电压为0.8V,如下图所示,试在图中画出此时电压表指针的位置,金属片A是“水果电池”的
负
负
极.关于水果电池,请你再提出一个值得探究的问题水果电池的电压与金属种类是否有关?
水果电池的电压与金属种类是否有关?

学过电学知识后,物理兴趣小组的同学们对身边的有关现象产生了浓厚的探究欲望:
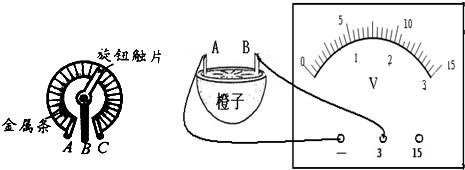
(1)图示是一种调节Mp3音量兼开关的调节器,小明拆开后发现它实际上是一个旋钮型______.当顺时针转动旋钮触片时,Mp3的音量变大,是将接线柱______接入电路.
(2)在物理课外活动中,小刚把两种不同的金属片A、B插入橙子,制成“水果电池”,并用电压表测量水果电池的电压为0.8V,如下图所示,试在图中画出此时电压表指针的位置,金属片A是“水果电池”的______极.关于水果电池,请你再提出一个值得探究的问题______
查看习题详情和答案>>
某校八年级物理兴趣小组的同学们对噪声的控制进行了探究.他们从发现比提出问题,做出猜想和假设,设计实验,通过观察、实验和调查走访等途径来收集数据,发现控制噪声污染已经引起社会的高度重视,尤其是城市在控制噪声方面已经采取了许多有效的措施:①将噪声严重的工厂迁出市区;②积极搞好城市绿化;③在嘈杂的环境中工作的人们带上耳罩、耳塞;④在市区内不安装高音喇叭,车辆尽量少鸣喇叭;⑤对噪声较大的机器安装消音器并限制使用;⑥采用多孔建筑材料加强隔音等.
(1)由上述兴趣小组提供的材料分析论证,可以得出减弱噪声的三条途径:其中______是在声源处减弱噪声,______是在传播过程中减弱噪声,______是在人耳处减弱噪声.
(2)如图所示,在闹市区的主要干道设立噪声监测及分贝数显示装置,以加强每个公民控制噪声的环保意识,这种装备反映声音的什么特征?显示数字的单位是什么?
(3)在教室里上课,室外常有噪声干扰,请你向学校提出两种减少学校噪声干扰的合理化建议:
①______;
②______.
查看习题详情和答案>>
(1)由上述兴趣小组提供的材料分析论证,可以得出减弱噪声的三条途径:其中______是在声源处减弱噪声,______是在传播过程中减弱噪声,______是在人耳处减弱噪声.
(2)如图所示,在闹市区的主要干道设立噪声监测及分贝数显示装置,以加强每个公民控制噪声的环保意识,这种装备反映声音的什么特征?显示数字的单位是什么?
(3)在教室里上课,室外常有噪声干扰,请你向学校提出两种减少学校噪声干扰的合理化建议:
①______;
②______.

某校八年级物理兴趣小组的同学们对噪声的控制进行了探究.他们从发现比提出问题,做出猜想和假设,设计实验,通过观察、实验和调查走访等途径来收集数据,发现控制噪声污染已经引起社会的高度重视,在市区的主要干道设立噪声监测及分贝数显示装置,以加强每个公民控制噪声的环保意识,控制噪声方面已经采取了许多有效的措施:①将噪声严重的工厂迁出市区;②未装消音设备的机车不得驶入市区;③在市区内不安装高音喇叭,车辆尽量少鸣喇叭; ④积极搞好城市绿化; ⑤采用多孔建筑材料加强隔音;⑥在嘈杂的环境中工作的人们带上耳罩、耳塞等.
(1)由上述兴趣小组提供的材料分析论证,可以得出减弱噪声的三条途径:其中______是在声源处减弱噪声,______是在传播过程中减弱噪声,______是在人耳处减弱噪声.(填序号)
(2)如图所示,它是一种什么装置?
(3)这种装备反映声音的什么特征?显示数字的单位是什么?
(4)在教室里上课,室外常有噪声干扰,请你向学校提出两种减少学校噪声干扰的合理化建议:
①______;
②______.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)由上述兴趣小组提供的材料分析论证,可以得出减弱噪声的三条途径:其中______是在声源处减弱噪声,______是在传播过程中减弱噪声,______是在人耳处减弱噪声.(填序号)
(2)如图所示,它是一种什么装置?
(3)这种装备反映声音的什么特征?显示数字的单位是什么?
(4)在教室里上课,室外常有噪声干扰,请你向学校提出两种减少学校噪声干扰的合理化建议:
①______;
②______.
 查看习题详情和答案>>
查看习题详情和答案>>