摘要:(四)化学量 [典型例题讲解] 例1.按要求用正确的化学符号表示: 2个氢原子 (3)3个钠离子 3个亚铁离子 (6)n个硫酸根离子 (7)m个氢氧根离子 (8)+2价的镁元素 [解析]本题主要考查同学们对化学用语的书写能力.解题关键是要看清化学用语所表达的对象(分子.原子.离子还是化合价).只有分清所表达的对象后.在化学符号前或其它位置加上适当的计量数就能完整地表达意义. 答案:(1)N2 3Na+ (4)4H2O (5)3Fe2+ (6)nSO (7)mOH- (8)Mg+2 例2.下列符号只有微观意义的是( ) A.N B.O2 C.Fe D.2N [解析]元素符号的意义有两点:表示这种元素的一个原子.前者属于宏观意义.后者属于微观意义.N表示氮元素,又表示一个氮原子表示物质铁表示铁元素表示一个铁原子.O2的意义:表示氧气由氧元素组成表示一个氧分子(4)表示一个氧分子由两个氧原子构成.2N仅有微观意义.表示2个氮原子. 答案:D 例3.判断下列化学符号中数字“2 表示的意义.将其序号填在相应的横线上: A.Ca2+ B.NO2 C.2NO D. E. ①表示分子个数的是 ②表示一个离子所带电荷数的是 ③表示元素化合价的是 ④表示一个分子中所含原子个数的是 [解析]对化学用语表示意义的正确理解是解决本题的关键. 答案:①C ②A ③D ④B 例4.一个CO分子的质量为akg.其中氧原子质量为bkg.若以一个碳原子质量的作为标准.则CO的相对分子质量为( ) A. B. C. D. [解析]相对分子质量化学式中各原子的相对原子质量的总和.而相对原子质量是以一种碳原子质量的为标准.其它原子的质量跟它相比较所得的值.所以相对分子质量也是以碳原子质量的为标准.用分子质量除以它所得的值.因此可先求出一个碳原子的质量.碳原子的质量=akg-bkg.则CO的相对分子质量.答案:B 例5.大运河岸边某化工厂甲.乙两车间排放的废水中分别含有较多量的Na2CO3和有毒物质CuSO4.两车间排放的废气中含有较多的SO2等有害气体.环保部门建议选用生石灰.铁屑和水等廉价易得的原料.综合治理上述污染.并回收得到的铜和亚硫酸钠等有用物质.写出实现上述要求的化学方程式. [解析]书写化学方程式关键要从分析废水.废气中所含物质(CuSO4.Na2CO3.SO2)与所给原料之间的相互反应规律入手.同时考虑最终能否得到所需的副产品Cu和Na2SO3. 答案:Fe+CuSO4=Cu+FeSO4 CaO+H2O=Ca(OH)2 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH SO2+2NaOH=Na2SO3+H2O [综合测试]
网址:http://m.1010jiajiao.com/timu3_id_13098[举报]
 10、将洗净的碎鸡蛋壳放到足量的稀盐酸中,立即用沾有澄清石灰水的玻璃片盖住,如图所示.能解释实验现象的的化学方程式是( )
10、将洗净的碎鸡蛋壳放到足量的稀盐酸中,立即用沾有澄清石灰水的玻璃片盖住,如图所示.能解释实验现象的的化学方程式是( )①CaCO3+HCl=CaCl+CO2↑+H2O
②CaCO3+2HCl=CaCl2+CO2↑+H2O
③CaCl2+CO2+H2O=CaCO3↓+HCl
④CO2+Ca(OH)2=CaCO3↓+H2O.
查看习题详情和答案>>
分离、除杂提纯和检验是化学实验的重要环节.下面实验设计能够达到目的是( )
| 实验内容 | 实验设计 | |
| A | 除去粗盐中的沙子 | 溶解、过滤 |
| B | 提纯久置变质的氢氧化钠溶液 | 先加入足量氯化钙溶液,充分反应后,过滤 |
| C | 验证某溶液为稀盐酸 | 先测溶液的pH<7,再加入锌粒 |
| D | 分离二氧化碳和一氧化碳混合物 | 先用氢氧化钠溶液吸收掉二氧化碳分离出一氧化碳,再向该氢氧化钠溶液加足量稀盐酸“释放”出二氧化碳 |
| A、A | B、B | C、C | D、D |
近几年,为了使汽油燃烧的更加充分而且减少燃烧过程产生的有害物质,人们在汽油中点燃掺入一定量的乙醇并称之为乙醇汽油.乙醇燃烧的化学方程式为:C2H5OH+xO2
2CO2+3H2O,则每消耗2mol乙醇,需要氧气的物质的量为( )
| 高温 |
| A、3mol | B、6mol |
| C、7mol | D、6.5mol |
通过化学学习,应该知道有多种途径可以制取氧气.如:
A.电解水 B.分离空气 C.加热高锰酸钾 D.分解过氧化氢 E. .
(1)相信你在E处还可以写出另一种制取氧气的方法;其中, 是发生的物理变化.
同时,写出其他四种反应的文字表达式,及其反应类型
;
;
;
;
(2)若用甲图装置加热高锰酸钾制取氧气,实验结束,停止加热时要先把导管移出水面,其理由是 ,此时发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是 ;
(3)若分解过氧化氢制取氧气,供选用的装置如下:
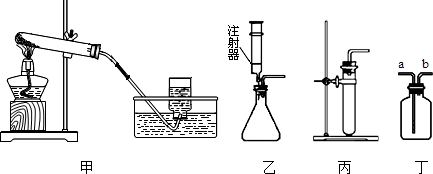
要得到平稳的氧气流,应选用的发生装置是 (选填“乙”或“丙”);
若用丁收集生成的氧气,气体应从 (选填“a”或“b”)端导入.
(4)用排水法收集氧气,当气泡 时,再开始收集;
(5)研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:
用足量等体积H2O2溶液制取相同体积O2所需的时间
问题:从上表中能得出哪些结论?(只任写一条即可)
.
查看习题详情和答案>>
A.电解水 B.分离空气 C.加热高锰酸钾 D.分解过氧化氢 E.
(1)相信你在E处还可以写出另一种制取氧气的方法;其中,
同时,写出其他四种反应的文字表达式,及其反应类型
(2)若用甲图装置加热高锰酸钾制取氧气,实验结束,停止加热时要先把导管移出水面,其理由是
(3)若分解过氧化氢制取氧气,供选用的装置如下:

要得到平稳的氧气流,应选用的发生装置是
若用丁收集生成的氧气,气体应从
(4)用排水法收集氧气,当气泡
(5)研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:
用足量等体积H2O2溶液制取相同体积O2所需的时间
| 浓度 时间(min) 条件 |
30% H2O2 | 15% H2O2 | 5% H2O2 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入a g Fe2O3 | 7.0 | 9.0 | 16.0 |