网址:http://m.1010jiajiao.com/timu3_id_1246720[举报]
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-,横坐标表示加入NaOH的体积)。根据图示判断,下列说法正确的是( )
A.当V(NaOH)=20mL时, 溶液中离子浓度大小关系:
C(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
B.HA-的电离程度小于水解程度
C.滴加过程中当溶液呈中性时,V(NaOH)<20mL
D.当V(NaOH)=40mL时, 向所得溶液加水稀释的过程中pH增大
查看习题详情和答案>>
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-), 根据图示判断,下列说法正确的是
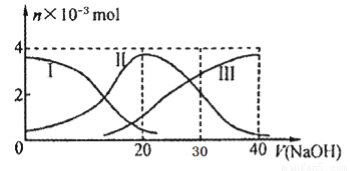
A.H2A在水中的电离方程式是: H2A? === H+? +? HA-? ;? HA-??????  H+? +? A2-
H+? +? A2-
B.当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
D. 当V(NaOH)=30mL时,溶液中存在以下关系:2c(H+)+ c(HA-)+ 2c(H2A)= c(A2-)+ 2 c(OH-)
查看习题详情和答案>>
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-,横坐标表示加入NaOH的体积)。根据图示判断,下列说法正确的是( )
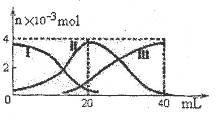
A.当V(NaOH)=20mL时, 溶液中离子浓度大小关系:
C(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
B.HA-的电离程度小于水解程度
C.滴加过程中当溶液呈中性时,V(NaOH)<20mL
D.当V(NaOH)=40mL时, 向所得溶液加水稀释的过程中pH增大
查看习题详情和答案>>
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-,横坐标表示加入NaOH的体积)。根据图示判断,下列说法正确的是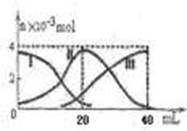
| A.当V(NaOH)=40mL时,c (Na+)+ c(H+)="2" c(A2-)+c(OH-) |
| B.当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| C.滴加过程中当溶液呈中性时,V(NaOH)<20mL |
| D.HA-的电离程度小于水解程度 |
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-), 根据图示判断,下列说法正确的是
A.H2A在水中的电离方程式是: H2A === H+ + HA- ; HA-  H+ + A2-
H+ + A2-
B.当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
D. 当V(NaOH)=30mL时,溶液中存在以下关系:2c(H+)+ c(HA-)+ 2c(H2A)= c(A2-)+ 2 c(OH-)