摘要:28.水是宝贵的自然资源.在工农业生产和日常生活中有着极其广泛的应用. (1)自来水的生产过程大体如下图: 上图过滤池中有活性炭层.活性炭起 作用.该过程中发生 变化.氯化时.通常通入一定量氯气.它与水反应生成盐酸和次氯酸.实验室配制AgNO3溶液时不宜使用自来水.其原因是 . (2)电解水时.加入少量NaOH可以增强水的导电性.现将0.1gNaOH溶解在99.9g水里.接通直流电源后.与电源正极相连的一端放出的气体是 .当溶液中NaOH的质量分数变为0.2%时.有 水被分解. (3)在河旁有甲.乙.丙.丁四座工厂.每个工厂排出的废液只含有Na2CO3.FeCl3.NaOH.HCl中的一种.某环保小组对河水监测时发现:甲处河水呈无色,乙处河水呈红褐色,丙处河水由浑变清,丁处产生气泡.河水澄清.请回答: ①甲工厂排出的废液是一种碱性物质.检验该物质呈碱性可选用的试剂是 . ②乙处河水呈红褐色的化学方程式是 . ③丁处产生气泡的化学方程式是 .
网址:http://m.1010jiajiao.com/timu3_id_12443[举报]
水是宝贵的自然资源,在工农业生产和日常生活中有着及其广泛的应用.
(1)自来水的生产流程大体如图:

如图加入的絮凝剂是一种叫做明矾的净水剂,加明矾的作用是
(2)电解水时,与电源负极相连的一端放出的气体是
(3)溶有较多含钙、镁物质的水是硬水,长期饮用硬水对人体健康不利,一些工业用水也不能用硬水.请设计一简单的实验区分硬水和软水.
(4)我们的家乡泰州既美丽富饶又充满水乡灵韵.正确处理好发展与环保之间的关系,利在当代,功在千秋.请你从保护水资源的角度向全市人民发出两条倡议:①
查看习题详情和答案>>
(1)自来水的生产流程大体如图:

如图加入的絮凝剂是一种叫做明矾的净水剂,加明矾的作用是
溶于水后吸附水中的悬浮杂质而沉降
溶于水后吸附水中的悬浮杂质而沉降
.投药消毒时,通常通入一定量的氯气(Cl2),它与水反应生成盐酸(HCl)和次氯酸(HClO),写出该反应的化学方程式Cl2+H2O=HCl+HClO
Cl2+H2O=HCl+HClO
.高铁酸钾(K2FeO4)是一种理想的水处理剂,高铁酸钾由3
3
种元素组成.(2)电解水时,与电源负极相连的一端放出的气体是
氢气
氢气
,小明同学实验证明该气体具有可燃性,纯净的该气体在空气中燃烧时,发生反应的化学方程式是:2H2+O2
2H2O
| ||
2H2+O2
2H2O
,其所属反应的基本类型是
| ||
化合反应
化合反应
.直接点燃该气体前,应先验纯
验纯
,以防止爆炸.(3)溶有较多含钙、镁物质的水是硬水,长期饮用硬水对人体健康不利,一些工业用水也不能用硬水.请设计一简单的实验区分硬水和软水.
| 实验步骤 | 现象和结论 |
禁用含磷洗衣粉;生活污水、工业污水处理达标后再排放;农业上合理使用农药、化肥
禁用含磷洗衣粉;生活污水、工业污水处理达标后再排放;农业上合理使用农药、化肥
;②一水多用或洗衣机使用节水程序,防止自来水人为流失
一水多用或洗衣机使用节水程序,防止自来水人为流失
.水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的运用,图为自来水厂净水过程示意图: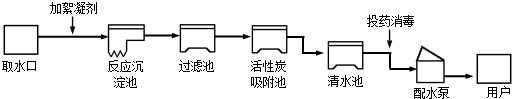
(1)上图吸附池内的活性炭起
(2)自来水厂常用的消毒剂有二氧化氯(ClO2)、漂白粉、“84消毒液”等.ClO2 中氯元素的化合价为
(3)家庭生活中可以用
查看习题详情和答案>>

(1)上图吸附池内的活性炭起
吸附
吸附
作用,经沉淀、过滤等净化处理后所得的不是
不是
纯水(填“是”或“不是”).(2)自来水厂常用的消毒剂有二氧化氯(ClO2)、漂白粉、“84消毒液”等.ClO2 中氯元素的化合价为
+4
+4
.(3)家庭生活中可以用
肥皂水
肥皂水
检验某水样是硬水还是软水.水是宝贵的自然资源,在工农业生产和日常生活中有着广泛的运用.图为自来水厂净水过程示意图:

(1)上图吸附池内的活性炭起
(2)可以降低水硬度的方式是
(3)家庭生活中可以用
(4)有些科学家预言:“世界上最后一滴水就是人类的眼泪.”这句话警示我们应树立保护水资源的意识:一是节约用水,二是防止水体污染.请你举一例生活中节约用水的做法:
查看习题详情和答案>>

(1)上图吸附池内的活性炭起
吸附
吸附
作用,经沉淀、过滤等净化处理后所得的水不是
不是
(填“是”或“不是”)纯水.(2)可以降低水硬度的方式是
煮沸、蒸馏
煮沸、蒸馏
.(3)家庭生活中可以用
肥皂水
肥皂水
检验某水样是硬水还是软水.(4)有些科学家预言:“世界上最后一滴水就是人类的眼泪.”这句话警示我们应树立保护水资源的意识:一是节约用水,二是防止水体污染.请你举一例生活中节约用水的做法:
一水多用
一水多用
.水是宝贵的自然资源,在工农业生产和日常生活中有着及其广泛的应用.自来水的生产流程大体如下图:
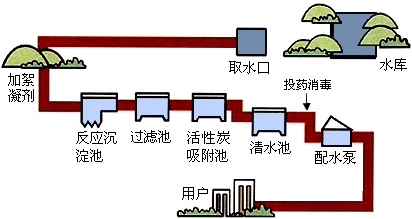
上图加入的絮凝剂是一种叫做明矾的净水剂,加明矾的作用是
查看习题详情和答案>>

上图加入的絮凝剂是一种叫做明矾的净水剂,加明矾的作用是
溶于水形成的胶体能将水中的不溶性固体杂质吸附在其表面,加快沉降
溶于水形成的胶体能将水中的不溶性固体杂质吸附在其表面,加快沉降
.活性炭的作用是吸附
吸附
.水是宝贵的自然资源,在工农业生产和生活中有着极其广泛的应用.节约用水、保护水资源是每个公民应尽的义务

(1)电解水的实验装置如图所示,根据图回答:
①收集到d气体名称是
(2)海水、河水、湖水都是天然水,天然水是
(3)根据资料一和资料二的数据,分析浙江省的水资源紧缺程度为
(4)制药时为了在不超过80℃温度下从溶液中除去水分而提取抗菌素,采用的方法是
(5)水是良好的溶剂.在①70%的酒精 ②食盐水 ③碘酒 ④糖水等几种溶液中,溶剂是水的是
查看习题详情和答案>>
| 紧缺性 | 极度缺水 | 重度缺水 | 中度缺水 | 轻度缺水 |
| 人均水量/(米3/年) | <500 | 500~1000 | 1000~1700 | 1700~3000 |
| 资料一:我国部分省市人均水量图 | ||||

(1)电解水的实验装置如图所示,根据图回答:
①收集到d气体名称是
氢气
氢气
.②电解水的实验说明水是由氢元素和氧元素
氢元素和氧元素
组成的.③检验c试管内气体的方法是用带火星的木条,看是否复燃
用带火星的木条,看是否复燃
.④图中现象表明实验是已进行
已进行
(选填“未开始”或“已进行”)一段时间”.(2)海水、河水、湖水都是天然水,天然水是
混合物
混合物
(填“纯净物”或“混合物”)(3)根据资料一和资料二的数据,分析浙江省的水资源紧缺程度为
轻度缺水
轻度缺水
.(4)制药时为了在不超过80℃温度下从溶液中除去水分而提取抗菌素,采用的方法是
降低
降低
(选填“升高”或“降低”)容器内的气压,使水的沸点低于80℃.(5)水是良好的溶剂.在①70%的酒精 ②食盐水 ③碘酒 ④糖水等几种溶液中,溶剂是水的是
①②④
①②④
.氢氧化钙属于微溶物质,它的溶解度随温度的升高而减小
减小
.