摘要: 33.8克NaCl和Na2CO3的混合物与125克稀盐酸恰好完全反应,得到溶液150克,求(1)原混合物中Na2CO3的质量(2)若将反应后的溶液稀释成溶质质量分数为8%的溶液,需要水多少克?
网址:http://m.1010jiajiao.com/timu3_id_123455[举报]
海洋是个巨大的宝库,为人类提供了宝贵的自然资源.
(1)食用海鱼摄取的主要营养素是________.
(2)如图1为海水淡化装置,利用的能源是________,获得的蒸馏水属于________.
A.单质 B.化合物 C.混合物
(3)利用海水可制取许多化工产品.用海水制食盐,常通过海水晒盐得到粗盐,粗盐中含有少量的CaCl2、Na2SO4等杂质.除去上述杂质,先加过量的BaCl2溶液除去,再加过量________溶液除去CaCl2和过量的BaCl2,生成的沉淀经________除去,最后加入________调节pH,蒸发、结晶,制得粗盐.
(4)用氯化钠和碳酸氢铵可制备碳酸氢钠和氯化铵,该反应化学方程式可表示为;NaCl+NH4HCO3=NaHCO3+NH4Cl.20℃时,按上述化学方程式中反应物的质量比,向100克水中加入11.7克NaCl和15.8克NH4HCO3,理论上从溶液中提出晶体的质量为________g.
资料:20℃时四种物质的溶解度如下:假设它们同时溶解在水中各自的溶解度不变,
| 物质 | NaCl | NH4CO3 | NH4Cl | NaHCO3 |
| 溶解度 | 36.0 | 21.6 | 37.2 | 9.6 |
①写出氯气置换出溴单质的化学方程式;________;该反应在pH=3的酸性条件下进行,可用________测定反应液的酸碱度.
②吹出的溴和大量空气混合在一起进入吸收塔(吸收塔中发生的反应;Br2+SO2+2H2O?H2SO4+2HBr).根据流程图分析,通入SO2的目的是________.
 查看习题详情和答案>>
查看习题详情和答案>>
一定质量的某化合物完全燃烧,消耗9.6克氧气,生成8.8克二氧化碳和5.4克水.对该化合物的组成判断正确的是( )
| A、含有C、H、O三种元素 | B、只含有C、H两种元素 | C、分子中C、H原子个数比为3:1 | D、以上答案都不正确 |
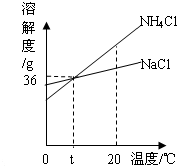 根据右图判断,下列说法错误的是( )
根据右图判断,下列说法错误的是( )| A、NaCl和NH4Cl的溶解度都随温度升高而增大 | B、20℃时,20克NaCl加入到50克水中,搅拌后将全部溶解 | C、t℃时,NH4Cl饱和溶液和NaCl饱和溶液溶质质量分数相等 | D、将20℃时某NH4Cl溶液降温到0℃,其溶质质量分数一定减小了 |
 15、根据如图判断,下列说法错误的是( )
15、根据如图判断,下列说法错误的是( )