摘要:[物质结构与性质] X.Y.Z.W是原子序数依次增大的短周期元素.且互不同族.其中只有一种为金属.X的核外电子排布式为nsnnpn.Z的最外层电子数是其电子层数的2倍. Y原子与Z原子的最外层电子数之和为9.且Y和W单质都可与烧碱溶液反应.请回答以下问题: (1)Y.Z.W的原子半径由大到小的顺序是 (2)XZ2的电子式是 .空间结构为 . 形成晶体时属于 晶体. (3)Y的价电子排布式是 .工业上生产单质Y的原理是 ( (4)试用勒夏特列原理解释用饱和食盐水收集W单质的原理
网址:http://m.1010jiajiao.com/timu3_id_1233087[举报]
[化学-物质结构与性质]X、Y、Z、W是元素周期表前四周期的4种常见元素,其相关信息如下表:

(1)Y位于元素周期表第________周期________族;Y和Z的最高价氧化物对应的水化物的酸性较强的是________(写化学式).
(2)XY2是一种常见溶剂,XY2的分子中存在________个σ键.在H-Y、H-Z两种共价键中,键的极性较强的是________(用化学式表示),键长较长的是________(用化学式表示).
(3)W的基态原子核外电子排布式是________.
W2Y在空气中煅烧生成W2O的化学方程式是:________.
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.已知:
XO(g)+1/2O2(g)=XO2(g);ΔH=-283.0 kJ/mol
Y(s)+O2(g)=YO2(g);ΔH=-296.0 kJ/mol
此反应的热化学方程式是:________.
[化学--选修3:物质结构与性质]X、Y、Z、W是元素周期表中前四周期中的四种元素,其中X的原子中不存在中子,Y原于的最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.请回答下列问题: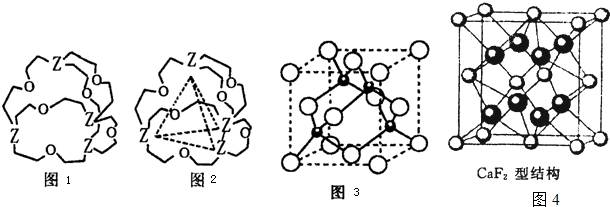
(1)写出Y原子基态时的价电子排布式: .
(2)X和Y可以形成Y2X4分子,1个Y2X4分子中含有σ键的数目为 ,其中Y原子的杂化轨道类型为 .
(3)元素Y的一种氧化物与元素2的一种氧化物互为等电子体,则元素Z的这种氧化物的分子式是 .
(4)图1表示某种含Z有机化合物的结构,其分子内4个Z原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别.下列分子或离子中,能被该有机化合物识别的是 (填标号).
A.CF4 B.CH4 C.NH
D.H2O
(5)元素W的一种氯化物晶体的晶胞结构如图3所示,该氯化物的化学式是 .已知其晶胞边长为a nm,则其晶体密度为 g?cm-3(列出算式即可).该氯化物可与浓盐酸发生非氧化还原反应,生成配合物HnWCl3,则反应的化学方程式为 .
(6)元素金(Au)与W形成的一种合金晶体具有立方最密堆积的结构,在晶胞中W原子处于面心,Au原子处于顶点位置.该晶体中原子之间的作用力是 ;该晶体具有储氢功能,氢原子可进入到由W原子与Au原子构成的四面体空隙中.若将W原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的结构图4相似,该晶体储氢后的化学式应为 .
查看习题详情和答案>>

(1)写出Y原子基态时的价电子排布式:
(2)X和Y可以形成Y2X4分子,1个Y2X4分子中含有σ键的数目为
(3)元素Y的一种氧化物与元素2的一种氧化物互为等电子体,则元素Z的这种氧化物的分子式是
(4)图1表示某种含Z有机化合物的结构,其分子内4个Z原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别.下列分子或离子中,能被该有机化合物识别的是
A.CF4 B.CH4 C.NH
+ 4 |
(5)元素W的一种氯化物晶体的晶胞结构如图3所示,该氯化物的化学式是
(6)元素金(Au)与W形成的一种合金晶体具有立方最密堆积的结构,在晶胞中W原子处于面心,Au原子处于顶点位置.该晶体中原子之间的作用力是
X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
(1)W位于元素周期表第
(2)X的活泼性比Y的
(3)写出Z2Y2的电子式
 ,XY2的结构式
,XY2的结构式
(4)在X原子与氢原子形成的多种分子中,有些分子的核磁共振氢谱显示有两种氢,写出其中一种分子的名称
查看习题详情和答案>>
| 元素 | 相关信息 |
| X | X原子的L层电子数是K层电子数的2倍 |
| Y | Y原子的最外层电子排布式为:nsnnpn+2 |
| Z | Z存在质量数为23,中子数为12的原子核 |
| W | W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
四
四
周期第Ⅷ
Ⅷ
族,其原子最外层有2
2
个电子.(2)X的活泼性比Y的
弱
弱
(填“强”或“弱”);X和Y的气态氢化物中,较稳定的是H2O
H2O
(写化学式).(3)写出Z2Y2的电子式


O=C=O
O=C=O
.(4)在X原子与氢原子形成的多种分子中,有些分子的核磁共振氢谱显示有两种氢,写出其中一种分子的名称
丙烷(或丙炔或2-甲基丙烯或1,2,4,5-四甲基苯等)
丙烷(或丙炔或2-甲基丙烯或1,2,4,5-四甲基苯等)
.氢元素、X、Y的原子也可共同形成多种分子和某种常见无机阴离子,写出其中一种分子与该无机阴离子反应的离子方程式CH3COOH+HCO3-→CH3COO-+H2O+CO2↑
CH3COOH+HCO3-→CH3COO-+H2O+CO2↑
.X、Y、Z、W是四种短周期元素,X原子M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的氢化物水溶液呈碱性;W元素最高正价是+7价.回答下列问题:
(1)元素X原子结构示意图为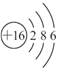
 .
.
(2)元素Y的一种同位素可测定文物年代,这种同位素的符号是
(3)元素Z能与氢元素形成-1价阴离子,该阴离子的电子总数是
(4)元素W的单质与元素X的低价氧化物在水溶液中反应的离子方程式为
(5)ZW3常温下呈液态,可与水反应生成一种酸和一种碱,反应的化学方程式为
(6)探寻物质的性质差异性是学习的重要方法之一.X、Y、Z、W四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是
查看习题详情和答案>>
(1)元素X原子结构示意图为


(2)元素Y的一种同位素可测定文物年代,这种同位素的符号是
146C
146C
.(3)元素Z能与氢元素形成-1价阴离子,该阴离子的电子总数是
10
10
,与该离子电子总数相等的Z与氢形成的微粒是NH3、NH4+
NH3、NH4+
.(4)元素W的单质与元素X的低价氧化物在水溶液中反应的离子方程式为
Cl2+SO2+2H2O═4H++2Cl-+SO42-
Cl2+SO2+2H2O═4H++2Cl-+SO42-
删除此空
删除此空
.(5)ZW3常温下呈液态,可与水反应生成一种酸和一种碱,反应的化学方程式为
NCl3+4H2O═3HClO+NH3?H2O
NCl3+4H2O═3HClO+NH3?H2O
.(6)探寻物质的性质差异性是学习的重要方法之一.X、Y、Z、W四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是
H2CO3
H2CO3
(用酸的分子式表示).X、Y、Z、W是原子序数依次增大的四种短周期元素.X与W可形成正四面体型的共价化合物,Y的次外层电子数等于其最外层和最内层电子数之和的2倍,Y、Z的最外层电子数之和等于W的最外层电子数.回答下列问题:
(1)用化学符号表示X的一种核素
(2)写出Y的单质与X的最高价氧化物反应的化学方程式
(3)Z的单质在W的单质中燃烧,生成的产物中各原子的最外层均达到8电子稳定结构的分子属于
(4)Y与W形成的化合物的电子式为
 .
.
(5)与Z同主族的元素M可与X形成一种化合物,该化合物是新近人工合成的比金刚石硬度大的无机非金属材料,其化学式为
(6)W的氢化物R是实验室一种常用试剂的主要成分,该试剂可用于实验室多种气体的制备,写出实验室制取气体时满足下列条件的离子方程式.
①R作氧化剂:
②R作还原剂:
查看习题详情和答案>>
(1)用化学符号表示X的一种核素
612C或613C或614C
612C或613C或614C
.(2)写出Y的单质与X的最高价氧化物反应的化学方程式
2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
.
| ||
(3)Z的单质在W的单质中燃烧,生成的产物中各原子的最外层均达到8电子稳定结构的分子属于
极性分子
极性分子
(填“极性分子”或“非极性分子”).(4)Y与W形成的化合物的电子式为


(5)与Z同主族的元素M可与X形成一种化合物,该化合物是新近人工合成的比金刚石硬度大的无机非金属材料,其化学式为
C3N4
C3N4
.(6)W的氢化物R是实验室一种常用试剂的主要成分,该试剂可用于实验室多种气体的制备,写出实验室制取气体时满足下列条件的离子方程式.
①R作氧化剂:
2H++Zn═Zn2++H2↑
2H++Zn═Zn2++H2↑
.②R作还原剂:
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
.
| ||