网址:http://m.1010jiajiao.com/timu3_id_1230409[举报]
(2)化合物DY2和DW2的分子空间构型相似,DW2的结构式为___________________。
(3)已知元素W和E的最外层电子数之和与Y和X的最外层电子数之和相差6;又知aX、bY、cZ三种元素,a + b + c=26。化合物XZ3是合成抗禽流感药物“达菲”的中间活性物质,XZ3受撞击会生成一种非金属单质和一种离子化合物X3Z,请写出该反应的化学方程式_______________________。若反应生成标准状况下11.2 L气体单质,则电子转移的物质的量为________________mol。

(2)化合物DY2和DW2的分子空间构型相似,DW2的结构式为________。
(3)已知元素W和E的最外层电子数之和与Y和X的最外层电子数之和相差6;又知aX、bY、cZ三种元素,a + b + c=26。化合物XZ3是合成抗禽流感药物“达菲”的中间活性物质,XZ3受撞击会生成一种非金属单质和一种离子化合物X3Z,请写出该反应的化学方程式____________。若反应生成标准状况下11.2 L气体单质,则电子转移的物质的量为__________mol。
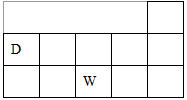
已知W、D、E、X、Y、Z是六种短周期主族元素.元素W与元素Y位于同一主族.X、W、E三元素位于同一周期,且原子序数依次增大.D、W在周期表中的位置如下图.
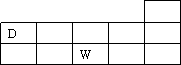
请回答下列问题.
(1)请在上图中用元素符号标明E的位置.
![]() (2)化合物DY2和DW2的分子空间构型相似,DW2的结构式为________.
(2)化合物DY2和DW2的分子空间构型相似,DW2的结构式为________.
(3)已知元素W和E的最外层电子数之和与Y和X的最外层电子数之和相差6;又知aX、bY、cZ三种元素,a+b+c=26.化合物XZ3是合成抗禽流感药物“达菲”的中间活性物质,XZ3受撞击会生成一种非金属单质和一种离子化合物X3Z,请写出该反应的化学方程式________.若反应生成标准状况下11.2 L气体单质,则电子转移的物质的量为________mol.
A、B、C、D、E、F、G七种元素均是短周期元素,且原子序数依次增大。A原子无中子, B、G原子的最外层电子数均为其电子层数的两倍,D、G元素原子的最外层电子数相等。X、Y、Z、W、甲、乙六种物质均由上述元素的两种或三种元素组成,元素B形成的单质M与甲、乙(甲、乙是高中常见的浓酸)均能反应(相对分子质量甲< 乙)转化关系如图(反应条件略去),原子E最外层电子数和其电子层数相等。元素F形成的单质是 “21世纪的能源”,是目前应用最多的半导体材料。请回答下列问题:

(1)A2D的熔沸点比A2G高的原因是 。B、D、G各一个原子构成每原子均满足8电子的分子,其电子式是 。
(2)E4B3和水反应的化学方程式 。
(3)写出M与甲的浓溶液加热时反应的化学方程式 。
(4)X、Y、Z、W属于同一类物质,这类化合物固态时的晶体类型为 ;X、Y、W都能与Z反应,则Z的结构式为 。
(5)已知CH4 (g)+ 2O2 (g)=CO2 (g)+2H2O (l) △H1=a kJ/mol
欲计算反应CH4 (g)+ 4NO (g)=2N2 (g)+CO2 (g)+2H2O (l)的焓变△H2 , 则还需要查找某化合反应的焓变△H3,当反应中各物质化学计量数之比为最简整数比时 △H3 = b kJ/mol,则该反应的热化学方程式为 。
据此计算出△H2 = kJ/mol(用含a和b的式子表示)。
查看习题详情和答案>>
A、B、C、D、E、F、G七种元素均是短周期元素,且原子序数依次增大。A原子无中子, B、G原子的最外层电子数均为其电子层数的两倍,D、G元素原子的最外层电子数相等。X、Y、Z、W、甲、乙六种物质均由上述元素的两种或三种元素组成,元素B形成的单质M与甲、乙(甲、乙是高中常见的浓酸)均能反应(相对分子质量甲< 乙)转化关系如图(反应条件略去),原子E最外层电子数和其电子层数相等。元素F形成的单质是 “21世纪的能源”,是目前应用最多的半导体材料。请回答下列问题: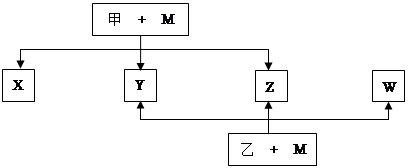
(1)A2D的熔沸点比A2G高的原因是 。B、D、G各一个原子构成每原子均满足8电子的分子,其电子式是 。
(2)E4B3和水反应的化学方程式 。
(3)写出M与甲的浓溶液加热时反应的化学方程式 。
(4)X、Y、Z、W属于同一类物质,这类化合物固态时的晶体类型为 ;X、Y、W都能与Z反应,则Z的结构式为 。
(5)已知CH4 (g)+ 2O2(g)=CO2 (g)+2H2O(l) △H1=a kJ/mol
欲计算反应CH4 (g)+ 4NO (g)=2N2 (g)+CO2 (g)+2H2O(l)的焓变△H2 ,则还需要查找某化合反应的焓变△H3,当反应中各物质化学计量数之比为最简整数比时 △H3 =" b" kJ/mol,则该反应的热化学方程式为 。
据此计算出△H2 = kJ/mol(用含a和b的式子表示)。