网址:http://m.1010jiajiao.com/timu3_id_1228242[举报]
①NA=
| vρ |
| m |
| μ |
| NA△ |
| μ |
| NA |
| v |
| NA |
其中正确的是( )
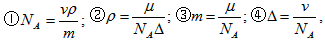
B.①③
C.③④
D.①④
①该气体的物质的量为
| m |
| M |
| m |
| M |
②该气体所含原子总数为
| 2mNA |
| M |
| 2mNA |
| M |
③该气体在标准状况下的体积为
| 22.4m |
| M |
| 22.4m |
| M |
④该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为
| m |
| (m+1000) |
| m |
| (m+1000) |
(2)利用“化学计量在实验中的应用”的相关知识进行填空
①含有6.02×1023个氧原子的H2SO4的物质的量是
②与标准状况下VLCO2所含氧原子数目相同的水的质量是
| 18V |
| 11.2 |
| 18V |
| 11.2 |
③在一定的温度和压强下,1体积X2 (g)跟3体积Y2 (g)化合生成2体积化合物,则该化合物的化学式是
④三种正盐的混合溶液中含有0.2mol Na+、0.25mol Mg2+、0.4mol Cl-、SO42-,则
n(SO42-) 为
(3)假如12C相对原子质量为24,以0.024kg所含12C原子数为阿伏加德罗常数,下列数值肯定不变的是
A.氧气的溶解度
B.气体摩尔体积
C.一定质量的气体体积
D.阿伏加德罗常数
E.O2相对分子质量
F.跟2mLH2 相化合的O2的质量、物质的量.
根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量Ar(Cu)(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),同时生成有一种对环境无害的气体,由此计算Ar(Cu)。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
实验室制取氨气的方程式是:
△
2NH4Cl+Ca(OH)2===2NH3↑+CaCl2+2H2O

请回答下列问题:
(1)检验装置A的气密性的方法是
。
(2)氨气还原炽热氧化铜的化学方程式为 。当4摩尔氨气完全反应.反应中转移的电子数为 mol
(3)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→ 。
(4)在本实验中,若测得m(CuO)=ag,m(H2O)=bg,则Ar(Cu)= 。
(5)在本实验中,使测定结果Ar(Cu)偏大的是_______________(填序号)。
①CuO未完全起反应 ②CuO不干燥 ③CuO中混有不反应的杂质
④碱石灰不干燥 ⑤NH4C1与Ca(OH)2混合物不干燥
(6)在本实验中,还可通过测定______________和_____________,或_______________和_______________达到实验目的。
查看习题详情和答案>>自然界存在一种被称为白云石的矿石,其化学式是xCaCO3·yMgCO3.以它为原料,可制取耐火材料等.
(1)称取Mg白云石,经充分加热,可以生成耐火材料MgO多少摩尔?(用含m、x、y的代数式表示).
(2)称取27.6 g白云石,高温加热到质量不再变化,收集到CO2体积6.72L(标准状况),求白云石的化学式(取x、y的最小正整数比).
(3)将上述收集到的6.72L CO2通入200 mL 2.25 mol/L NaOH溶液中,充分反应后,试确定溶液中的溶质及其物质的量之比(不考虑离子的水解).
(4)已知:CaO+3C![]() CaC2+CO;2MgO+5C
CaC2+CO;2MgO+5C![]() Mg2C3+2CO.
Mg2C3+2CO.
若称取白云石Mg,研碎后与过量炭粉混合,放在特定仪器中隔离空气强热一段时间后,测得白云石分解率为a,生成VL(标准状况)一氧化碳.
①试列出V的计算式(用含m、a的代数式表示)
②请在下图中画出V和a的关系图.
