摘要: 今天是实验室的开放日.某小组的同学利用下列装置进行实验. (1)写出图中指定仪器的名称:① ,② , (2)要制取干燥的H2.并用H2还原氧化铜.应选取的装置为 .在氢气还原氧化铜的过程中.同学们能观察到的现象是 . (3)若制取氢气时需要100g 9.8%的稀硫酸.配制上述稀硫酸需要98%的浓硫酸(密度为1.84g/cm3) mL.配制过程中.除上图装置中的仪器外.还缺少的仪器有 . ①天平 ②胶头滴管 ③药匙 ④10mL量筒 ⑤100mL量筒 (4)还原氧化铜的实验结束后.同学们发现得到的铜中还混有未反应的氧化铜.为了得到纯净的铜.他们进行了以下实验操作: 操作 简答 ①将反应后的固体放入烧杯中.加入足量的稀硫酸.搅拌.使其充分反应. 加足量稀硫酸的目的是: ②将操作①中所得的混合物过滤. 滤液中所含有的溶质是: ③将操作②所得的滤渣洗涤.烘干.得到纯净的铜. A组 46. 某元素原子结构示意图为 .则x的值为 .根据元素原子结构示 意图.不能直接获得的信息是 . A. 核电荷数 B. 相对原子质量 C. 电子层数 D. 最外层电子数
网址:http://m.1010jiajiao.com/timu3_id_122337[举报]
今天是实验室的开放日,某小组的同学利用下列装置进行实验.
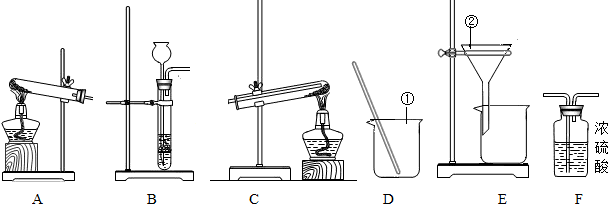
(1)写出图中指定仪器的名称:①________;②________;
(2)要制取干燥的H2,并用H2还原氧化铜,应选取的装置为________(填装置编号).在氢气还原氧化铜的过程中,同学们能观察到的现象是________.
(3)若制取氢气时需要100g 9.8%的稀硫酸,配制上述稀硫酸需要98%的浓硫酸(密度为1.84g/cm3)________mL.配制过程中,除上图装置中的仪器外,还缺少的仪器有________(填序号).
①天平 ②胶头滴管 ③药匙 ④10mL量筒 ⑤100mL量筒
(4)还原氧化铜的实验结束后,同学们发现得到的铜中还混有未反应的氧化铜.为了得到纯净的铜,他们进行了以下实验操作:
| 操作 | 简答 |
| ①将反应后的固体放入烧杯中,加入足量的稀硫酸,搅拌,使其充分反应. | 加足量稀硫酸的目的是:________ |
| ②将操作①所得的混合物过滤. | 滤液中所含有的溶质是:________ |
| ③将操作②所得的滤渣洗涤、烘干,得到纯净的铜, |
19、今天是实验室的开放日,某小组的同学利用下列装置进行实验.

(1)写出图中指定仪器的名称:①
(2)要制取干燥的H2,并用H2还原氧化铜,应选取的装置为
(3)若制取氢气时需要100g 9.8%的稀硫酸,配制上述稀硫酸需要98%的浓硫酸(密度为1.84g/cm3)
①天平 ②胶头滴管 ③药匙 ④10mL量筒 ⑤100mL量筒
(4)还原氧化铜的实验结束后,同学们发现得到的铜中还混有未反应的氧化铜.为了得到纯净的铜,他们进行了以下实验操作:
查看习题详情和答案>>

(1)写出图中指定仪器的名称:①
烧杯
;②漏斗
;(2)要制取干燥的H2,并用H2还原氧化铜,应选取的装置为
B、F、C
(填装置编号).在氢气还原氧化铜的过程中,同学们能观察到的现象是黑色固体变红色,试管口有水滴
.(3)若制取氢气时需要100g 9.8%的稀硫酸,配制上述稀硫酸需要98%的浓硫酸(密度为1.84g/cm3)
5.4
mL.配制过程中,除上图装置中的仪器外,还缺少的仪器有②④⑤
(填序号).①天平 ②胶头滴管 ③药匙 ④10mL量筒 ⑤100mL量筒
(4)还原氧化铜的实验结束后,同学们发现得到的铜中还混有未反应的氧化铜.为了得到纯净的铜,他们进行了以下实验操作:
| 操作 | 简答 |
| ①将反应后的固体放入烧杯中,加入足量的稀硫酸,搅拌,使其充分反应. | 加足量稀硫酸的目的是: 使氧化铜完全反应 |
| ②将操作①所得的混合物过滤. | 滤液中所含有的溶质是: CuSO4、H2SO4 |
| ③将操作②所得的滤渣洗涤、烘干,得到纯净的铜, |
今天是实验室的开放日,某小组的同学利用下列装置进行实验.
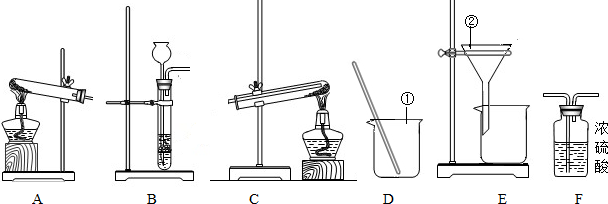
(1)写出图中指定仪器的名称:①______;②______;
(2)要制取干燥的H2,并用H2还原氧化铜,应选取的装置为______(填装置编号).在氢气还原氧化铜的过程中,同学们能观察到的现象是______.
(3)若制取氢气时需要100g 9.8%的稀硫酸,配制上述稀硫酸需要98%的浓硫酸(密度为1.84g/cm3)______mL.配制过程中,除上图装置中的仪器外,还缺少的仪器有______(填序号).
①天平 ②胶头滴管 ③药匙 ④10mL量筒 ⑤100mL量筒
(4)还原氧化铜的实验结束后,同学们发现得到的铜中还混有未反应的氧化铜.为了得到纯净的铜,他们进行了以下实验操作:
查看习题详情和答案>>

(1)写出图中指定仪器的名称:①______;②______;
(2)要制取干燥的H2,并用H2还原氧化铜,应选取的装置为______(填装置编号).在氢气还原氧化铜的过程中,同学们能观察到的现象是______.
(3)若制取氢气时需要100g 9.8%的稀硫酸,配制上述稀硫酸需要98%的浓硫酸(密度为1.84g/cm3)______mL.配制过程中,除上图装置中的仪器外,还缺少的仪器有______(填序号).
①天平 ②胶头滴管 ③药匙 ④10mL量筒 ⑤100mL量筒
(4)还原氧化铜的实验结束后,同学们发现得到的铜中还混有未反应的氧化铜.为了得到纯净的铜,他们进行了以下实验操作:
| 操作 | 简答 |
| ①将反应后的固体放入烧杯中,加入足量的稀硫酸,搅拌,使其充分反应. | 加足量稀硫酸的目的是:______ |
| ②将操作①所得的混合物过滤. | 滤液中所含有的溶质是:______ |
| ③将操作②所得的滤渣洗涤、烘干,得到纯净的铜, |
(2008?浦东新区二模)今天是实验室的开放日,某小组的同学利用下列装置进行实验.
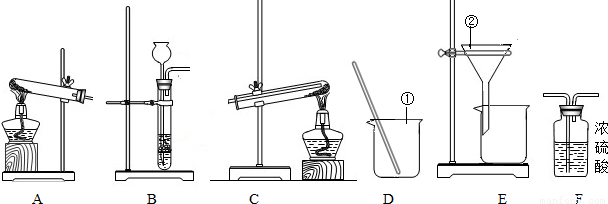
(1)写出图中指定仪器的名称:①;②;
(2)要制取干燥的H2,并用H2还原氧化铜,应选取的装置为(填装置编号).在氢气还原氧化铜的过程中,同学们能观察到的现象是.
(3)若制取氢气时需要100g 9.8%的稀硫酸,配制上述稀硫酸需要98%的浓硫酸(密度为1.84g/cm3)mL.配制过程中,除上图装置中的仪器外,还缺少的仪器有(填序号).
①天平 ②胶头滴管 ③药匙 ④10mL量筒 ⑤100mL量筒
(4)还原氧化铜的实验结束后,同学们发现得到的铜中还混有未反应的氧化铜.为了得到纯净的铜,他们进行了以下实验操作:
查看习题详情和答案>>

(1)写出图中指定仪器的名称:①;②;
(2)要制取干燥的H2,并用H2还原氧化铜,应选取的装置为(填装置编号).在氢气还原氧化铜的过程中,同学们能观察到的现象是.
(3)若制取氢气时需要100g 9.8%的稀硫酸,配制上述稀硫酸需要98%的浓硫酸(密度为1.84g/cm3)mL.配制过程中,除上图装置中的仪器外,还缺少的仪器有(填序号).
①天平 ②胶头滴管 ③药匙 ④10mL量筒 ⑤100mL量筒
(4)还原氧化铜的实验结束后,同学们发现得到的铜中还混有未反应的氧化铜.为了得到纯净的铜,他们进行了以下实验操作:
| 操作 | 简答 |
| ①将反应后的固体放入烧杯中,加入足量的稀硫酸,搅拌,使其充分反应. | 加足量稀硫酸的目的是: |
| ②将操作①所得的混合物过滤. | 滤液中所含有的溶质是: |
| ③将操作②所得的滤渣洗涤、烘干,得到纯净的铜, |
