网址:http://m.1010jiajiao.com/timu3_id_116253[举报]
方案一:
称取一定量的氢氧化钠样品,加水溶解后,逐滴加入沉淀剂氢氧化钡溶液至不再产生沉淀为止.将沉淀过滤、洗涤、烘干、称量.
则:(1)沉淀洗涤的目的是
方案二:
(2)利用下图装置测定氢氧化钠样品中 Na2CO3的质量分数,则必需的数据有:样品质量、反应前
 锥形瓶及其中各物质的总质量、
锥形瓶及其中各物质的总质量、方案三:
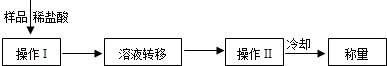
(3)操作Ⅰ中加入稀盐酸应过量的原因是
操作Ⅱ中需要的仪器有铁架台(含铁圈)、玻璃棒、酒精灯和
为计算碳酸钠的质量分数,小刚同学通过列二元一次方程组的办法得到两个表达式:
解:设样品中NaOH的质量为x,Na2CO3的质量为y.
|
请判断这两个方程组中是否存在问题,若有错误,请将纠正后的方程写在横线上:
经计算碳酸钠的质量分数为
氢氧化钠固体常因吸收空气中的二氧化碳而变质.某研究性学习小组为探究氢氧化钠固体样品中的碳酸钠的质量分数(仅考虑样品为NaOH和Na2CO3的混合物),设计了多种实验方案,请结合以下方案回答有关问题:
方案一:
称取一定量的氢氧化钠样品,加水溶解后,逐滴加入沉淀剂氢氧化钡溶液至不再产生沉淀为止.将沉淀过滤、洗涤、烘干、称量.
则:(1)沉淀洗涤的目的是________,若不洗涤,则所测定的样品中碳酸钠的质量分数________(填“偏大”、“偏小”或“无影响”).证明沉淀已经洗涤干净的方法:向最后一次洗涤后的滤液中加入________试剂(填化学式),若无沉淀产生,说明洗涤干净.
方案二:
(2)利用下图装置测定氢氧化钠样品中 Na2CO3的质量分数,则必需的数据有:样品质量、反应前 锥形瓶及其中各物质的总质量、________.该方案有误差,请写出引起误差的一个原因:________.
锥形瓶及其中各物质的总质量、________.该方案有误差,请写出引起误差的一个原因:________.
方案三:

(3)操作Ⅰ中加入稀盐酸应过量的原因是________,
操作Ⅱ中需要的仪器有铁架台(含铁圈)、玻璃棒、酒精灯和________,若该方案中样品质量为9.3g,最终称量冷却后的晶体质量为11.7g.
为计算碳酸钠的质量分数,小刚同学通过列二元一次方程组的办法得到两个表达式:
解:设样品中NaOH的质量为x,Na2CO3的质量为y.

请判断这两个方程组中是否存在问题,若有错误,请将纠正后的方程写在横线上:________.
经计算碳酸钠的质量分数为________.(写出计算过程)
查看习题详情和答案>>
分析:H2SO4和BaCl2反应生成BaSO4和HCl,再用NaOH中和剩余H2SO4时,不能忽视NaOH又和生成HCl发生反应的这个隐蔽反应,而且这个反应是解题时不走弯路的关键。
【常规解法】(l)设BaCl2消耗H2SO4的质量为x,反应生成HCl的质量为y
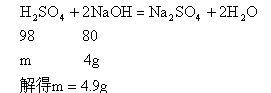 (2)设HCl消耗NaOH的质量为z
(2)设HCl消耗NaOH的质量为z
在反应中共消耗NaOH质量为32g×25%=8g,中和HCl用去4g,尚余4g
 (3)设4gNaOH中和的H2SO4质量为m
(3)设4gNaOH中和的H2SO4质量为m
硫酸中溶质的质量分数为
 答案:(略)
答案:(略)
【解法二】此题稍加分析,即可一步解出:用BaCl2的量不能求出H2SO4的量是因BaCl2不足量,而用NaOH的量却可求出H2SO4的量,因二者是完全中和的反应。之所以可用NaOH 而H+并未参加反应,而H+却恰好被NaOH中和完全,所以可据与NaOH的中和反应求H2SO4的量。
而H+并未参加反应,而H+却恰好被NaOH中和完全,所以可据与NaOH的中和反应求H2SO4的量。
设:H2SO4的量为x

硫酸中溶质的质量分数为 答案:(略)
答案:(略)
分析:天平平衡问题的计算一般指反应前天平已处于平衡,向托盘两边烧杯中加入物质后,引起烧杯内物质净增的变化量,从而确定天平能否再处于平衡。烧杯内物质净增质量=加入物质质量-放出气体质量,当左边净增质量=右边净增质量时,天平处于平衡;当左边净增质量>右边净增质量,天平指针会向左边偏转。
(1)当m1=m2=a时,要判断天平指是否偏转,关键要判断两边放出气体的质量是否相等。
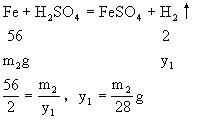
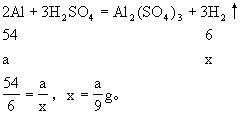 设ag铝片生成氢气质量为x,ag铁片生成氢气质量为y。
设ag铝片生成氢气质量为x,ag铁片生成氢气质量为y。

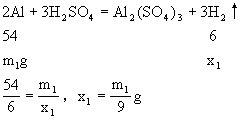 乙烧杯中物质的质量大,指针偏向乙烧杯。
乙烧杯中物质的质量大,指针偏向乙烧杯。
(2)若要指针不偏转,则要求甲、乙两烧杯中物质净增质量相等。设m1 g铝片生成氢气质量为x1,m1 g铁片生成氢气质量为y1。
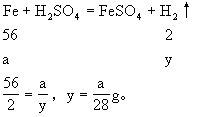
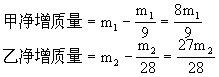
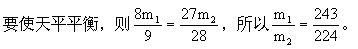 答:(1)偏乙;等质量的Al和Fe比较,Al反应产生的H2多些。 (2)243:224。
答:(1)偏乙;等质量的Al和Fe比较,Al反应产生的H2多些。 (2)243:224。