摘要:25. K2CO3+H2SO4== K2SO4+ CO2↑+ H2O 44.8%.87
网址:http://m.1010jiajiao.com/timu3_id_11591[举报]
 11、某探究小组的同学用H2SO4、Ba(NO3)2、NaOH、K2CO3四种溶液进行“复分解反应发生条件”及应用的实验探究.
11、某探究小组的同学用H2SO4、Ba(NO3)2、NaOH、K2CO3四种溶液进行“复分解反应发生条件”及应用的实验探究.(1)将四种溶液两两混合,其中用H2SO4与另三种溶液分别混合的现象如下:
| Ba(NO3)2 | NaOH | K2CO3 | |
| H2SO4 | 白色沉淀 | 无明显现象 | 产生气体 |
H2SO4+Ba(NO3)2=BaSO4↓+2HNO3
.②实验中的H2SO4与NaOH混合“无明显现象”实际上发生了化学反应,其反应过程如图所示,反应的实质是H+和OH-结合生成H2O.同理H2SO4与K2CO3发生反应的实质是
H+和CO32-结合生成H2CO3.H2CO3不稳定分解放出二氧化碳
.由此同学们总结得出:复分解反应发生的条件是有沉淀或气体或水生成.(2)若某复分解反应的生成物中有NaCl,则该反应的反应物是
NaOH和HCl,Na2CO3和HCl
(写出两组).(3)若将原四种溶液混合反应后过滤,其滤液经检验:溶液呈碱性且不含Ba2+、SO42-.滤液中除可以肯定存在的离子外,设计实验证明还可能存在的离子
取滤液少量,加入BaCl2溶液,无沉淀产生,再滴入几滴酚酞试液,溶液变红色,则证明溶液中还有OH-;
取滤液少量,加入足量BaCl2溶液,有白色沉淀产生,再取上层清液滴入酚酞试液,若溶液不变色,则证明溶液中还含有CO32-;若溶液变为红色,则证明溶液中同时还有CO32-、OH-
.取滤液少量,加入足量BaCl2溶液,有白色沉淀产生,再取上层清液滴入酚酞试液,若溶液不变色,则证明溶液中还含有CO32-;若溶液变为红色,则证明溶液中同时还有CO32-、OH-
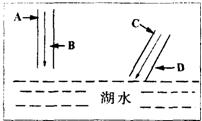 26、如图所示,两条河的河水流入湖中.某校环保小组到河边四家工厂调查,这四家工厂A、B、C、D依次分别排出的废水中含有H2SO4、K2CO3、Ca(OH)2、FeCl3.
26、如图所示,两条河的河水流入湖中.某校环保小组到河边四家工厂调查,这四家工厂A、B、C、D依次分别排出的废水中含有H2SO4、K2CO3、Ca(OH)2、FeCl3.(1)请书写A、B废水汇合处的化学方程式:
K2CO3+H2SO4═K2SO4+H2O+CO2↑
.(2)请书写C、D废水汇合处的化学方程式:
2FeCl3+3Ca(OH)2═2Fe(OH)3↓+3CaCl2
.(3)河边工厂排出的废水有的呈酸性,有的呈碱性.若要检测最终湖水的酸碱性和酸碱度,应如何操作?(请简述操作步骤)
酸碱性:
取少量湖水水样于试管中,滴加1~2滴紫色石蕊试液,观察溶液的颜色
;酸碱度:用玻璃棒蘸取湖水水样滴到pH试纸上,与标准比色卡对比,读出pH值
.(2010?吉林)某校化学兴趣小组选用H2SO4、Ba(NO3)2、NaOH、K2CO3四种溶液进行“复分解反应条件”的实验探究.
[实验设计]
将上面四种溶液两两混合分成6组进行实验,请你在下表横线上将组合⑥填写完整.
[实验记录]
(1)请写出组合③反应的化学方程式:
(2)组合①与组合⑤相同的反应现象是
(3)需要借助指示剂才可判断反应发生的是
[实验结论]
由以上探究实验可得出复分解反应发生的条件:
[反思与拓展]
根据你对物质溶解性的了解,请写出一种不能作为反应物发生复分解反应的盐:
查看习题详情和答案>>
[实验设计]
将上面四种溶液两两混合分成6组进行实验,请你在下表横线上将组合⑥填写完整.
| 组合序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 组合物质 | H2SO4 Ba(NO3)2 |
H2SO4 NaOH |
H2SO4 K2CO3 | Ba(NO3)2 NaOH | Ba(NO3)2 K2CO3 | NaOH NaOH K2CO3 |
(1)请写出组合③反应的化学方程式:
K2CO3+H2SO4=K2SO4+H2O+CO2↑
K2CO3+H2SO4=K2SO4+H2O+CO2↑
;(2)组合①与组合⑤相同的反应现象是
有白色沉淀生成
有白色沉淀生成
;(3)需要借助指示剂才可判断反应发生的是
②
②
(填组合序号).[实验结论]
由以上探究实验可得出复分解反应发生的条件:
两种化合物相互交换成分,有沉淀或气体或水生成
两种化合物相互交换成分,有沉淀或气体或水生成
.[反思与拓展]
根据你对物质溶解性的了解,请写出一种不能作为反应物发生复分解反应的盐:
氯化银
氯化银
.35、某研究性学习小组在探究Na2CO3和K2CO3性质时发现它们的性质相似,如何鉴别它们呢?通过查询资料,得知它们都能跟稀硫酸反应,反应的化学方程式如下:
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑和K2CO3+H2SO4═K2SO4+H2O+CO2↑
小组同学取Na2CO3和K2CO3各10g,分别进行如下实验:

请通过计算得出:(若不能整除,结果精确到0.1)
(1)10.6g Na2CO3完全反应生成CO2质量与10.6g K2CO3完全反应生成CO2的质量哪个多?
(2)反应后所得溶液的质量m1和m2哪个大?
经测定,实验值与理论值相符合.通过上述实验他们知道了可用此法鉴别Na2CO3和K2CO3.
查看习题详情和答案>>
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑和K2CO3+H2SO4═K2SO4+H2O+CO2↑
小组同学取Na2CO3和K2CO3各10g,分别进行如下实验:

请通过计算得出:(若不能整除,结果精确到0.1)
(1)10.6g Na2CO3完全反应生成CO2质量与10.6g K2CO3完全反应生成CO2的质量哪个多?
(2)反应后所得溶液的质量m1和m2哪个大?
经测定,实验值与理论值相符合.通过上述实验他们知道了可用此法鉴别Na2CO3和K2CO3.