题目内容
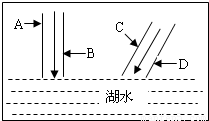
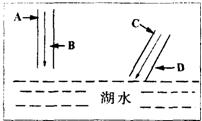 26、如图所示,两条河的河水流入湖中.某校环保小组到河边四家工厂调查,这四家工厂A、B、C、D依次分别排出的废水中含有H2SO4、K2CO3、Ca(OH)2、FeCl3.
26、如图所示,两条河的河水流入湖中.某校环保小组到河边四家工厂调查,这四家工厂A、B、C、D依次分别排出的废水中含有H2SO4、K2CO3、Ca(OH)2、FeCl3.(1)请书写A、B废水汇合处的化学方程式:
(2)请书写C、D废水汇合处的化学方程式:
(3)河边工厂排出的废水有的呈酸性,有的呈碱性.若要检测最终湖水的酸碱性和酸碱度,应如何操作?(请简述操作步骤)
酸碱性:
该反应的化学方程式为:K2CO3+H2SO4═K2SO4+H2O+CO2↑.
(2)C处的废水中的氢氧化钙与D处的废水中的氯化铁反应生成氢氧化铁沉淀和氯化钙.
该反应的化学方程式为:2FeCl3+3Ca(OH)2═2Fe(OH)3↓+3CaCl2.
(3)溶液的酸碱性可以用紫色石蕊试液来检验,酸性溶液能使紫色石蕊试液变红色.因此可以通过如下的操作来检验溶液的酸碱性:取少量湖水水样于试管中,滴加1~2滴紫色石蕊试液,观察溶液的颜色.
溶液的酸碱度可以用pH试纸来检验,具体的操作是:用玻璃棒蘸取湖水水样滴到pH试纸上,与标准比色卡对比,读出pH值.
故答案为:
(1)K2CO3+H2SO4═K2SO4+H2O+CO2↑;
(2)2FeCl3+3Ca(OH)2═2Fe(OH)3↓+3CaCl2;
(3)取少量湖水水样于试管中,滴加1~2滴紫色石蕊试液,观察溶液的颜色;
用玻璃棒蘸取湖水水样滴到pH试纸上,与标准比色卡对比,读出pH值.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(12分)水是人类最宝贵的自然资源 ,多一滴水,就可能多一条生命
,多一滴水,就可能多一条生命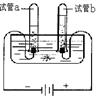
(1)小明利用如图所示的装置探究水的组成。通电一段时间后,试管a与试管b所收集到的气体体积之比约为 ,该实验的化学方程式为
,通过该实验小明得出了许多结论,请你说出一条 。
(2)请回答下列有关水的问题:
①自来水生产过程中先用 的方法除去水中不溶性杂质,再进行消毒。X是一种常见的自来水消毒剂,工业上制取X的化学方程式为:Cl2+2NaClO2=2NaCl+2X,则X的化学式是 。
②地下水硬度过大会影响生产和生活,应软化后使用。
a.检验硬水常用的是物质是 。
b.生活中常用 的方法降低水的硬度。
③我市不少村镇小型河沟中藻类疯长,说明水体富营养化,你认为造成该现象的原因可能有 (正确选项有多个,请选填字母序号)。
(正确选项有多个,请选填字母序号)。
A.化学肥料流失到河中 B.排放的生活污水中有含磷洗涤剂
C.人畜的粪便流失到河中 D.工业废水的排放
④爱护水资源从我做起,下列做法可行的有 (正确选项有多个,请选填字母序号)。
A.洗脸、刷牙时随时关闭水龙头 B.用洗菜、洗衣的水冲厕所、拖地
C.用洗衣机洗一两件衬衫 D.用残茶水浇灌某些花卉
(3)有机物A在氧气中燃烧后只生成二氧化碳和水,为确定A的组成,某同学进行了如下探究。
【猜想】
猜想一:A中只含C、H两种元素
猜想二:A中含C、H、O三种元素
【实验】
|
|
|
|
 燃烧
燃烧【结论】猜想 正确(选填“一”或“二”)。
【反思】有机物A中所含元素的质量比为

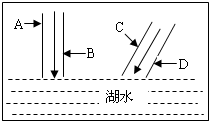 如图所示,两条河的河水流入湖中.某校环保小组到河边四家工厂调查,这四家工厂A、B、C、D依次分别排出的废水中含有H2SO4、K2CO3、Ca(OH)2、FeCl3.
如图所示,两条河的河水流入湖中.某校环保小组到河边四家工厂调查,这四家工厂A、B、C、D依次分别排出的废水中含有H2SO4、K2CO3、Ca(OH)2、FeCl3.