摘要:铁与硫酸铜反应:Fe + CuSO4==Cu + FeSO4 现象:铁条表面覆盖一层红色的物质.溶液由蓝色变成浅绿色. (古代湿法制铜及“曾青得铁则化铜 指的是此反应)
网址:http://m.1010jiajiao.com/timu3_id_115598[举报]
 (2005?绵阳)(1)硫酸亚铁是一种重要的化工原料,可用作杀虫剂、净水剂和木材防腐剂,还可用来治疗缺铁性贫血.工业上用废铁屑与稀硫酸反应制硫酸亚铁,主要反应的化学方程式为
(2005?绵阳)(1)硫酸亚铁是一种重要的化工原料,可用作杀虫剂、净水剂和木材防腐剂,还可用来治疗缺铁性贫血.工业上用废铁屑与稀硫酸反应制硫酸亚铁,主要反应的化学方程式为Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
.废铁屑与硫酸反应产生的气体中含有有毒气体H2S,用CuSO4溶液可以吸收这种气体并产生黑色沉淀,该反应的化学方程式为
H2S+CuSO4═CuS↓+H2SO4
H2S+CuSO4═CuS↓+H2SO4
.(2)为了探究CO的还原性,某同学将绕成螺旋状的铜丝放在酒精灯上加热至铜丝变黑后,立即将铜丝伸入盛满CO的集气瓶中(内装适量澄清石灰水),铜丝又恢复光亮的红色,振荡集气瓶,还可以看到集气瓶中
石灰水变浑浊
石灰水变浑浊
.上述实验过程中,能表明CO具有还原性的反应的化学方程式是
CuO+CO
Cu+CO2
| ||
CuO+CO
Cu+CO2
.将上述表面变黑的铜丝冷却后放入稀硫酸中,可以看到的现象是
| ||
黑色固体逐渐消失
黑色固体逐渐消失
溶液由无色变成蓝色
溶液由无色变成蓝色
,CuO+H2SO4=CuSO4+H2O
CuO+H2SO4=CuSO4+H2O
.(3)一包白色固体可能含有NaCl、CuSO4、NH4NO3、BaC12、K2 C O3中的一种或几种.有同学进行下列实验来确定该固体的成分:
(a)取少许固体放入试管,加入NaOH浓溶液并微热,把湿润的红色石蕊试纸放在试管口,试纸变为蓝色.
(b)取一些白色固体放入试管加水溶解,得无色透明溶液.
(c)向实验b所得溶液中滴2滴酚酞试液,溶液变为红色,再向其中加入过量CaC12溶液,红色褪去,产生白色沉淀.
(d)将实验c所得溶液中的沉淀滤去,向滤液中加入AgNO3溶液,又产生白色沉淀.
①根据以上实验现象判断:这包白色固体中一定有
NH4NO3、K2CO3
NH4NO3、K2CO3
,肯定没有CuSO4、BaC12
CuSO4、BaC12
.②若用这包白色固体配成稀溶液来浇花,可产生的作用是
AC
AC
(填下列选项的字母序号).A.促进花草的茎、叶生长茂盛,叶色浓绿
B.促进花草的根系发达,增强抗寒抗旱能力
C.促进花草生长健壮,茎杆粗硬,增强对病虫害和倒伏的抵抗能力
(4)实验室需用20%的稀硫酸(密度为1.14g?cm-3)460mL,若用如图标签所示的硫酸来配制,则至少需用这种硫酸
58.2
58.2
mL.
某活动小组用废铜制取硫酸铜溶液,实验过程为:
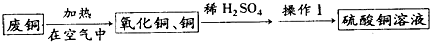
(1)废铜在空气中加热后得到的氧化铜中含有少量铜,原因是
a.加热时氧化铜易分解生成铜
b.铜与氧气没有完全反应
c.加热时铜不能与氧气反应
(2)操作Ⅰ的名称是
(3)盛放硫酸铜溶液不宜用铁制容器的原因是(用化学方程式解释)
(4)向AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生.根据上述现象可得,滤渣中一定含有
查看习题详情和答案>>
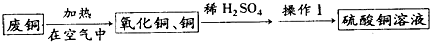
(1)废铜在空气中加热后得到的氧化铜中含有少量铜,原因是
b
b
(填字母序号).a.加热时氧化铜易分解生成铜
b.铜与氧气没有完全反应
c.加热时铜不能与氧气反应
(2)操作Ⅰ的名称是
过滤
过滤
,该操作用到的玻璃仪器有:玻璃棒、烧杯、漏斗
漏斗
.(3)盛放硫酸铜溶液不宜用铁制容器的原因是(用化学方程式解释)
Fe+CuSO4=FeSO4+Cu
Fe+CuSO4=FeSO4+Cu
.(4)向AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生.根据上述现象可得,滤渣中一定含有
Ag
Ag
.11、金属与化合物溶液的反应
(1)铁丝浸入硫酸铜溶液中,现象为浸入溶液中的铁钉表面覆盖
(2)铝丝浸入硫酸铜溶液中,现象为浸入溶液的铝丝表面覆盖一层紫红色的物质,溶液由
(3)铜丝浸入硝酸银溶液中,现象为浸入溶液中的铜丝表面覆盖
(4)结论:①根据以上实验,说明铝、铁、铜、银四种金属的活动性由强到弱的顺序为:
②
(5)注意:①此类反应一定在溶液中进行,
②K、Ca、Na活动性非常强,能同溶液中的水剧烈反应,不能用它们置换化合物溶液中的金属.
(6)置换反应:由
查看习题详情和答案>>
(1)铁丝浸入硫酸铜溶液中,现象为浸入溶液中的铁钉表面覆盖
红色物质
,溶液由蓝色
逐渐变为浅绿色
,反应的化学方程式为Fe+CuSO4═FeSO4+Cu
,反应后金属的质量增加
,溶液的质量减小
.能否有铁制品盛放硫酸铜溶液(或农药波尔多液)不能
.(2)铝丝浸入硫酸铜溶液中,现象为浸入溶液的铝丝表面覆盖一层紫红色的物质,溶液由
蓝色
逐渐变为无色
;反应的化学方程式为2Al+3CuSO4═Al2(SO4)3+3Cu
,反应后金属的质量增加
,溶液的质量减小
.(3)铜丝浸入硝酸银溶液中,现象为浸入溶液中的铜丝表面覆盖
银白色物质
,溶液由无色
逐渐变为蓝色
;反应的化学方程式为Cu+2AgNO3═Cu(NO3)2+2Ag
,反应后金属的质量增加
,溶液的质量减小
.(4)结论:①根据以上实验,说明铝、铁、铜、银四种金属的活动性由强到弱的顺序为:
铝>铁>铜>银
;②
位置在前
的金属能把位于其后
的金属从其化合物溶液中置换出来.(5)注意:①此类反应一定在溶液中进行,
不溶于水
的化合物一般不与金属反应.②K、Ca、Na活动性非常强,能同溶液中的水剧烈反应,不能用它们置换化合物溶液中的金属.
(6)置换反应:由
一种单质
与一种化合物
反应,生成另一种单质和另一种化合物
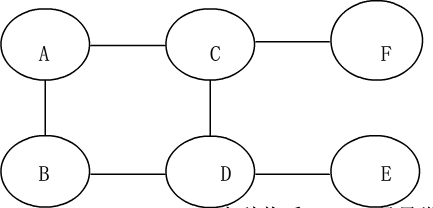
的反应叫做置换反应.23、已知A B C D E F分别是硫酸铜、氢氧化钠、铁、盐酸、氧化铁、二氧化碳中的一种物质,用六个圆表示这六种物质,在图中两圆用“-”连接表示两种物质一定条件下能发生反应.请回答下列问题:
(1)若A与C反应能产生蓝色沉淀,则 A与B能发生置换反应其化学方程式
(2)若D与B反应后溶液的颜色为浅绿色,则E和D反应的现象
(3)在图中标出六种物质的化学式.
查看习题详情和答案>>
(1)若A与C反应能产生蓝色沉淀,则 A与B能发生置换反应其化学方程式
CuSO4+Fe═FeSO4+Cu
(2)若D与B反应后溶液的颜色为浅绿色,则E和D反应的现象
红色粉末逐渐溶解(或消失),溶液的颜色由无色变为黄色
(3)在图中标出六种物质的化学式.

将一根洁净的铁丝分别插入盛有①硫酸锌溶液、②稀盐酸、③硫酸铜溶液的试管中.
(1)请按照顺序分别写出能反应的化学方程式①
(2)铁生锈就是铁与
(3)多数食品容易吸收空气中的水分变潮湿,并与空气中的氧气反应而腐败.生产上多在食品中放入一小包CaO粉末 吸收水生成氢氧化钙,可使食品保持干燥:其反应的化学方程式是
A.生成的铁锈是一种混合物 B.铁粉干燥剂能与水和氧气发生化学反应
C.CaO保护食品的效果比铁粉好 D.两种干燥剂袋上都要有明显的“误食”字样.
查看习题详情和答案>>
(1)请按照顺序分别写出能反应的化学方程式①
不能反应
不能反应
②Fe+2HCl═FeCl2+H2↑
Fe+2HCl═FeCl2+H2↑
属于置换
置换
反应 ③Fe+CuSO4═FeSO4+Cu
Fe+CuSO4═FeSO4+Cu
,观察到的现象为铁的表面附着着一层红色固体,溶液由蓝色变为浅绿色
铁的表面附着着一层红色固体,溶液由蓝色变为浅绿色
.(2)铁生锈就是铁与
氧气
氧气
、水
水
发生复杂的化学变化,生成红棕
红棕
色铁锈,防止钢铁制品生锈的办法有在表面涂保护膜:如自行车的车篓采用刷漆
刷漆
、自行车链条采用涂油
涂油
方法达到隔氧、隔水的目的而防锈.(3)多数食品容易吸收空气中的水分变潮湿,并与空气中的氧气反应而腐败.生产上多在食品中放入一小包CaO粉末 吸收水生成氢氧化钙,可使食品保持干燥:其反应的化学方程式是
CaO+H2O═Ca(OH)2
CaO+H2O═Ca(OH)2
;现已研究成功在食品中放入一小包铁粉(包裹在多孔泡沫中),铁粉吸收水分和氧气变为铁锈,从而保护食品.下列说法不正确的是C
C
A.生成的铁锈是一种混合物 B.铁粉干燥剂能与水和氧气发生化学反应
C.CaO保护食品的效果比铁粉好 D.两种干燥剂袋上都要有明显的“误食”字样.