摘要:氢气 H2 氮气 N2 氯气 Cl2 氧气 O2 臭氧 O3 氦气 He 氖气 Ne 氩气 Ar 碳 C 硅 Si 硫 S 磷 P 碘 I2 钾 K 钙 Ca 钠 Na 镁 Mg 铝 Al 锌 Zn 铁 Fe 铜 Cu 汞 Hg 银 Ag
网址:http://m.1010jiajiao.com/timu3_id_107503[举报]
请完成下列表格,然后总结出气体密度与相对分子质量的关系规律.
气体密度与相对分子质量的关系规律是:
查看习题详情和答案>>
| 气体名称 | 氢气 | 氧气 | 氮气 | 氯气 | 二氧化硫 |
| 化学式 | H2 | O2 | N2 | Cl2 | SO2 |
| 相对分子质量 | 2 | 32 32 |
28 28 |
71 71 |
64 64 |
| 密度(g/L) | 0.0893 | 1.429 | 1.977 | 3.170 | 2.858 |
气体相对分子质量越小(大),其标准状况下的密度越小(大)
气体相对分子质量越小(大),其标准状况下的密度越小(大)
.1909年化学家哈伯在实验室首次将氮气和氢气在一定条件下合成了氨(NH3).常温下,氨是一种无色有刺激性气味的气体,密度小于空气,极易溶解于水,氨和氧气在铂催化剂和一定温度下反应产生一氧化氮和水.
(1)从以上信息中你能总结出氨的物理性质是
(2)下图为实验室制取气体常使用的实验装置:

在实验室中,常用加热氯化铵(固体)和熟石灰(固体)混合物的方法制取氨气.
①采用上述方法制取氨气应选择
②氨气的收集装置应该选用
(3)2007年化学家格哈德?埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖.用 、
、 、
、 分别表示N2、H2、NH3分子.在催化剂表面
分别表示N2、H2、NH3分子.在催化剂表面 (下图中表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
(下图中表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:

①观察上图,可发现合成氨反应过程的顺序为:E→
②综合以上五张图示,请从微观角度描述化学反应的过程:
查看习题详情和答案>>
(1)从以上信息中你能总结出氨的物理性质是
常温下,氨气是无色有刺激性气味的气体,密度小于空气,极易溶解于水
常温下,氨气是无色有刺激性气味的气体,密度小于空气,极易溶解于水
.(2)下图为实验室制取气体常使用的实验装置:

在实验室中,常用加热氯化铵(固体)和熟石灰(固体)混合物的方法制取氨气.
①采用上述方法制取氨气应选择
A
A
(填装置序号)作为气体的发生装置;②氨气的收集装置应该选用
E
E
(填装置序号),理由是密度小于空气,极易溶解于水
密度小于空气,极易溶解于水
.(3)2007年化学家格哈德?埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖.用
 、
、 、
、 分别表示N2、H2、NH3分子.在催化剂表面
分别表示N2、H2、NH3分子.在催化剂表面 (下图中表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
(下图中表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
①观察上图,可发现合成氨反应过程的顺序为:E→
D
D
→A
A
→B
B
→C(在括号中填写其它三张图示的序号);②综合以上五张图示,请从微观角度描述化学反应的过程:
在化学变化中,分子可分解为原子,原子又重新组合成新的分子
在化学变化中,分子可分解为原子,原子又重新组合成新的分子
.写出满足下列条件的化学方程式:
(1)红磷在空气中燃烧
(2)铁丝在氧气中燃烧
(3)用高锰酸钾制取氧气
(4)将钠加入到水中会生成氢氧化钠(NaOH)和氢气:
(5)将氢气和氮气在高温、高压和催化剂的条件下合成氨(NH3):
查看习题详情和答案>>
(1)红磷在空气中燃烧
4P+5O2
2P2O5
| ||
4P+5O2
2P2O5
;
| ||
(2)铁丝在氧气中燃烧
3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
;
| ||
(3)用高锰酸钾制取氧气
2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
;
| ||
(4)将钠加入到水中会生成氢氧化钠(NaOH)和氢气:
2Na+2H2O═2NaOH+H2↑
2Na+2H2O═2NaOH+H2↑
;(5)将氢气和氮气在高温、高压和催化剂的条件下合成氨(NH3):
N2+3H2
2NH3
| ||
| 高温、高压 |
N2+3H2
2NH3
.
| ||
| 高温、高压 |
(2012?无锡)通过对化学的学习,你已掌握了实验室制取气体的有关规律,请结合下图回答有关问题:
(1)图中标有a的仪器名称是
(2)实验室用氯酸钾制取氧气,反应的化学方程式为
(3)实验室用锌和稀硫酸制取氢气,应选择的发生装置是
(4)氨气是一种无色、有刺激性气味、极易溶于水的气体,可用于制氮肥、硝酸、药物和燃料等.
①实验室用加热氯化铵和熟石灰的固体混合物的方法制取氨气,则实验室制取并收集氨气应选择的装置组合是
②工业上用氮气和氢气合成氨气(反应的化学方程式:N2+3H2
2NH3).
实验室模拟合成氨气的流程如下:

流程中“气体的混合”是在F装置中进行的,F装置的作用有三个:一是将氮气和氢气干燥;二是使氮气和氢气充分混合;三是
查看习题详情和答案>>

(1)图中标有a的仪器名称是
集气瓶
集气瓶
.(2)实验室用氯酸钾制取氧气,反应的化学方程式为
2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
,可选择的收集装置是D或
| ||
| △ |
C
C
(填字母,下同).(3)实验室用锌和稀硫酸制取氢气,应选择的发生装置是
A
A
,反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑
Zn+H2SO4═ZnSO4+H2↑
.(4)氨气是一种无色、有刺激性气味、极易溶于水的气体,可用于制氮肥、硝酸、药物和燃料等.
①实验室用加热氯化铵和熟石灰的固体混合物的方法制取氨气,则实验室制取并收集氨气应选择的装置组合是
BE
BE
.②工业上用氮气和氢气合成氨气(反应的化学方程式:N2+3H2
| ||
| 高温、高压 |
实验室模拟合成氨气的流程如下:

流程中“气体的混合”是在F装置中进行的,F装置的作用有三个:一是将氮气和氢气干燥;二是使氮气和氢气充分混合;三是
使氢气和氮气气流稳定
使氢气和氮气气流稳定
,从而提高氮气和氢气的利用率.
1909年化学家哈伯在实验室首次合成了氨.2007年化学家格哈德?埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖.
(1)将氢气和氮气在高温、高压和催化剂的条件下合成氨(NH3).反应的化学方程式为 .
(2)用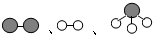 分别表示N2、H2、NH3.观察下图,写出符合在催化剂表面合成氨反应过程的顺序 (将下面五张图按反应过程顺序用序号排列).
分别表示N2、H2、NH3.观察下图,写出符合在催化剂表面合成氨反应过程的顺序 (将下面五张图按反应过程顺序用序号排列).
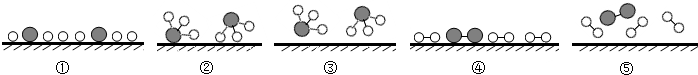
(3)表面化学对于化学工业很重要,它可以帮助我们了解不同的过程.在潮湿的空气里,铁表面吸附了一层薄薄的水膜,同时由于空气中O2的溶解,水膜呈中性.若空气中CO2溶解,水膜呈酸性,写出该反应的化学方程式 .在汽车排气管上安装尾气净化装置,可使尾气中的CO和NO在催化剂表面发生反应,产生两种空气组成的气体,写出该反应的化学方程式 .
查看习题详情和答案>>
(1)将氢气和氮气在高温、高压和催化剂的条件下合成氨(NH3).反应的化学方程式为
(2)用
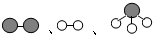 分别表示N2、H2、NH3.观察下图,写出符合在催化剂表面合成氨反应过程的顺序
分别表示N2、H2、NH3.观察下图,写出符合在催化剂表面合成氨反应过程的顺序
(3)表面化学对于化学工业很重要,它可以帮助我们了解不同的过程.在潮湿的空气里,铁表面吸附了一层薄薄的水膜,同时由于空气中O2的溶解,水膜呈中性.若空气中CO2溶解,水膜呈酸性,写出该反应的化学方程式