摘要:1.化工厂用饱和食盐水制取Cl2和NaOH.为了除去粗盐中的泥沙及MgSO4. CaCl2等杂质.可将粗盐溶于水.然后进行如下5项操作:①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液.下列操作顺序正确的是( ) (A)⑤④②①③ (B)④①②⑤③ (C)①⑤④②③ (D)②⑤④①③
网址:http://m.1010jiajiao.com/timu3_id_106027[举报]
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
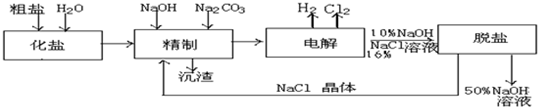
(1)粗盐中主要含有CaCl2、MgCl2杂质,精制工序中加入适量的NaOH和Na2CO3主要目的是为了除去杂质,试分析沉渣中的固体主要有
(2)电解工序中发生2NaCl+2H2O
Cl2+H2+2
(3)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
查看习题详情和答案>>

(1)粗盐中主要含有CaCl2、MgCl2杂质,精制工序中加入适量的NaOH和Na2CO3主要目的是为了除去杂质,试分析沉渣中的固体主要有
CaCO3
CaCO3
、Mg(OH)2
Mg(OH)2
(填化学式);(2)电解工序中发生2NaCl+2H2O
| ||
NaOH
NaOH
(填化学式)(3)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
蒸发
蒸发
、冷却、过滤
过滤
(填写操作名称)除去NaCl;该工业流程中可循环利用的物质是NaCl
NaCl
.氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
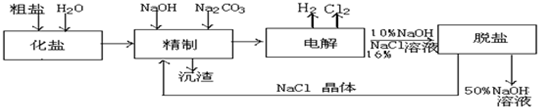
(1)粗盐中主要含有CaCl2、MgCl2杂质,精制工序中加入适量的NaOH和Na2CO3主要目的是为了除去杂质,试分析沉渣中的固体主要有______、______(填化学式);
(2)电解工序中发生2NaCl+2H2O
Cl2+H2+2______(填化学式)
(3)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过______、冷却、______(填写操作名称)除去NaCl;该工业流程中可循环利用的物质是______.
查看习题详情和答案>>

(1)粗盐中主要含有CaCl2、MgCl2杂质,精制工序中加入适量的NaOH和Na2CO3主要目的是为了除去杂质,试分析沉渣中的固体主要有______、______(填化学式);
(2)电解工序中发生2NaCl+2H2O
| ||
(3)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过______、冷却、______(填写操作名称)除去NaCl;该工业流程中可循环利用的物质是______.
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
|
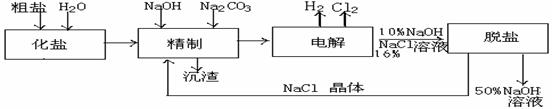 (1)粗盐中主要含有CaCl2、MgCl2杂质,精制工序中加入适量的NaOH和Na2CO3主要目的是为了除去杂质,试分析沉渣中的固体主要有_____、___ ____(填化学式);
(1)粗盐中主要含有CaCl2、MgCl2杂质,精制工序中加入适量的NaOH和Na2CO3主要目的是为了除去杂质,试分析沉渣中的固体主要有_____、___ ____(填化学式); 
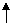 (2)电解工序中发生2NaCl+2H2O====Cl2 +H2 +2______ ___(填化学式)
(2)电解工序中发生2NaCl+2H2O====Cl2 +H2 +2______ ___(填化学式)
(3)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过___ ___、冷却、_ __(填写操作名称)除去NaCl;该工业流程中可循环利用的物质是__________。
查看习题详情和答案>>
氯碱厂电解饱和食盐水溶液制取NaOH的工艺流程示意图如图:
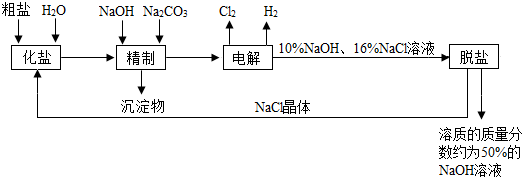
依据图,完成下列填空:
(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和 ,请用适当的数字和符号填空
②2个氯分子 ③粗盐中含有的一种阳离子
④零价的氢元素 ⑤硫酸钠
(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是 .
(3)在电解过程中,发生反应的化学方程式为 ,
电解后溶液的pH .(填“升高”、“不变”、“降低”)
(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是 .
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(5)为了有效地除去氯化镁、氯化钙、硫酸钠,加入试剂的合理顺序为 .
A.先加入NaOH,后加入Na2CO3,再加入钡试剂
B.先加入NaOH,后加入钡试剂,再加入Na2CO3
C.先加入钡试剂,后加入NaOH,再加入Na2CO3
D.先加入钡试剂,后加入Na2CO3,再加入NaOH
(6)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过 (填写操作名称)、冷却、过滤除去NaCl.
(7)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式 .
查看习题详情和答案>>

依据图,完成下列填空:
(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和
②2个氯分子
④零价的氢元素
(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是
(3)在电解过程中,发生反应的化学方程式为
电解后溶液的pH
(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(5)为了有效地除去氯化镁、氯化钙、硫酸钠,加入试剂的合理顺序为
A.先加入NaOH,后加入Na2CO3,再加入钡试剂
B.先加入NaOH,后加入钡试剂,再加入Na2CO3
C.先加入钡试剂,后加入NaOH,再加入Na2CO3
D.先加入钡试剂,后加入Na2CO3,再加入NaOH
(6)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
(7)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式
氯碱厂电解饱和食盐水溶液制取NaOH的工艺流程示意图如图:
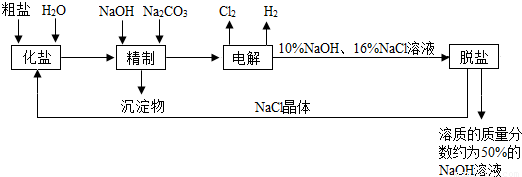
依据图,完成下列填空:
(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和 ,请用适当的数字和符号填空
②2个氯分子 ③粗盐中含有的一种阳离子
④零价的氢元素 ⑤硫酸钠
(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是 .
(3)在电解过程中,发生反应的化学方程式为 ,
电解后溶液的pH .(填“升高”、“不变”、“降低”)
(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是 .
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(5)为了有效地除去氯化镁、氯化钙、硫酸钠,加入试剂的合理顺序为 .
A.先加入NaOH,后加入Na2CO3,再加入钡试剂
B.先加入NaOH,后加入钡试剂,再加入Na2CO3
C.先加入钡试剂,后加入NaOH,再加入Na2CO3
D.先加入钡试剂,后加入Na2CO3,再加入NaOH
(6)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过 (填写操作名称)、冷却、过滤除去NaCl.
(7)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式 . 查看习题详情和答案>>

依据图,完成下列填空:
(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和 ,请用适当的数字和符号填空
②2个氯分子 ③粗盐中含有的一种阳离子
④零价的氢元素 ⑤硫酸钠
(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是 .
(3)在电解过程中,发生反应的化学方程式为 ,
电解后溶液的pH .(填“升高”、“不变”、“降低”)
(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是 .
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(5)为了有效地除去氯化镁、氯化钙、硫酸钠,加入试剂的合理顺序为 .
A.先加入NaOH,后加入Na2CO3,再加入钡试剂
B.先加入NaOH,后加入钡试剂,再加入Na2CO3
C.先加入钡试剂,后加入NaOH,再加入Na2CO3
D.先加入钡试剂,后加入Na2CO3,再加入NaOH
(6)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过 (填写操作名称)、冷却、过滤除去NaCl.
(7)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式 . 查看习题详情和答案>>