摘要:(二)配备练习 1.下列溶液.能使无色酚酞试液变红的是( ) A.石灰水 B.氢氧化钠溶液 C.食醋 D.汽水 2.现有NaOH 溶液.稀硫酸.蒸馏水.若将它们一次鉴别出来.可选用的试剂是( ) A.无色酚酞试液 B.紫色石蕊试液 C.稀盐酸 D.Na2CO3 溶液 3.下列有关盐酸的叙述中错误的是( ) A.浓盐酸是有刺激性气味的液体 B.浓盐酸具有挥发性.在空气中会形成白烟 C.人的胃液中含有少量盐酸.可帮助消化 D.盐酸是氯化氢气体的水溶液 4.下列用途中盐酸和硫酸都具有的是( ) A.金属表面除锈 B.生产化肥 C.制火药 D.干燥剂 5.在4个小烧杯里分别盛有等质量的下列物质.在空气中放置一段时间后.烧杯内物质的总质量显著增加且溶质质量分数减小的是( ) A.浓盐酸 B.浓硫酸 C.石灰水 D.蔗糖溶液 6.将浓硫酸滴在滤纸上.滤纸很快变黑.这说明浓硫酸具有的特性是( ) A.酸性 B.吸水性 C.脱水性 D.氧化性 7.小明想除去自己白衬衫上的铁锈痕迹.在用清水洗涤前.他从家中选择的最合适的物质是 A.汽油 B.食盐水 C.白醋 D.红醋 8.等质量的锌分别与足量的稀盐酸.稀硫酸充分反应.产生氢气的质量关系是( ) A.相等 B.与稀盐酸反应的多 C.与稀硫酸反应的多 D.不能确定 9.下列溶液跟铁片充分反应后.所得溶液质量比反应前溶液质量减轻的是( ) A.稀盐酸 B.稀硫酸 C.FeSO4 溶液 D.CuSO4溶液 10.酒厂用发酵法生产白酒时.需加入适量硫酸来控制酸度.发酵完成后进行蒸馏.即可得到白酒.但不能用盐酸代替硫酸.因为 .
网址:http://m.1010jiajiao.com/timu3_id_103645[举报]
33、常温下,氯气(Cl2)是一种黄绿色气体,有毒,能溶于水.氯气的水溶液叫“氯水”.溶解的氯气部分能与水起反应,生成盐酸与次氯酸(HClO).次氯酸能杀死水里的病菌,所以自来水常用氯气来杀菌消毒.次氯酸还能使某些染料和有机色素褪色,可用作棉、麻和纸张的漂白剂.请回答:
(1)氯气的物理性质(写一点)
(2)若用自来水(密度为1g/cm3)配制1%的下列溶液,溶质质量分数不受影响的是
A.稀盐酸 B.纯碱溶液 C.烧碱溶液 D.硝酸钾溶液
(3)紫色石蕊试液(含有机色素)遇到氯水后,首先变红,但很快又褪色,这是因为
(4)在实验中发现:Br2、I2、Cl2及其化合物之间有如下反应:Br2+2NaI=I2+2NaBr;Cl2+2NaBr=Br2+2NaCl.你是否发现这些反应与金属和盐反应相似,即活泼非金属单质可以把较不活泼的非金属从盐溶液中
查看习题详情和答案>>
(1)氯气的物理性质(写一点)
黄绿色(或气体、能溶于水)
,与水反应的化学方程式Cl2+H2O═HCl+HClO
.(2)若用自来水(密度为1g/cm3)配制1%的下列溶液,溶质质量分数不受影响的是
D
.A.稀盐酸 B.纯碱溶液 C.烧碱溶液 D.硝酸钾溶液
(3)紫色石蕊试液(含有机色素)遇到氯水后,首先变红,但很快又褪色,这是因为
氯水显酸性,使石蕊试液变红,氯水中的次氯酸具有漂白作用,使红色褪去
.(4)在实验中发现:Br2、I2、Cl2及其化合物之间有如下反应:Br2+2NaI=I2+2NaBr;Cl2+2NaBr=Br2+2NaCl.你是否发现这些反应与金属和盐反应相似,即活泼非金属单质可以把较不活泼的非金属从盐溶液中
置换
出来.由此可知,非金属Br2、I2、Cl2的化学活动性由强到弱的顺序为Cl2>Br2>I2
;Cl2与NaI反应的化学方程式为Cl2+2NaI═2NaCl+I2
.
2006年底,我国颁布新的生活饮用水卫生标准,该标准中包含以下内容:
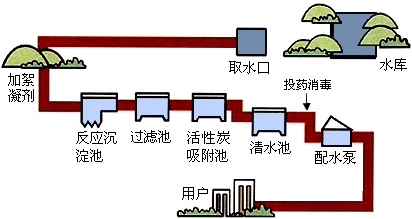
城市住宅饮用水经下图所示过程处理后,质检必须达到国家饮用水标准.

(1)上述净水过程中,能消除天然水臭和味的是 .
(2)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂.与氯气(Cl2)相比,二氧化氯不但具有更强的杀菌能力,而且不会产生对人体有潜在危害的有机氯化物.
①二氧化氯(ClO2)中,氯元素的化合价为 .
②在二氧化氯的制备方法中,有下列两种途径:
方法一:2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O
方法二:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
用上述两种方法制备的二氧化氯,更适合用于饮用水消毒的是 (填“方法一”或“方法二”).
③用氯气做水消毒剂时,发生如下反应:Cl2+H2O=HClO+HCl,若用氯气消毒后的自来水(密度视为1g/cm3)配制溶质质量分数为1%的下列溶液,溶质的质量分数受影响的是 (填字母).
A.稀盐酸 B.碳酸钠溶液 C.氢氧化钠溶液 D.硝酸钾溶液
(3)水质检验员对各项指标进行检验
①检测水的酸碱度应该用 (填序号).
A.紫色石蕊试液 B.无色酚酞试液 C.pH试纸
②天然水中一般都含有Ca2+、Mg2+等离子,当Ca2+、Mg2+总含量超过饮用水硬度标准时,称为不合格.经水质检验员测定1L某地区自来水中含钙元素0.1g,镁元素0.06g,若按24g镁元素相当于40g钙元素换算成硬度,判断该水样 (填“符合”或“不符合”)我国饮用水标准中的总硬度.
查看习题详情和答案>>
| 指标 | 检测项目及单位 | 限值 |
| 微生物指标 | 总大肠杆菌群(MPN/100ml) | 不得检出 |
| 感官性状指标 | 臭和味 | 无异嗅、无异味 |
| 肉眼可见物 | 无 | |
| 一般化学指标 | pH | 不小于6.5且不大于8.5 |
| 总硬度(以CaCO3计)(mg/l) | 450 | |
| 溶解性总固体( mg/l) | 1000 |

(1)上述净水过程中,能消除天然水臭和味的是
(2)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂.与氯气(Cl2)相比,二氧化氯不但具有更强的杀菌能力,而且不会产生对人体有潜在危害的有机氯化物.
①二氧化氯(ClO2)中,氯元素的化合价为
②在二氧化氯的制备方法中,有下列两种途径:
方法一:2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O
方法二:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
用上述两种方法制备的二氧化氯,更适合用于饮用水消毒的是
③用氯气做水消毒剂时,发生如下反应:Cl2+H2O=HClO+HCl,若用氯气消毒后的自来水(密度视为1g/cm3)配制溶质质量分数为1%的下列溶液,溶质的质量分数受影响的是
A.稀盐酸 B.碳酸钠溶液 C.氢氧化钠溶液 D.硝酸钾溶液
(3)水质检验员对各项指标进行检验
①检测水的酸碱度应该用
A.紫色石蕊试液 B.无色酚酞试液 C.pH试纸
②天然水中一般都含有Ca2+、Mg2+等离子,当Ca2+、Mg2+总含量超过饮用水硬度标准时,称为不合格.经水质检验员测定1L某地区自来水中含钙元素0.1g,镁元素0.06g,若按24g镁元素相当于40g钙元素换算成硬度,判断该水样