摘要: 解:(1)产生氢气的质量为98.0g+20.0g-117.8g=0.2g 则标况下氢气的体积为 (2)设生成硫酸锌的质量为x.参加反应的锌的质量为y 65 161 2 y x 0.2g 解得:y = 6.5g x = 16.1g 硫酸锌的质量分数为 答:(1)产生氢气0.2g.在标况下体积为2.2L, (2)反应后所得溶液的溶质的质量分数15.4% .
网址:http://m.1010jiajiao.com/timu3_id_101907[举报]
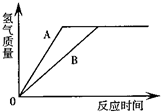 有等质量的A、B两金属,A相对原子质量小于B相对原子质量,将A、B分别放入相同溶度、相同质量的稀硫酸中,在反应中A、B均为正二价,产生氢气的质量随反应时间变化曲线如如图.下列说法正确的是( )
有等质量的A、B两金属,A相对原子质量小于B相对原子质量,将A、B分别放入相同溶度、相同质量的稀硫酸中,在反应中A、B均为正二价,产生氢气的质量随反应时间变化曲线如如图.下列说法正确的是( )
查看习题详情和答案>>
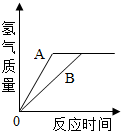
 (2011?南昌)有等质量的A、B两金属,相对原子质量Ar(A)<Ar(B),将A放入质量分数为15%的稀硫酸中,B放入质量分数为15%的稀盐酸中,在反应中A、B均为正二价,产生氢气的质量随反应时间变化曲线如右图.下列说法正确的是( )
(2011?南昌)有等质量的A、B两金属,相对原子质量Ar(A)<Ar(B),将A放入质量分数为15%的稀硫酸中,B放入质量分数为15%的稀盐酸中,在反应中A、B均为正二价,产生氢气的质量随反应时间变化曲线如右图.下列说法正确的是( )
查看习题详情和答案>>
 有等质量的A、B两金属,相对原子质量A<B,将A放入质量分数为15%的稀硫酸中,B放入质量分数为15%的稀盐酸中,在反应中A、B均为正二价,产生氢气的质量随反应时间变化曲线如图.下列说法正确的是 ( )
有等质量的A、B两金属,相对原子质量A<B,将A放入质量分数为15%的稀硫酸中,B放入质量分数为15%的稀盐酸中,在反应中A、B均为正二价,产生氢气的质量随反应时间变化曲线如图.下列说法正确的是 ( )
查看习题详情和答案>>

 大
大