高一化学同步测试原子结构
YCY
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分.共100分,考试用时60分钟.
第Ⅰ卷(选择题,共50分)
一、选择题(本题包括10小题,每小题3分,共30分。每小题只有一个选项符合题意)
1.我国的“神舟五号”载人飞船已发射成功,“嫦娥”探月工程也已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的 ,每百吨
,每百吨 核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氮元素主要以
核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氮元素主要以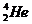 的形式存在。下列说法正确的是 ( )
的形式存在。下列说法正确的是 ( )
A.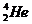 原子核内含有4个质子
原子核内含有4个质子
D. 和
和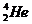 互为同位素
互为同位素
C. 原子核内含有3个中子
原子核内含有3个中子
D.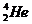 的最外层电子数为2,所以
的最外层电子数为2,所以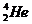 具有较强的金属性
具有较强的金属性
2.据报道,某些建筑材料会产生放射性同位素氡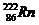 ,从而对人体产生伤害,该同位素原
,从而对人体产生伤害,该同位素原
子的中子数和质子数之差是 ( )
A.136 B.
3.下列离子中,所带电荷数与该离子的核外电子层数相等的是 ( )
A.Al3+ B.Mg2+ C.Be2+ D.H+
4.下列各组物质中,互为同位素的是 ( )
A.重氢、超重氢 B.氧、臭氧 C.红磷、白磷 D.乙酸、丙酸
5.下列有关原子结构的说法,正确的是 ( )
A.稀有气体元素原子的最外层电子数都是8
B.非金属元素的最外层电子数都大于3
C.金属元素的最外层电子数都小于4
D.氢原子的电子云是球形对称的
6.对第n电子电子层, 若它作为原子的最外层, 则容纳的电子数最多与(n-1)层的相同;
当它作为次外层, 则其容纳的电子数比(n+1)层上电子数最多能多10个, 那么第n层
为 ( )
A. L层 B. M层 C. N层 D. 任意层
7.A元素的原子最外层电子数是a,次外层电子数是b;B元素的原子M层电子数是(a-b),
L层电子数是(a+b),则A、B两种元素形成的化合物的化学式可能表示为 ( )
A.B
8.设某元素的原子核内的质子数为m,中子数为n,则下述论断正确的是 ( )
A.不能由此确定该元素的相对原子质量
B.这种元素的相对原子质量为(m+n)g
C.碳原子质量为wg,此原子的质量为(m+n)wg
D.核内中子的总质量小于质子的总质量
9.自然界中钙元素有两种天然同位素: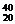 Ca和
Ca和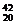 Ca,已知钙元素的近似相对原子质量为
Ca,已知钙元素的近似相对原子质量为
40.08,则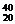 Ca和
Ca和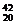 Ca的原子个数比是 ( )
Ca的原子个数比是 ( )
A.12:1 B.24:
10.在离子 RO3n- 中, 共有 x 个核外电子, R 原子的质量数为 A, 则 R 原子核内含有的中
子数目是: ( )
A.A ? x + n + 48 B. A ? x + n + 24
C. A ? x - n ? 24 D. A + x - n ? 24
二、选择题(本题包括5小题,每小题4分,共20分。在每题给出的四个选项中,有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确给满分,但只要选错一个该小题就为0分)
11.周期表中16号元素和4号元素的原子相比较,前者的下列数据是后者的4倍的是( )
A.电子数 B.最外层电子数 C.电子层数 D.次外层电子数
12.X和Y是原子序数大于4的短周期元素,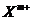 、
、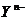 两种离子的核外电子排布相同。下列说法中正确的是 ( )
两种离子的核外电子排布相同。下列说法中正确的是 ( )
A.X的原子半径比Y的原子半径小 B.X和Y的核电荷数之差为m -- n
C.Y原子核内所含质子数比X多 D.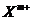 半径比
半径比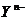 小
小
13.
( )
A.
C.15N与14N互为同位素 D.15N的核外电子数与中子数相同
14.核内中子数为N的R2+离子,质量数为A,则n g它的氧化物中所含质子的物质的量
( )
A.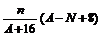 mol B.
mol B.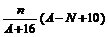 mol
mol
C.(A-N+2)mol D.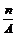 mol
mol
15.若某氖原子的质量是ag,
A.氖元素的原子量一定是
C.该氖原子的摩尔质量是aNAg D.wg该氖原子所含质子数是10w/a
第Ⅱ卷(非选择题 共50分)
三、填空、简答和计算(共8个小题,满分50分)
16.(6分)(1)请写出五种化学性质不同的物质的化学式,这些物质的原子核外都具有10个电子,它们的化学式分别为 、 、 、 、 .
(2)请写出五种具有10个电子的单核带电微粒,并按照半径由大到小排列
_____________________________________
17.(6分)用A.质子数 B.中子数 C.核外电子数 D.最外层电子数 E.电子层数 填写下列空白:
(1)原子种类由 决定; (2)元素种类由 决定;
(3)核电荷数由 决定。 (4)元素的化学性质主要由 决定;
(5)元素的原子半径由 决定; (6)元素的化合价主要由 决定;
18.(6分)(1)原子核外第N电子层最多可容纳 个电子,当N层为最外层时最多可容纳 个电子,当N层为次外层时最多可容纳 个电子。
(2)原子序数在20号以前的元素,原子最外层电子数等于次外层电子数的有____种
(3)最外层电子数是次外层电子数3倍的元素与核电核数为12的元素形成的化合物的化学式_______.
(4)两种元素化合为离子化合物CD,已知CD中所含电子总数为12,C为+1价,CD化合物的化学式是_ ___。
19.(6分).已知An+、B(n+1)+、Cn-、D(n+1)-都具有相同的电子层结构,则A、B、C、D的原子半径由大到小的顺序是 ;离子半径由大到小的顺序是 ;阳离子中氧化性较强的是 ,阴离子中还原性较强的是 _____ 。
20.(6分)设X、Y、Z代表3种元素。已知:①X+和Y-两种离子具有相同的电子层结构;②Z元素原子核内质子数比Y元素原子核内质子数少9个;③Y和Z两元素可以形成四核42个电子的负一价阴离子。据此,请填空:
(1)Y元素是 ,Z元素是 。
(2)由X、Y、Z三元素所形成的含68个电子的盐类化合物之分子式(即化学式)
是
21.(8分)有A、B、C、D、E五种微粒:
①A微粒核内有14个中子,核外M电子层上有2个电子;②B微粒得到2个电子后,其电子层结构与Ne相同;③C微粒带有一个单位的正电荷,核电荷数为11;④D微粒核外有18个电子,当失去1个电子时呈电中性;⑤E微粒不带电,其质数量为1。
试回答下列问题:
(1)依次写出A、E各微粒的符号 、 ;
(2)B、C、E所属元素两两组合时,可形成哪些离子化合物化学式 ;共价化合物化学式 ;
(3)B、C、D所属三种元素共同组合时所形成的物质有多种,请写出其中两种的化学式 .
22.(6分)某元素M所形成的气态单质为双原子分子,共有三种形式,其式量分别为70、72、74,它们的物质的量之比为9∶6∶1,则:
(1)M有 种同位素;
(2)各种同位素的质量数及占的原子数百分比分别为 _____________;?
(3)M2的平均式量为 。
23.(6分)由氧元素的两种同位素16O和18O所形成的两种气体单质18Om、16On,在同温同压同体积时,中子数之比为5:6,求
(1)m :n为多少?
(2)18Om与16On的质量比是多少?
YCY
一、选择题
题号
1
2
3
4
5
6
7
8
9
10
答案
A
B
B
A
D
B
B
A
B
B
二、选择题
题号
11
12
13
14
15
答案
AD
D
C
C
BD
三、空、简答和计算
16.(1)Ne、HF、H2O、NH3、CH4 (2)N3-、O2-、 F-、Na+、Mg2+、Al3+(按照上述顺序写出其中的5个即可)
17.(1)A B;(2)A;(3)A;(4)D;(5)AE;(6)D
18.(1)32,8,18;(2)2;(3)MgO;(4) NaH
19.A>B> D > C; D(n+1)- >Cn-> An+ >B(n+1)+;B(n+1)+,D(n+1)-。
20.(1)氧或O,氯或Cl;(2)KClO4
21. (1)2612Mg、11H?
(2)离子化合物、Na2O、Na2O2;共价化合物、H2O、H2O2
(3)NaClO、NaClO2、NaClO3、NaClO4(写出其中两个即可)
22. (1)2、35、37、 75%、25% (2)71
23. (1) 16O的中子数为8 ,18O的中子数为10。则有:


(2) 