甘肃省兰州一中2009年4月份模拟考试
理科综合试题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
第Ⅰ卷(共126分)
以下数据可供解题时参考:
相对原子质量(原子量):Cu-64
Na-23 O-16 Ba
一、选择题(本题包括13小题。每小题6分,共78分,每小题只有一个选项符合题意)
1.科学家用15N的硝酸盐作为标记物浸泡蚕豆幼苗,追踪蚕豆根尖细胞分裂情况,得到蚕豆根尖分生区细胞连续分裂的有关数据,如下图。下列叙述正确的是
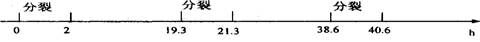
A.高尔基体、线粒体、叶绿体在细胞分裂过程中活动旺盛
B.非等位基因的自由组合可发生在19.3~21.3h
C.O~2h期间,DNA分子始终处于解旋状态
D.蚕豆根尖细胞分裂的一个细胞周期为19.3h
2. 以下各种植物杂交方式及所采取的处理方法不相符合的是
杂交方式 处理方式
A.蛇麻属雌雄异株,若二倍体♀×四倍体♂ 不需套袋,不需去雄
B.西瓜属雌雄同株异花,若四倍体♀×二倍体♂ 母本去雄
C.玉米属雌雄同株异花,若同时正反交 亲本双方均对雌花套袋,并人工授精
D.豌豆属雌雄同株同花,若高茎♀×矮茎身♂ 母本去雄并套袋
3.试用生物进化论的观点解释病菌抗药性不断增强的原因是
A. 使用抗生素的剂量不断加大,病菌向抗药能力增强方向变异
B. 抗生素对病菌进行人工选择,生存下来的病菌都是抗药能力强的
C. 抗生素的使用使病菌向抗药性强的方向进化
D. 病菌中原来就有抗病性强的个体,在使用抗生素的过程中淘汰了抗药性弱的个体
4.在调查某小麦种群时发现T(抗锈病)对t(易感染)为显性,在自然情况下该小麦种群可以自由交配,据统计TT为20%,Tt为60%,tt为20%,该小麦种群突然大面积感染锈病,致使易感染小麦在开花之前全部死亡。计算该小麦在感染锈病之前与感染锈病之后基因T的频率分别是多少?
A.50%和50% B.50%和62.5% C.62.5%和50% D.50%和100%
 5.右图是人体局部内环境示意图。以下各项中正确的是
5.右图是人体局部内环境示意图。以下各项中正确的是
A.某人长期营养不良,则会引起C液减少
B.新陈代谢主要发生在1中
C.3处细胞的内环境为淋巴
D.A液中的02进入组织细胞中被利用至少要通过3层生物膜
6.α-银环蛇毒能与突触后膜上的乙酰胆碱受体牢固结合;有机磷农药能抑制乙酰胆碱酯酶的活性,而乙酰胆碱酯酶的作用是清除与突触后膜上受体结合的乙酰胆碱。因此,α-银环蛇毒与有机磷农药中毒的症状分别是
A.肌肉松弛、肌肉僵直 B.肌肉僵直、肌肉松弛
C.肌肉松弛、肌肉松弛 D.肌肉僵直、肌肉僵直
7. 下列事实中不能利用勒沙特列原理来解释的
A. 往硫化氢水溶液中加碱有利于S2-的增多
B. 打开汽水瓶有大量气体冒出
C.
D. 高压有利于合成氨的反应
8.下列描述中,符合化学科学的是
A.“曾青得铁则化为铜”中的“曾青”是指硝酸铜
B.“冰,水为之,而寒于水”,说明相同质量的水和冰,水的能量高
C.“玉不琢不成器”、“百炼方能成钢”的说法都与物质的化学变化有关
D.“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是纤维素和油脂
9. 若阿伏加德罗为NA,下列说法不正确的是:
A.标准状况下,以任意比混和的氢气和一氧化碳气体共
B.
C.常温
D.1mol FeCl3完全转化为Fe(OH)3胶体后形成NA个胶粒
10.下列反应的离子方程式错误的是:
A. 氯化铝溶液中加入过量的氨水:Al3+ + 4NH3•H2O == AlO2- + 4NH4+ + 2H2O
B. 用氨水吸收过量的二氧化硫 NH3•H2O + SO2 == NH4+ + HSO3-
C. 碳酸钠溶液中加入过量的苯酚 C6H5-OH + CO32- == C6H5O- + HCO3-
D. 次氯酸钙溶液中通入过量的二氧化碳 ClO- + CO2 + H2O == HCO3- + HClO
11. 在一个
 4X (气) + 3Y(气)
4X (气) + 3Y(气)  2Q(气) +
nR(气)达平衡后,容器内温度不变,混和气体的压强比原来增加5%,X的浓度减小1/3,则该反应方程式中的n值是( )
2Q(气) +
nR(气)达平衡后,容器内温度不变,混和气体的压强比原来增加5%,X的浓度减小1/3,则该反应方程式中的n值是( )
A. 3 B.
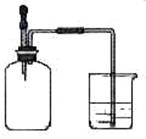
12.如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的
水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶气体是
① CO、O2 ② Cl2、CH4 ③ NO2、O2 ④ N2、H2
A.①② B.②③ C.③④ D.②④
13. 今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、
Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀
A. K+一定存在 B. 100mL溶液中含0.01mol CO32-
C. Cl-一定存在 D. Ba2+一定不存在,Mg2+可能存在
 二、选择题:本题共8小题,每小题6分,在每小题给出的四个选项中,有的只有一处选项正确,有的有多个选项正确,全部选对的得6分,选对但不全的得3分,有选错的得0分。
二、选择题:本题共8小题,每小题6分,在每小题给出的四个选项中,有的只有一处选项正确,有的有多个选项正确,全部选对的得6分,选对但不全的得3分,有选错的得0分。
14.一有固定斜面的小车在水平面上做直线运动,小球通过细绳与车顶相连。小球某时刻正处于图示1状态。设光滑斜面对小球的支持力为N,细绳对小球的拉力为T,关于此时刻小球的受力情况,下列说法正确的是 ( )
A.若小车向左匀速运动,N可能为零
B.若小车向左匀加速运动,T可能为零
C.若小车向右匀速运动,N可能为零
 D.若小车向右匀加速运动,T可能为零
D.若小车向右匀加速运动,T可能为零
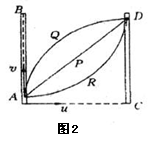
15.如图2所示,红蜡块能在玻璃管的水中匀速上升,若红
蜡块在A点匀速上升的同时,使玻璃管水平向右做匀加速直线
运动,则红蜡块实际运动的轨迹是图2中的( )
A.曲线Q B.直线P
C.曲线R D.无法确定
 A. 前
A. 前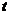 秒物体作加速运动,后
秒物体作加速运动,后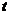 秒物体作减速运动。
秒物体作减速运动。
B. 前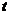 秒A的位移与后
秒A的位移与后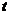 秒A的位移之比为1:2
秒A的位移之比为1:2
C. A由传送带左端到右端的平均速度为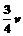
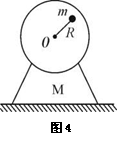 17.在质量为M的电动机飞轮上,固定着一个质量为m的重物,重物到轴心O的距离为R,如图4所示,为了使电动机不从地面上跳起,电动机
17.在质量为M的电动机飞轮上,固定着一个质量为m的重物,重物到轴心O的距离为R,如图4所示,为了使电动机不从地面上跳起,电动机
飞轮转动的最大角速度不能超过( )
A.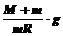 B.
B.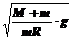
C. D.
D.
18.仅从已知下面的哪组数据,可以计算出地球的质量M地(已知万有引力常量为G)
A.地球“同步卫星”离地面的高度h
B.地球绕太阳运动的周期T1及地球到太阳中心的距离R1
C.地球表面的重力加速g和地球绕太阳运动的周期T
D.月球绕地球运动的周期T2及月球中心到地球中心的距离R2
19.质量为M的汽车在平直公路上以恒定的功率P由静止开始运动,已如汽车受到的
阻力是车重的k倍.根据以上条件在我们现在所学的知识范围内可以求出:(重力加速度为g)
A.汽车加速运动的时间 B.汽车加速运动中通过的路程
C.汽车运动的最大速度 D.汽车速度为最大速度一半时的加速度
 20.在距地面
20.在距地面
A.抛出时人对物体做功为50J B.自抛出到落地,重力对物体做功为100J
C.飞行过程中物体克服阻力做功22J D.物体自抛出到落地时间为1s
21.如图5所示,质量为m的小球,用OB和O′B两根轻绳
吊着,两轻绳与水平天花板的夹角分别为30°和60°,这时
OB绳的拉力为F1,若烧断O′B绳,当小球运动到最低点C时,
OB绳的拉力为F2,则F1∶F2等于?( )
A.1∶1 B.1∶2?
C.1∶3 D.1∶4?
22.填空题(本题2小题,,每小题8分、共16分)
 (1)风力发电是绿色能源 ,某地强风的风速为V,设空气密度为ρ,如果把通过横截面为S的风的动能的50%转化为电能,则电功率为_______。
(1)风力发电是绿色能源 ,某地强风的风速为V,设空气密度为ρ,如果把通过横截面为S的风的动能的50%转化为电能,则电功率为_______。
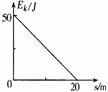
(2)如右图,质量为
擦阻力的作用,其动能随位移变化的图线如图所示,g取
与水平面的动摩擦因数μ= .物体滑行的总时间为_____ s
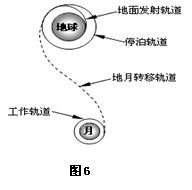 23.(15分)“嫦娥一号”探月卫星在空中运动过程简化如图6所示.卫星由地面发射后,经过发射轨道进入停泊轨道,在停泊轨道经过调速后进入
23.(15分)“嫦娥一号”探月卫星在空中运动过程简化如图6所示.卫星由地面发射后,经过发射轨道进入停泊轨道,在停泊轨道经过调速后进入
地月转移轨道,再次调速后进入工作轨道.已知卫星在停
泊轨道和工作轨道运行的轨道半径分别为R1和R2,地球半
径为r1,月球半径为r2,地球表面重力加速度为g,月球
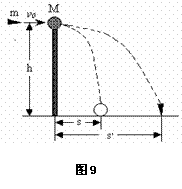
 24.(16分)如图7为一固定在地面上的楔形木块,质量分
24.(16分)如图7为一固定在地面上的楔形木块,质量分
别为m和M两个物体, 用轻质细绳相连跨过固定在斜面顶端的
定滑轮, 已知斜面的倾角为α, 且M>m sinα。用手托住物体
M, 使之距地面高为h时,物体m恰停在斜面的底端,细绳恰
好绷直,并且与斜面的斜边平行,如果突然释放物M,不计一
切摩擦,物体m能沿斜面滑行的最大距离是多少? 设斜面足够长。
 25.(10分)将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,
25.(10分)将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,
请回答下列问题:
(1)判断该反应达到平衡状态的标志是 。(填字母)(2分)
a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是 。(填字母)(2分)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
(3)求该反应达到平衡时SO2的转化率(用百分数表示)。(写出计算过程)(4分)
(4)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀多少克?(不要求过程)(2分)
26.(10分)某试剂厂用银(含杂质铜)和硝酸(含杂质Fe3+)反应制取硝酸银.步骤如下:
 |

依据上述步骤,完成下列填空:
(1) 溶解银的硝酸应该用 硝酸(填浓或稀) (2分),原因是 (2分)。
a. 减少过程中产生NOx 的量 b. 减少原料银的消耗量 c. 节省硝酸物质的量
(2) 步骤B加热保温的作用是 . (2分)
a. 有利于加快反应速度
b. 有利于未反应的硝酸挥发
c. 有利于硝酸充分反应,降低溶液中c(H+)
(3) 步骤C是为了除去Fe3+、Cu2+ 等杂质.冲稀静置时发生的化学反应是 (选类型)(2分),产生的沉淀物化学式 。(2分)
a. 置换反应 b. 水解反应 c. 氧化―还原反应
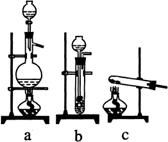
27.(23分)实验室模拟合成氨和氨催化氧化的流程如下:
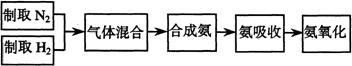
已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和
氯化铵溶液经加热后反应制取氮气。
(1)从右图中选择制取气体的合适装置:
氮气 (2分)、氢气 (2分)
(2)氮气和氢气通过甲装置,甲装置的作用除了将气
体混合外,还有 (2分)、 (2分)
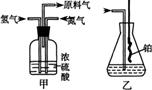 (3)氨合成器出来经冷却的气体连续通人乙装置的水中吸收氨,
(2分)(“会”或“不会”)发生倒吸,原因是:
(2分)。
(3)氨合成器出来经冷却的气体连续通人乙装置的水中吸收氨,
(2分)(“会”或“不会”)发生倒吸,原因是:
(2分)。
(4)用乙装置吸收一段时间氨后,再通入空气,同时将
经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热
的原因是: (2分),
锥形瓶中还可观察到的现象是: 。(2分)
(5)写出乙装置中氨氧化的化学方程式: (3分)
(6)反应结束后锥形瓶内的溶液中含有H+、OH-、 、 离子。(各2分)
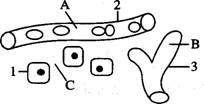
28.(16分)下列是某高等动物雌激素分泌及作用机制模式图。请结合所学知识及图中有关信息回答。
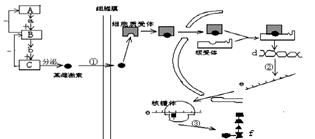
(1)结构A是 ,结构C是 ;结构ABC中具有神经传导和激素分泌双重功能的是 (填名称);物质b是 ,物质e是 ;
(2)过程①通过的方式是 ,细胞质受体、核受体与细胞膜上受体的物质属性及功能相似,因此,细胞质和细胞核受体的物质成分应是 ,导致细胞质受体与核受体差异的直接原因是 .
 29.(22分)图甲和乙分别是果蝇细胞的局部结构示意图,1、2、3、4、5、6、7、8 分别表示染色体,A、a、B、b、C、c、D、d
29.(22分)图甲和乙分别是果蝇细胞的局部结构示意图,1、2、3、4、5、6、7、8 分别表示染色体,A、a、B、b、C、c、D、d
分别表示所在染色体上控制一定性状
的基因。请据图回答:
(1)假如图甲为果蝇的一个卵原细
胞,则:
该卵原细胞中含有 对同源染
色体,写出其中的一个染色体组 ;
若将该卵原细胞的一个DNA分子用15N标记,并只供给卵原细胞含14N的原料,正常情况下该卵原细胞分裂形成的卵细胞中含14N的比例为 。
(2)假如图乙为果蝇的一个体细胞,设常染色体上的基因A(长翅)对a(残翅)显性,性染色体X上的基因D(红眼)对d(白眼)显性。用图示代表的果蝇与另一果蝇杂交得到的子代中,若残翅与长翅各占一半,雌蝇均为红眼,那么与图示果蝇进行杂交的果蝇的基因型是 ,表现型为 。
(3)果蝇的卵原细胞在减数分裂形成卵细胞过程中常常发生染色体不分开的现象,因此常出现性染色体异常的果蝇,并产生不同的表型,如下表所示:
受精卵中异常的性染色体组成方式
表现型
XXX
在胚胎期致死,不能发育为成虫
YO(体细胞中只有一条Y染色体,没有X染色体)
在胚胎期致死,不能发育为成虫
XXY
表现为雌性可育
XYY
表现为雄性可育
XO(体细胞中只有一条X染色体,没有Y染色体)
表现为雄性不育
为探究果蝇控制眼色的基因是否位于性染色体上,著名的遗传学家摩尔根做了下列杂交实验。
让白眼雄果蝇和红眼雌果蝇交配,后代全部是红眼果蝇;让白眼雌果蝇和红眼雄果蝇交配,子代雄性果蝇全是白眼的,雌性果蝇全是红眼的。他的学生蒂更斯用白眼雌果蝇与红眼雄果蝇交配,子代大多数雄果蝇都是白眼,雌果蝇都是红眼,但有少数例外,大约每2000个子代个体中,有一个白眼雌蝇或红眼雄蝇,该红眼雄蝇不育。
①请根据上表信息用遗传图解,解释蒂更斯实验中为什么会出现例外(设有关基因为D、d)。
②提出一个验证蒂更斯实验的简单思路,并预测结果,得出结论(提示:专业技术人员在光学显微镜下,可以根据有丝分裂中期染色体形态分辨性染色体和常染色体)。
简单思路:
预期结果:
结论:
31.物理选考题
A.[物理─选修3-4](15分)
(1)(6分)下列关于振动和波的说法正确的是 。 (填入选项前的字母,有填错的不得分)
A.弹簧振子的加速度和速度每过平衡位置方向就会改变
 B.横波在介质中的传播速度由介质本身的性质决定
B.横波在介质中的传播速度由介质本身的性质决定
C.无论是横波还是纵波只要从空气进入介质速度一定变小
D.当观察者静止,声源向着观察者运动时观察者感到声音的音调变高了
(2)(9分)如图8所示,己知平行玻璃砖的折射率
玻璃砖的上表面,经玻璃砖折射从下表面射出,出射光
线与入射光线平行,求两平行光线间距离.(结果可用
根式表示)
B.[物理─选修3-5](15分)
(1)(6分)下列说法正确的是 (填序号)。
在下列四个方程中,x1、x2、x3和x4各代表某种粒子
① ®
®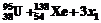 ②
②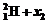 ®
®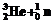
③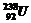 ®
® ④
④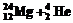 ®
®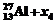
 以下判断中正确的是( )
以下判断中正确的是( )
A.x1是中子 B.x2是质子
C.x3是a粒子 D.x4是氘核
(2)(9分)如图9,一个质量为M=
32.化学选考题:
A.(化学与生活)分析下面两个案例并回答有关问题。
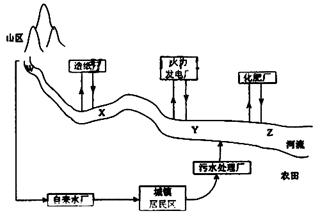 (1)某城镇生产、生活的分布情况如图所示,河流中W、X、Y、Z处某次水样抽测结果如表所示。
(1)某城镇生产、生活的分布情况如图所示,河流中W、X、Y、Z处某次水样抽测结果如表所示。
地点
项目
W
X
Y
Z
水温/℃
15
18
26
25
pH
6
8
5
5
溶解氧量/(mg?L-1)
11
9
7
3
①导致X、Y处水样pH变化的原因可能是 ;
②Z处鱼类大量减少,产生这种现象的原因可能是 。
(2)某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2O2,还含有SiO2等杂质)、煤 矿、石灰石和黏土。拟在该地区建设大型炼铁厂。
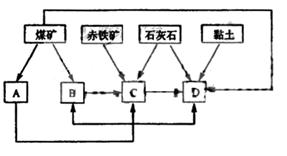
①随着铁矿的开发和炼铁厂的建立,需要在该地区相应建立焦化厂、发电厂、水泥厂等,形成规模的工业体系。据此确定上图中相应工厂的名称A 、B 、C 、D ;
②以赤铁矿为原料,写出高炉炼铁中得到生铁和产生炉渣的化学方程式 ;
③从“三废”利用、环境保护等角度考虑,该地区和企业在生产中应采取的一些措施有(举出2种措施即可) 。
B.(物质结构)
元素A~D是元素周期表中短周期的四种元素,请根据表中的信息回答下列问题。
元素
A
B
C
D
物质或结构信息
单质制成的的高压灯,发出的黄光透雾力强、射程远。
工业上通过分离液态空气获得其单质。原子的最外层未达到稳定结构
单质常温、常压下是气体,原子的L层有一个未成对的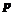 电子
电子
+2价阳离子的核外电子排布与氖原子相同。
(1)上表中与A属于同一周期的元素是_____________(写元素符号)(2分),写出D离子的电子排布式______________________。(2分)
(2)D和C形成的化合物属于_________晶体(2分)。写出C单质与水反应的化学方程式_________________________(3分)。
(3)对元素B的单质或化合物描述正确的是_________。(2分)
a.B元素的最高正价为+6 b.常温、常压下单质难溶于水
c.单质分子中含有18个电子 d.在一定条件下镁条能与单质B反应
(4)A和D两元素金属性较强的是(写元素符号)_____。(2分)写出能证明该结论的一个实验事实________________。(2分)
C.(有机化学)
A、B、C、D、E均为有机化合物,它们之间的关系如图所示(提示:RCH=CHR'在酸性高锰酸钾溶液中反应生成RCOOH和R'COOH,其中R和R'为烷基)。
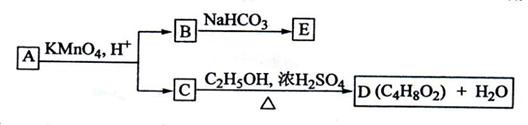
回答下列问题:
(1)直链化合物A的相对分子质量小于90,A分子中碳、氢元素的总质量分数为0.814,其余为氧元素,则A的分子式为_____________;(2分)B的结构简式是__________________(2分)
(2)已知B与NaHCO3溶液完全反应,其物质的量之比为1:2,则在浓硫酸的催化下,B与足量的C2H5OH发生反应的化学方程式是___________,(3分)反应类型为_____:(2分)
(3)A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则A的结构简式是__________________(2分)
(4)D的同分异构体中,能与NaHCO3溶液反应放出CO2的有__________种,(2分)其相应的结构简式是__________________。(2分)

半的部位及面积相等(任意两项,有其他合理的分析也可以)
(5)O2的释放量 CO2的吸收量
化学参考答案

(2)①发电厂;焦化厂;炼铁厂;水泥厂。
②Fe2O3+3CO 2Fe+3CO2;CaCO3+SiO2
2Fe+3CO2;CaCO3+SiO2 CaSiO3+CO2↑
CaSiO3+CO2↑

物理参考答案


 的物体Q轻轻放在水平传送带的左端A处,经
的物体Q轻轻放在水平传送带的左端A处,经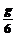
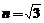 ,厚度为
,厚度为 .入射光线
.入射光线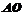 以入射角
以入射角