2008-2009学年度聊城市阳谷第一学期九年级期末学业水平检测
化学试卷
说明:1.考试时间为40分钟,满分40分;
2.本试卷分试题和答题卷两部分,请同学把所有答案写在答题卷上
3.考试结束时,只收答题卷,请同学填好姓名。
相对原子质量:H:1 O:16 Cl:35.5 Ca:40
一、选择题(本题包括12个小题,每小题只有一个选项符合题意。1~4题每小题1分,5~12小题每小题2分,共20分。)
1.用分子的观点解释下列现象,不合理的是( )
A.食物变质――分子本身发生了变化
B.汽油挥发――分子大小发生了变化
C.热胀冷缩――分子间隔发生了变化
D.花香四溢――分子作扩散运动
2.化学上把“生成新物质的变化叫做化学变化”。下面对化学变化中“新物质”的解释,正确的是( )
A.“新物质”就是指自然界中不存在的物质
B.“新物质”就是与变化前的物质在颜色、状态等方面有所不同的物质
C.“新物质”就是与变化前的物质在元素组成上不同的物质
D.“新物质”就是在组成或结构上与变化前的物质不同的物质
3.某校同学以“××河水污染情况调查”为课题进行研究性学习,为了较准确地测定河水样品的酸碱度,可以使用( )
A.紫色石蕊试液 B.无色酚酞试液
C.pH试纸 D.蓝色石蕊试纸
4.如下图所示的实验操作与方法正确的是( )


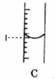

5.雄伟壮观的国家大剧院主体建筑表面安装了近两万块钛(Ti)金属板。下列关于钛及其化合物的说法正确的是( )
A.Ti可以表示钛元素,也可以表示一个钛原子,还可以表示钛单质
B.TiO2中含有氧分子
C.CaTiO3属于氧化物
D.Ti原子核内有22个质子,则Ti3+核外有25个电子
6.下列关于水的天然循环的说法中,正确的是( )
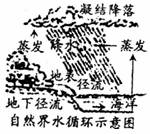
①水在天然循环过程中实现了水的自身净化;②水的天然循环是通过水的三态变化实现的;③太阳为水的天然循环提供了能量;④水的天然循环完成了水资源的重新分配
A.①③ B.①② C.③④ D.①②③④
7.用氯化钠配制
①配制溶液;②称取氯化钠固体;③过滤;④量取蒸馏水;⑤计算。正确的操作顺序是( )
A.①②③④ B.⑤②④① C.⑤①②④ D.③②④①
8.下列分别为二氧化碳的制取、干燥、收集和性质检验的装置图,其中错误的是( )
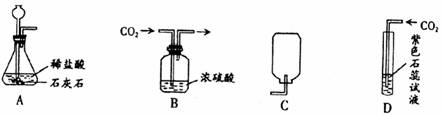
9.下列化学方程式的书写不正确的是( )
A.CaCO3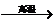 CaO+CO2↑ B.2KMnO4
CaO+CO2↑ B.2KMnO4 K2MnO4+Mn O2+ O2↑
K2MnO4+Mn O2+ O2↑
C.2Fe+6HCl===2FeCl3+3H2 ↑ D.CO2+Ca(OH)2===CaCO3↓+H2O
10.海洋是人类巨大的资源宝库,海洋资源的开发前景十分广阔。下列有关海洋资源的叙述错误的是( )
A.利用海水可以提取镁盐制取镁
B.海水中溶解盐的质量分数高达5%
C.海底蕴藏着大量的煤、石油和天然气
D.海洋中蕴含着丰富的海洋动力资源
11.t℃时,有两份硝酸钾溶液,一份是饱和溶液(溶质的质量分数为40%),另一份是溶质的质量分数为10%的溶液。下列实验操作中,无法区分这两种溶液的是( )
A.加一定量的水 B.加入少量硝酸钾晶体
C.降低温度 D.t℃时蒸发少量的水
12.下图形象地表示某反应前后反应物与生成物分子及其数目的变化,其中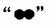
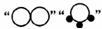 分别表示A、B、C三种不同的分子。该反应的化学方程式中A、B、C前的化学计量数之比为( )
分别表示A、B、C三种不同的分子。该反应的化学方程式中A、B、C前的化学计量数之比为( )
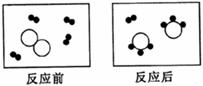
A.4:1:3 B.3:1:
二、填空与简答题(本题包括3小题。共l6分)
13.(4分)用化学用语填空:
(1)人体胃液中帮助消化的酸是__________;
(2)2个碳酸根离子_________;
(3)消石灰的主要成分_________;
(4)氧化镁中镁元素的化合价为+2_________。
14.(4分)写出下列错误操作可能造成的后果:
(1)试管口竖直向上,加入石灰石_________。
(2)使用量筒量取50ml稀硫酸时,俯视读数,量取的结果:_________。
(3)使用氢氧化钠溶液后,忘记盖胶塞:_________。
(4)用pH试纸测定稀盐酸的pH时,先将试纸用水湿润,测得的结果:_________。
15.(8分)下图是化学实验中的常见操作示意图:
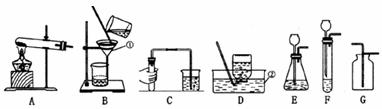
(1)写出图中标有数字的仪器名称:①_________,②_________。
(2)实验室用过氧化氢溶液制取氧气,采用的发生装置可选取上图中的_________(填序号)装置;写出组装该装置时一条注意事项:_________,原因是_________。收集装置可选用_________。
(3)图B实验操作的名称是_________,其中玻璃棒的作用是_________。
(4)图C实验操作的名称是_________。
三、计算题(本题4分)
16.某同学在参加学校开展的综合实践活动中,考察了一家化工厂的污水处理情况。该同学在考察过程中收集到了以下资料:
(1)该化工厂排放的污水中主要成分是盐酸,提取未经处理的污水水样,用pH试纸测得pH=3;
(2)处理污水步骤之一是:污水进入中和池进行中和处理,所用的原料是较经济的石 灰水;
(3)提取经过处理后可排放的水样,测得pH在7.0左右。根据上述资料回答问题:
已知污水中盐酸的质量分数为0.004%。假设中和池中有1.0×