2009年江苏省淮安市初中毕业暨中等学校招生文化统一考试
化学试卷
相对原子质量:H-1 O-16 S-32 Fe-56
一、选择题(本题包括15小题。1-10题每小题1分,11-15题每小题2分,共20分,每小题只有1个选项符合题意。)
1.下列变化属于化学变化的是
A.火药爆炸 B.矿石粉碎 C.蜡烛熔化 D.汽油挥发
2.下列食物中富含维生素的是
A.鸡蛋 B.米饭 C.黄瓜 D.鱼虾
3.一氧化氮(NO)是人体中枢神经系统的信号因子,其中氮元素的化合价是
A.+1 B.+
4.工业上常用如下反应制取金属镁:MgCl2(熔融) Mg+Cl2↑,该反应属于
Mg+Cl2↑,该反应属于
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
5.下列物质属于纯净物的是
A.海水 B.糖水 C.冰水 D.汽水
6.人体缺少微量元素会影响健康,甚至引起疾病。下列属于人体所需微量元素的是
A.锌 B.碳 C.氢 D.氧
7.节能减排有利于国民经济的可持续发展。下列图标为我国节能标志的是

8.生产生活中经常会遇到去除油污的问题。下列去除油污的方法错误的是
A.用食盐水清除灶具上的油污 B.用汽油清除机器上的油污
C.用洗涤剂洗涤餐具上的油污 D.用肥皂洗涤衣服上的油污
9.今年世界环境日中国主题为“减少污染――行动起来”。下列做法不利于减少污染的是
A.回收利用废旧电池 B.推广使用无磷洗衣粉
C.综合利用化石燃料 D.大量使用超薄塑料袋
10.钢铁的生产和使用是人类文明和社会进步的重要标志。下列说法正确的是
A.铁矿石在地壳中含量丰富,可以随意开采
B.为防止铁制品生锈,可在其表面涂上一层油漆
C.废弃铁制品再利用的成本太高,属于不可回收垃圾
D.钢的含碳量比生铁的高,所以钢的性能比生铁优越
11.下列有关物质燃烧现象的描述正确的是
A.铁丝在氧气中燃烧,火星四射 B.木炭在氧气中燃烧,产生大量白烟
C.红磷在空气中燃烧,发生耀眼白光 D.硫粉在空气中燃烧,发出蓝紫色火焰
12.下图所示的实验操作错误的是
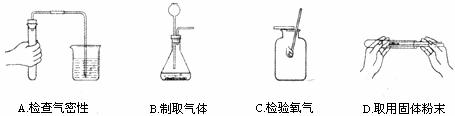
13.在进行硝酸钾与氯化钠溶解性比较的实验时,下列条件必须控制的是
①温度 ②溶质颗粒大小 ③溶质质量 ④溶剂质量 ⑤溶剂种类
A.①② B.②③④ C.①④⑤ D.①⑤
14.下列有关物质检验或鉴别方法正确的是
A.向某固体中加入稀盐酸,若产生无色气体,则该固体中一定含有碳酸盐
B.向某溶液中滴加紫色石蕊试液,若石蕊试液显蓝色,则该溶液一定是碱溶液
C.抽丝灼烧,通过闻是否有烧焦羽毛气味来区分蚕丝制品和羊毛制品
D.用水作试剂,通过观察溶液温度的变化来区分氯化钠和硝酸铵固体
15.除去下列物质中少量的杂质,所用方法错误的是
选项
物质
杂质
除杂方法
A
CaCl2
CaCO3
加入足量的水充分溶解后,过滤、蒸发
B
Cu
CuO
加入足量的稀盐酸充分反应后,过滤、洗涤、干燥
C
NaCl溶液
MgCl2
加入足量的氢氧化钠溶液充分反应后,过滤
D
Zn(NO3)2溶液
AgNO3
加入足量的锌粉充分反应后,过滤
二、填空与简答题(本题包括8小题,共32分)
16.用化学符号表示:
⑴磷元素_________;⑵3个一氧化碳分子________;⑶2个钠离子_________。
17.请从①氧气 ②稀有气体 ③硫酸 ④磷酸二氢铵 ⑤氯化钠中选择适当物质,并用其序号填空:
⑴可用作保护气的是___________;
⑵常用作调味剂的是___________;
⑶可用于金属表面除锈的是___________;
⑷急救病人时可供呼吸的是___________;
⑸能作为无土栽培营养液成分的是___________。
18.下图是甲、乙两种物质(均不含结晶水)的溶解度曲线。
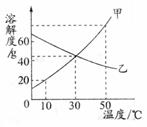
⑴当温度为_______℃时,甲和乙的溶解度相等;
⑵
⑶分别将
乙(填:“>”、“=”或“<”)。
19.对所学知识进行整理与归纳,是有效学习的重要手段。以下是对构成物质微粒知识的整理与归纳,请将有关内容填写完整:
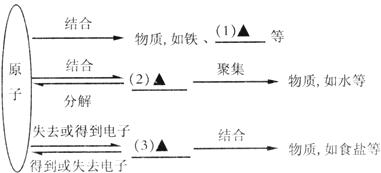
20.运用所学知识解释下列问题:
⑴真金不怕火炼,这是因为金的化学性质___________________________;
⑵农业上常用熟石灰和硫酸铜溶液配制农药波尔多液,该农药不能在铁制容器中配制的原因是________________________________________(用化学方程式表示);
⑶铝的化学性质比较活泼,在空气中比铁更容易氧化,但铝制品比铁制品经久耐用,其主要原因是_________________________________________________________。
21.化学晚会上,小华同学表演了下列两个趣味实验:
⑴将一块棉布手绢浸入由95%酒精和水配制的混合溶液中,浸透后取出,轻轻拧干,用坩埚钳夹持,在酒精灯上点燃,并轻轻抖动手绢。火焰熄灭后,手绢完好无损。手绢没有燃烧的原因是____________。
⑵向下图所示的瓶中加水到虚线,再向瓶中加无水酒精至满,塞紧玻璃塞,颠倒数次, 发现瓶中液体体积减少。以检查,实验时瓶中液体无渗漏。请用微粒的观点解释瓶中液体体积减少的主要原因:_______________。

22.小军在参加野外夏令营活动时带了食品、瓶装矿泉水、纱布、肥皂、火柴和铁锅等物品。
⑴所带物品中由金属材料制成的是__________,该物质的中使用主要是利用了金属具有良好的_____________性。
⑵为净化一定量的河水,小军进行了如下操作:取河水→静置→过滤。其中静置的作用是_________________,所带物品中能组装成简易过滤器的是_______________。
⑶小军在用河水和肥皂洗衣服时,发现产生的泡沫很少,并有白色垢状物,此现象说明该河水是_________(填:“硬水”或“软水”)。
23.根据下图所示的循环过程,回答下列问题。

⑴写出反应②的化学方程式:________________________________。
⑵已知反应①的化学方程式为:6CO2+6H2O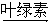 A+6O2,则A中所含元素种类有
A+6O2,则A中所含元素种类有
_________种。A所属的物质类别是_________(填:“无机物”或“有机物”)。
⑶反应③和反应④的循环有效地实现了能量的转化,该能量的转化形式为________。
⑷《京都协议》中明确规定:到2010年,发达国家排放的温室气体量要比1990年的水平削减5.2%。上述循环中,人类为控制大气中二氧化碳含量的增加,采取了多项措施,请具体说明其中的两项:__________________;___________________。
三.实验与探究题(本题包括3小题,共20分)
24.下图所示为实验室用高锰酸钾制取氧气的装置。

⑴写出试管中所发生反应的化学方程式:________________________________,图中收集氧气的方法是________________。
⑵停止实验时,应先________________,然后再熄灭酒精灯。熄灭酒精灯的方法是:____
____________________。
25.在做盐酸与氢氧化钠溶液中和反应的实验时,化学兴趣小组的同学围绕盐酸和氢氧化钠是否恰好完全反应等问题进行了探究。
【实验一】用pH试纸测定反应过程中溶液的pH:用__________(填一种仪器名称)醮取溶液沾在pH试纸上,再把pH试纸显示的颜色与___________对照。当测得溶液的pH_______7时(填:“>”、“=”或“<”),说明盐酸与氢氧化钠恰好完全反应。
【实验二】用无色酚酞试液作指示剂进行如下实验:
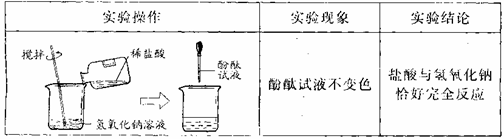
⑴指出(或改正)上述操作中存在的错误:_____________________________。
⑵你认为上述实验结论是否可靠,请说明理由:____________________________。
【实验三】用温度计测反应中溶液温度变化:向一定体积10%的氢氧化钠溶液中加入10%的盐酸(室温下),反应中溶液温度的变化如下:
加入盐酸的体积(V)mL
2
4
6
8
10
12
14
16
18
20
溶液温度上升
(△t)℃
5.2
9.6
12.0
16.0
18.2
16.7
15.7
14.7
13.7
12.9
⑴如图所示,温度计的位置正确的是_______(用字母表示)。

⑵盐酸与氢氧化钠恰好完全反应时,所用盐酸体积最接近于__________mL。
26.空气中的二氧化碳超过正常含量时,会对人体健康产生如下影响:
空气中二氧化碳的体积分数
对人体健康的影响
1%
感到气闷、头晕、心悸
4%~5%
感到气闷、头痛、眩晕
6%以上
使人神志不清,呼吸停止,以致死亡
【提出问题】如何检验空气中二氧化碳的含量以便判断是否会影响人体健康?
【实验探究】
方法一:分别向二氧化碳含量不同的空气中放入燃着的蜡烛。
方法二:分别向二氧化碳含量不同的空气中加入适量的澄清石灰水。
【实验现象】
空气中二氧化碳体积分数
0.03%
1%
5%
10%
20%
方法一
正常燃烧
正常燃烧
正常燃烧
燃烧不旺
熄灭
方法二
不变混浊
变混浊
变混浊
变混浊
变混浊
【分析与应用】
⑴上述实验中,方法一所依据的二氧化碳的性质是_____________________;方法二所依
据的反应原理是_________________________________(用化学方程式表示)。
⑵菜窖中一般会含有较多的二氧化碳,人不能贸然进入。
①菜窖中二氧化碳气体的主要来源是_____________________________。
②为确保人体健康不受影响,在进入菜窖前,应对其中的二氧化碳的含量进行检验,有关操作步骤是__________________________________________________________。
【拓展探究】利用下图装置,粗略测定菜窖中二氧化碳的体积分数。

⑴连接实验装置:装置接口的连接顺序为a→____→____→____→____→f。
⑵用于实验的菜窖气体为50mL,最终量筒中共收集到水为45mL,该菜窖气体中二氧化碳的体积分数约为____________。
四.计算题(本题包括2小题,共8分)
27.赤铁矿石是炼铁的重要原料,其产要成分为氧化铁(Fe2O3)。请计算:
⑴氧化铁中铁、氧元素的质量比为______________。
⑵
28.现有一瓶未开启的浓硫酸,标签如图所示。试求:

⑴欲配制
⑵取上述配制好的稀硫酸