2009年辽宁中考综合复习训练化学试题(八)
理化考试时间l50分钟 化学试卷满分65分
可用到的相对原子质量:H―1 O―16 S―32 Fe―56
一、选择题(本题包括l3道小题,l―11小题每小题1分;l2、13小题每小题2分;共15分。每小题有一个最符合题目要求的选项,请选出后将其序号填在题后的括号内)
1.
A.大量植树造林 B.大量使用塑料袋
C.回收废旧电池 D.节约用水
2.节日里的下列景象伴随着化学变化的是 ( )
A.五光十色的烟火礼花 B.不断闪烁的霓虹灯
C.变幻无穷的音乐喷泉 D.满屋飘香的茅台酒
3.下列物质中,属于纯净物的是 ( )

4.古人曾有赞美菊花的诗句“冲天香阵透长安”。浓郁的花香遍布长安的原因是( )
A.分子的质量很小 B.分子间有间隔
C.分子在不断运动 D.分子由原子构成
5.
A.过氧乙酸中含有三种元素 B.过氧乙酸分子由9个原子构成
C.过氧乙酸是化合物 D.过氧乙酸是氧化物
6.2008年1月份的雪灾对我国南方的电力、交通造成很大的危害。有一种融雪剂含有Na2SiO3(硅酸钠),Na2SiO3中Si元素的化合价是 ( )
A.+1价 B.+2价 C.+3价 D.+4价
7.在金属Cu、Al、Ag、Zn中,既能与硝酸银溶液反应,又能与稀硫酸反应的是( )
A.Al、Ag、Zn B.Al、Zn C.Cu、Al、Zn D.Ag、Zn
8.下列物质的性质中,属于化学性质的是 ( )
A.铝具有导电性
B.碳酸氢钠能与稀盐酸反应
C.氯化钠是白色固体
D.常温下甲烷是无色无味气体
9.下列是一些物质的pH,酸碱性最接近中性的是 ( )
A.苹果汁(2.9~3.3) B.蕃茄汁(4.0~4.4)
C.玉米粥(6.8~8.0) D.肥皂水(9.8~10.2)
10.除去CO中混有少量CO2的方法是 ( )
A.通入浓硫酸 B.通入氢氧化钠溶液
C.点燃混合气体 D.通过灼热的氧化铁
11.某化工厂以石灰石、纯碱和水为主要原料制取烧碱。在制取过程中的变化关系为:CaCO3 →CaO→Ca(OH)2→NaOH,上述变化过程中没有涉及的化学反应基本类型是 ( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
12.从
A.用布袋代替塑料袋 B.重复使用某些塑料制品
C.回收利用各种废弃塑料 D.将废弃塑料集中到野外焚烧
13.将
A.
二、填空题(本题包括4道小题,每空1分,共14分)
14.氮气、氧气、氦气和二氧化碳都是空气的成分。用化学式填写:(1)占空气体积78%的是__________;(2)可用于制造霓虹灯的是__________;(3)固态时可用于人工降雨的是_________。
15.某实验小组同学准备用粗盐配制一定质量分数的氯化钠溶液,他们设计了如下实验流程:粗盐溶解→沉淀、过滤→蒸发结晶→配制溶液。请回答下列问题:
(1)过滤操作中除用到铁架台、烧杯、滤纸外,还要用到的仪器有______________;
(2)配制溶液过程中,需用____________称量氯化钠,用__________量取蒸馏水。
16.下列数据是硝酸钾固体在不同温度时的溶解度。
温度/℃
0
20
40
60
80
溶解度/g
13.3
31.6
63.9
110
169
(1)硝酸钾溶液中的溶剂是______________;
(2)
(3)20时,向
(4)如图所示,小烧杯中盛放的是上述(2)中所得的硝酸钾溶液。若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是__________ (填字母);
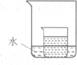
A.冰 B.浓硫酸 C.硝酸铵 D.干冰 E.氢氧化钠 F.氧化钙
17.钢铁是重要的金属材料。
(1)下列铁制品的用途中,利用金属导热性的是____________(填字母,下同);

(2)目前世界上已有50%以上的废钢铁得到回收利用,其目的是____________;
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(3)将生锈的铁制品放入盛有过量稀盐酸的洗槽中,观察到溶液变黄,有无色气泡逸出。
①写出发生溶液变黄的反应的化学方程式_____________________________________。
②氯化铁溶液可以作净水剂。欲将上述所得溶液中含铁的物质以氯化铁形式回收,加入过氧化氢溶液反应可生成氯化铁和水。已知每生成l62.
三、简答题(本题包括4道小题,共22分)
18.(2分)为什么水壶中水垢用醋可以除去呢?
19.(4分)1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德?埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖。
(1)将氢气和氮气在高温、高压和催化剂的条件下合成氨(NH3)。反应的化学方程式为____________________________________________________________________;
(2)用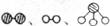 分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序:______________________(将下面五张图按反应过程顺序用序号排列)
分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序:______________________(将下面五张图按反应过程顺序用序号排列)
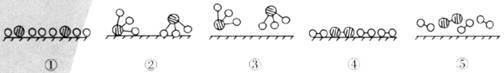
(3)表面化学对于化学工业很重要,它可以帮助我们了解不同的过程。
在潮湿的空气里,铁表面吸附了一层薄薄的水膜,同时由于空气中O2的溶解,水膜呈中性。若空气中CO2溶解,水膜呈酸性,写出该反应的化学方程式:_____________________,
在汽车排气管上安装尾气净化装置,可使尾气中的CO和NO在催化剂表面发生反应,产生两种空气组成的气体,写出该反应的化学方程式:____________________________。
20.(8分)在今年沈阳市化学实验操作考查中,我们认真完成了用双氧水和二氧化锰制取氧气的实验,请据此实验回答下列问题:
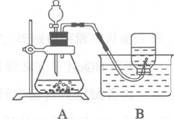
(1)要检查A装置的气密性是否良好,通常是把导管口插入水中,然后双手紧握锥形瓶外壁,观察导管口是否有气泡产生。请你回答这种做法的依据是什么。(用微粒的观点解释)
_________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
(2)A装置内发生反应的化学方程式为_____________________________________,二氧化锰在该反应中作_________剂,实验后回收二氧化锰的最佳方法是__________________;
(3)在实验过程中,某同学由于动作太慢,氧气还没有收集满,锥形瓶内的反应就已经停止(如上图所示)。若想集满这瓶氧气,在不拆卸装置的前提下,请你帮他想出两种方法。
①________________________________________________________________________,
②________________________________________________________________________。
21.(8分)下图所示为实验室常用实验装置:
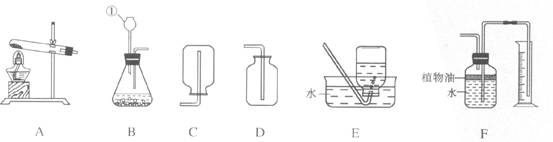
据此回答下列问题:
(1)写出带标号仪器的名称:_______________;
(2)常温下,用锌和稀硫酸反应制取氢气,应选用的发生装置是_____ ___(填序号,下同);
(3)实验室通常用稀盐酸和石灰石反应制取CO2,该反应的化学方程式为___________________________;此外,CO2也可以用碳酸氢钠(NaHCO3)固体加热分解(产物为碳酸钠、二氧化碳和水)来制取,该反应的化学方程式为______________,若用此法来制取CO2,应选用的发生装置是_____________;
(4)F装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是______________________________,植物油上方原有的空气对实验的结果____________(填“有”或“没有”)明显影响;为什么?___________________ _______________
四、探究题(本题包括1道小题,共分)
22.(分)请你参与下列探究:
【问题情景】某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出。这一现象激发起同学们的探究欲望,生成的是什么气体?
【提出猜想】从物质组成元素的角度,放出的气体可能是SO2、O2、H2。
【查阅资料】SO2易溶于水,它能与NaOH反应,生成Na2SO3。
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,则检验方法是______________________________;
(2)乙同学认为是SO2,则只需将放出的气体通入盛有NaOH溶液的洗气瓶中,称量通气前后洗气瓶得质量。写出SO2与NaOH反应的化学方程式: ______________________;
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。
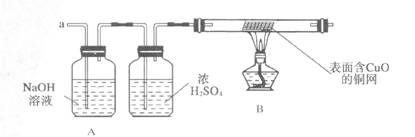
如果放出的是O2和H2,你认为方案中的安全隐患是____________________________。
丙同学认为:为确保安全,实验前应先收集一试管气体,用拇指_________________,若不发出________________,方可采用上面的装置进行实验。
【实验探究】经丙同学确认安全后,小组同学首先对装置A进行称量,再将收集到的气体从a通入,过一会儿点燃B处酒精灯;一段时间后,发现表面含CuO的铜网由黑色变为光亮的红色;停止通气,再次称量装置A,发现质量无增减。
结论:铁粉与硫酸铜溶液反应时,产生的气体是_____________________。
【思维拓展】
(1)由上述实验可以推出,硫酸铜溶液中可能含有______________物质。
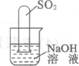
(2)不通过称量,如何判断SO2与NaOH溶液发生了反应呢?有一同学设计了如下图所示的装置进行实验,发现试管内液面上升,就得出SO2与NaOH溶液发生反应的结论。其他同学认为这一方案不严谨,理由是________________________________。要得到科学严谨的结论,仍利用该装置,补做的实验是__________________________。
五、计算题(本题包括1道小题,共6分)
23.(6分)生铁和钢都是铁合金,生铁中含碳量在2.0%~4.3%之间,钢的含碳量在0.03%~2.0%之间。将一块质量为
请根据计算回答: (计算结果精确到0.001)
(1)该铁合金是生铁还是钢?
(2)反应后所得溶液中的硫酸亚铁的质量。