网址:http://m.1010jiajiao.com/timu_id_914130[举报]
2008年9月份曝光的引起国人共愤的“结石宝宝”事件,与婴幼儿服用含有三聚氰胺的奶粉有关。已知三聚氰胺为白色晶体,将它用作食品添加剂可提高食品中蛋白质的检测值,俗称“蛋白精”, 化学式为C3H6N6。据此请计算:
(1)三聚氰胺中各元素的质量比 ;
(2)三聚氰胺中氮元素的质量分数 。(写出具体的计算过程,结果精确到0.01%)
(3)某品牌合格奶粉蛋白质含量为18%,含氮量为2.88%(假设奶粉中的含氮量全部来自蛋白质)。每100g奶粉中添加0.1g三聚氰胺,理论上能增加 g蛋白质。(写出具体的计算过程,结果精确到0.01g)
(共6分)
查看习题详情和答案>>(本题包括1小题,共12分)
27.(11分)四硫化钠(Na2S4)固体可替代红磷测定空气中氧气的体积分数,反应原理为:2 Na2S4 + O2 + 2H2O = 8S↓+ 4 NaOH。
【实验资料】
①四硫化钠(Na2S4)的相对分子质量为 ,其中硫元素的质量分数为 (结果精确到0.1%)。
②四硫化钠受热时,会与空气中的水蒸气反应,生成少量有毒气体硫化氢。
③NaOH溶液呈碱性,可吸收硫化氢、二氧化碳、二氧化硫等酸性气体
④硫代硫酸钠(Na2S2O3)可溶于水,常温下与NaOH溶液不反应。
【实验过程】
①取碳酸钠、 硫粉混合后置于试管中,加热(如图1所示,夹持装置已略去),制得Na2S4,反应为4Na2CO3 + 12S + X  2
Na2S4+ 2 Na2S2O3 + 4CO2,X 的化学式为
,蘸有浓NaOH 溶液的棉花的作用是
。
2
Na2S4+ 2 Na2S2O3 + 4CO2,X 的化学式为
,蘸有浓NaOH 溶液的棉花的作用是
。
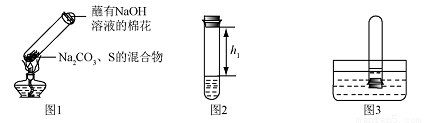
②冷却后,取下棉花,放置一段时间,再向该试管中加入10ml水,迅速塞紧橡胶塞,充分振荡,测量液面至橡胶塞下沿的距离,记录数据h1(如图2所示)
③将该试管插入水中(如图3所求),取下橡胶塞,观察到
,塞紧橡胶塞。将试管取出,倒过来,测量液面至橡胶塞下沿的距离,记录数据h2,理论上h1:h2=
④按照①~③再重复实验2次.3次实验数据如下表所示。
|
|
第1次 |
第2次 |
第3次 |
|
h1/cm |
11.2 |
11.4 |
11.6 |
|
h2/cm |
8.9 |
9.1 |
9.2 |
【解释与结论】根据第1次实验数据,计算空气中氧气的体积分数为 (结果精确到0.1%)。
【反思与评价】(1)若实验过程②中,取下棉花后,未放置一段时间即进行后续操作,会影响测定结果,请说明有何影响,并阐述理由: 。(2分)
(2)若要保证实验的效果,至少需要生成四硫化钠(Na2S4)0.174g ,则理论上实验时至少取碳酸钠粉末 克?写出计算过程(2分)
查看习题详情和答案>>
(7分)某同学进行试验探究时,欲配制10%的Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2试剂。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在未溶物。为探究原因,该同学查得Ba(OH)2在20℃时的溶解度2.1 g。
(1)烧杯中未溶物仅为BaCO3,理由是(用化学方程式表示) 。
(2)假设试剂由大量Ba(OH)2和少量BaCO3组成,设计试验方案,进行成分检验,在答题卡上写出实验步骤、预期现象和结论。
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、氯化铜溶液、烧杯、试管、带塞导气管、滴管
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。 | |
 步骤2:取适量滤液于试管中,滴加稀硫酸。 步骤2:取适量滤液于试管中,滴加稀硫酸。 | 有 ① 生成,说明有Ba2+ |
| 步骤3:取适量步骤1中的沉淀于是试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气管插入装有澄清石灰水的烧杯中。 | 试管中有 ②生成,烧杯中 ③ ,结合步骤2说明沉淀是BaCO3。 |
| 步骤4:取适量滤液于试管中, ④ 。 | 试管中有蓝色沉淀生成,说明有大量的OH—,综合上面步骤可知试剂由大量Ba(OH)2和少量BaCO3组成,假设成立。 |
五、计算与分析题(共2小题,共10分)
目前已制得的纯金属只有90余种,但由这些纯金属按一定组成和质量比制得的合金已达几千种。由于合金更容易适合不同的用途,因此被大量应用于日常生活、工农业及科学研究中。结合所学知识,完成27、28题。 查看习题详情和答案>>
(7分)某同学进行试验探究时,欲配制10%的Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2试剂。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在未溶物。为探究原因,该同学查得Ba(OH)2在20℃时的溶解度2.1 g。
(1)烧杯中未溶物仅为BaCO3,理由是(用化学方程式表示) 。
(2)假设试剂由大量Ba(OH)2和少量BaCO3组成,设计试验方案,进行成分检验,在答题卡上写出实验步骤、预期现象和结论。
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、氯化铜溶液、烧杯、试管、带塞导气管、滴管
|
实验步骤 |
预期现象和结论 |
|
步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。 |
|
|
步骤2:取适量滤液于试管中,滴加稀硫酸。 |
有 ① 生成,说明有Ba2+ |
|
步骤3:取适量步骤1中的沉淀于是试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气管插入装有澄清石灰水的烧杯中。 |
试管中有 ② 生成,烧杯中 ③ ,结合步骤2说明沉淀是BaCO3。 |
|
步骤4:取适量滤液于试管中, ④ 。 |
试管中有蓝色沉淀生成,说明有大量的OH—,综合上面步骤可知试剂由大量Ba(OH)2和少量BaCO3组成,假设成立。 |
(3)在20℃室温下, (填“能”或“不能”) 配制10%的Ba(OH)2溶液。
五、计算与分析题(共2小题,共10分)
目前已制得的纯金属只有90余种,但由这些纯金属按一定组成和质量比制得的合金已达几千种。由于合金更容易适合不同的用途,因此被大量应用于日常生活、工农业及科学研究中。结合所学知识,完成27、28题。
查看习题详情和答案>>
 (2013?丽水)工业烧碱具有较好的杀菌消毒作用且廉价易得,但工业烧碱中常含有杂质碳酸钠.某科学学习小组同学围绕工业烧碱样品纯度测定问题,展开了讨论与探究.
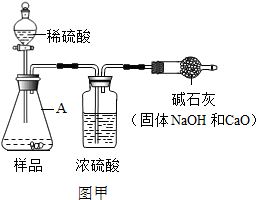
(2013?丽水)工业烧碱具有较好的杀菌消毒作用且廉价易得,但工业烧碱中常含有杂质碳酸钠.某科学学习小组同学围绕工业烧碱样品纯度测定问题,展开了讨论与探究.利用Na2CO3与稀H2SO4反应产生CO2,通过CO2质量的测定,确定样品中碳酸钠的质量,从而计算样品纯度.
(1)小科同学根据以上思路,设计了如图甲的实验方案(固定装置省略),图中仪器A的名称是
(2)小明认为图甲实验方案的设计有缺陷,若按该方案进行测定会导致难以避免的误差,如装置内空气中的CO2没有排出、反应产生的CO2未被完全吸收等.为减小误差,使CO2质量的测定更准确,该小组同学根据以上讨论,对图甲方案进行改进,设计了如图乙的实验方案(固定装置省略)
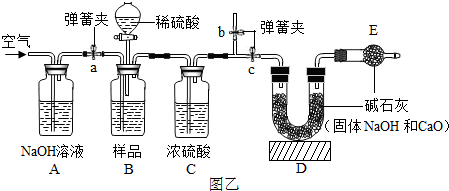 图乙B装置中样品在与稀硫酸反应前和停止反应后,都要通过量的空气,反应前通空气时a、b、c三个弹簧夹的开闭情况是
图乙B装置中样品在与稀硫酸反应前和停止反应后,都要通过量的空气,反应前通空气时a、b、c三个弹簧夹的开闭情况是(3)若撤去图乙中的C装置,则测得工业烧碱的纯度将
(4)已知Na2CO3溶液与稀硫酸反应先生成NaHCO3,当Na2CO3全部转化为NaHCO3后,生成的NaHCO3能继续与稀硫酸反应生成CO2.
现向样品中加一定量的稀硫酸,反应后产生无色气体并得到X溶液.请分析推断反应后所得X溶液的溶质,其所有的可能组成