2009年辽宁中考综合复习训练化学试题(五)
理化考试时间150分钟 化学试卷满分65分
可用到的相对原子质量 H―l C―
一、选择题(本题包括13道小题,1―11小题,每小题l分,l2、13小题每小题2分,共15分,每小题有一个最符合题目要求的选项)
1.2008年北京奥林匹克运动会上看到用大型遥控飞艇作为宣传工具以渲染活动气氛。为了飞艇在空中飞行安全而有效,飞艇内最好充入下列气体是 ( )
A.氢气 B.氦气 C.氧气 D.氮气
2.下列关于氧气的说法正确的是 ( )
A.氧气能支持燃烧,可用作燃料
B.氧气能跟所有物质发生氧化反应
C.水中的生物能依靠微溶于水中的氧气而生存
D.带火星的木条一定能在含有氧气的集气瓶中复燃
3.某溶质溶解在水中,形成的溶液与水相比较,一定不会改变的是 ( )
A.沸点 B.导电性 C.颜色 D.水分子的构成
4.食品与卫生健康密切相关。下列做法不会危害人体健康的是 ( )
A.为保持肉制品鲜美,在香肠中加过量的亚硝酸钠
B.为了增加奶粉中氮元素的含量,向奶粉中加入三聚氰胺
C.蒸馒头时加适量的纯碱
D.长期使用铝制餐具
5.齐文在学习“化学元素与人体健康”后,查阅到如下资料,请你给下表的“★”处选择恰当的选项 ( )
★ 种类
主要食物来源
钙
奶类、绿色蔬菜、水产品、肉类、豆类
铁
肝脏、瘦肉、蛋、鱼、豆类、芹菜
锌
海产品、瘦肉、肝脏、奶类、豆类、小米
碘
海产品、加碘盐
A.元素 B.分子 C.原子 D.离子
6.炒菜前,锅里正在加热的油如果燃烧起来最佳的处理方法是 ( )
A.马上向着火的油锅泼水
B.赶快将着火的油锅敞口移离火源(煤气灶)
C.立即向着火的锅里撒沙子并将锅移离火源
D.迅速盖上锅盖,或迅速倒入生冷的菜翻炒
7.不能与蛋白质发生化学反应的物质是 ( )
A.乙酸铅 B.浓硝酸 C.硫酸铵 D.甲醛
8.联肼(N2H4)和一氧化氮(NO)反应产生的能量可以作为火箭发射的动力,反应后生成两种物质:其中一种是空气中含量最多的气体,另一种是植物光合作用的原料之一,则两种物质是 ( )
A.N2和CO2 B.N2和H2O C.N2和O2 D.O2和H2O
9.下列做法能改变溶液中溶质质量分数的是 ( )
A.把氯化钠的饱和溶液恒温蒸发 B.将硝酸钾的饱和溶液升温
C.把氯化铵的饱和溶液降温 D.给蔗糖的饱和溶液中再加少量蔗糖
10.区别下列各组物质,选择的试剂或方法不正确的是 ( )
A.空气、二氧化碳、氧气………………………………………………澄清石灰水
B.羊毛毛线、棉线、腈纶线……………………………………………灼烧
C.淀粉、葡萄糖…………………………………………………………碘水
D.三种无色溶液:(NH4)2SO4、NH4Cl、Na2SO4……………………Ba(OH)2溶液
11.对下列化学变化的描述与事实相符的是 ( )
A.向氢氧化钙溶液中加入碳酸钠溶液,其溶液的pH有明显变化
B.向氢氧化钙溶液中通入二氧化碳,其溶液的质量会减少
C.向氢氧化钠溶液中滴人盐酸,溶液的pH减小,就说明发生了化学变化
D.向集满二氧化碳气体的塑料瓶中加入少量浓的氢氧化钠溶液,瓶子会变瘪,说明二氧化碳能与水反应生成碳酸
12.下列各物质能在pH=1的溶液中大量共存,且得到无色溶液的是( )
A.BaCl2、NaOH、NaCl、CaCl2 B.Mg(NO3)2、KNO3、NaCl、ZnSO4
C.CuSO4、KCl、Na2SO4、NaNO3 D.BaCl2、CaCl2、Al(NO3)3、Na2SO4
13.在一密闭容器里放入四种物质,使其在一定条件下充分反应,测得数据如下:
四种物质
甲
乙
丙
丁
反应前质量/g
25
15
1
5
反应后质量/g
11
未测
1
22
则下列表述正确的是 ( )
A.未测值为
C.该反应是分解反应 D.甲与乙反应的质量比为14:3
二、填空题(本题包括5道小题,每空1分,共14分)
14.今天中午,学校食堂的食谱见下表。请根据该食谱回答下列问题:
食谱
主食
米饭、馒头
副食
红烧鱼、凉拌黄瓜、酱茄子、海带汤
(1) 富含蛋白质的食物是____________________;
(2) 将黄瓜加醋凉拌可以存进_________________的吸收。
15.今年4月26日,2008年奥运会火炬“祥云”(如图)的发布仪式在北京举行。“祥云”不仅有着完美的外表,而且由于高科技的运用,大风、大雨天气都能正常燃烧。它采用的燃料是丙烷(化学式为C2H8),符合“绿色奥运”的要求。试回答下列问题:
(1)丙烷属于__________(填“无机物”或“有机物”);
(2)丙烷分子中,氢、碳两元素的质量之比为____________(最简整数比);
(3)火炬点燃后,所发生的反应为:C3H8+ O2
O2 3CO2+
3CO2+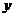 H2O,该反应中
H2O,该反应中 、
、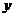 分别为__________,所用燃料符合“绿色奥运”的要求,原因是______________________。
分别为__________,所用燃料符合“绿色奥运”的要求,原因是______________________。
16.“稀硫酸沾到衣服上,时间稍长,水分蒸发,稀硫酸变浓,衣服被腐蚀。”这段话没有涉及硫酸的一个性质是__________(填“酸性”、“不易挥发”或“腐蚀性”)。除去稀盐酸中混有的少量硫酸宜选用的试剂是___________。
17.研究表明:木糖醇是一种理想的蔗糖替代品。它具有甜味足、溶解性好、防龋齿、适合糖尿病患者食用的优点。下图是木糖醇和蔗糖的溶解度曲线。请回答下列问题:
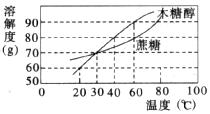
(1)在人体体温
(2)
(3)现有
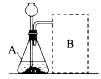
18.研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假设】H2O2生成O2的快慢与催化剂种类有关。
【实验方案】常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2和红砖粉,测量各生成一瓶(相同体积)O2所需要的时间。
【进行实验】下图是他们进行实验的装置图,此实验中B处宜采用的气体收集方法是____________,其理由是______________________________________________________。
【实验记录】
实验编号
1
2
反应物
6%H2O2
6%H2O2
催化剂
时间
152 s
35 s
【结论】该探究过程得出的结论是__________________________________________。
三、简答题(本题包括5道小题,共22分)
19.(3分)下图是元素周期表中的一部分。
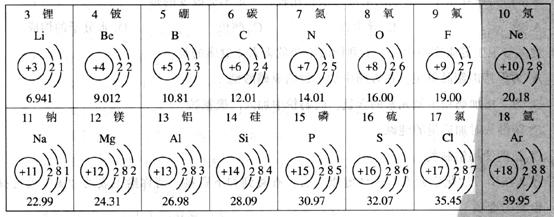
根据上图所示内容,回答下列问题。
(1)对上图所示内容说法正确的是____________;
①原子序数为14的元素是金属元素
②原子序数为15的磷原子相对原子质量为30
③氖和氩的原子核外电子排布都属于稳定结构
④从核外电子排布看钠原子容易失去电子
(2)表中不同元素最本质的区别是________________;
①质子数不同 ②中子数不同
③相对原子质量不同 ④核外电子数不同
(3)从上图中我们发现:随着原子序数的递增,其原子结构(或元素的性质)呈现的变化具有一定的规律。下面是天逸同学在学习时寻找出图中的一些变化规律,其中正确的是____________________。(填a、b、…)
①从上图的横向看: a.随着原子序数的递增,原子最外层电子数从1递增到8
b.每一横行中元素原子的核外电子层数相同
②从上图的纵向看: c.每一纵行中不同元素的原子最外层电子数相等
③从其他变化规律看: d.金属元素的原子最外层电子数一般少于4个
20.(9分)根据下列实验装置图回答问题:
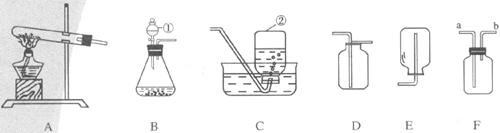
(1)请写出标号仪器的名称:①__________,②___________;
(2)若使用高锰酸钾固体制取氧气,应选择的发生装置为________________,收集装置为__________(填字母),反应的化学方程式为___________________________________;
(3)装置B可用于制备的气体有_____________(答两种);
(4)实验室在制取二氧化碳气体时常混有水蒸汽和氯化氢气体,如果用装置F来除去水蒸汽,气体应从导管__________端进入,可选用_________做干燥剂。如果用装置F来检验氯化氢气体,F中应盛放的试剂是_____________。
21.(3分)某课外小组的同学们收集了含一氧化碳和二氧化碳的废气,为了确认这种废气的组成,他们在实验室按如下装置进行了实验。
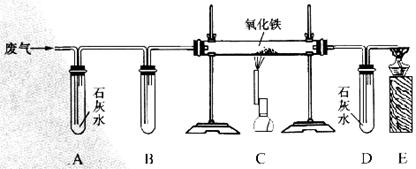
(1)B装置中盛放足量浓氢氧化钠溶液,其作用是_______________________________;
(2)C装置中发生反应的化学方程式是__________________________;
(3)A装置和D装置完全相同,其作用的不同之处是_____________________________。
22.(2分)A是一种白色难溶于水的钙盐,由三种元素组成,其相对分子质量为100。
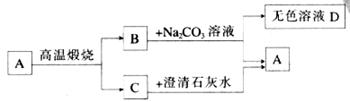
(1)写出A与盐酸反应的化学方程式:_______________________________________;
(2)D中含有的溶质可能有哪几种情况?
__________________________________________________________________________。
23.(5分)某校化学兴趣小组的同学为了探究裹在皮蛋壳外固体的成分,从资料和网上到腌制皮蛋的原料和方法。将生石灰、纯碱、草木灰(主要成分K2CO3)、食盐等用水调成糊状,敷于蛋上,密封保存,下面请你参与他们的讨论并协助完成相关实验。
(1)向烧杯中加入研碎的皮蛋外壳固体,再加入适量的水,搅拌后静置,观察烧杯底部有白色固体,该白色固体中一定含有_____________________;烧杯的上层溶液中一定含有__________________________________;
(2)为研究烧杯内的溶液中还可能含有的物质,同学们继续进行探究。
①志鹏同学从烧杯中取出少量溶液,加入稀盐酸,观察到有气泡冒出,说明溶液中含有________________;
②久馨同学从烧杯中取出少量溶液,向其中滴入酚酞试液,溶液变红。你认为该溶液中使酚酞试液变红的物质应该有__________、_________;
四、探究题(本题包括1道小题,共8分)
24.(分)请你参与某学习小组进行研究性学习的过程,并协助完成相关任务。
【研究课题】探究热水壶底部水垢的主要成分
【查阅资料】该小组同学通过查阅资料知道,天然水中一般都含Ca2+、Mg2+、HCO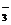 等离子,在加热条件下,这些离子趋于生成溶解度更小的物质――水垢(主要成分为碳酸盐、碱等的混合物),同时,他们还查阅到下列有关物质的溶解性:
等离子,在加热条件下,这些离子趋于生成溶解度更小的物质――水垢(主要成分为碳酸盐、碱等的混合物),同时,他们还查阅到下列有关物质的溶解性:
物质
Ca(HCO3)2
Mg(HCO3)2
Ca(OH)2
Mg(OH)2
CaCO3
MgCO3
溶解性
可溶
可溶
微溶
不溶
不溶
微溶
【提出猜测】水垢的主要成分一定含有Mg(OH)2和_______,可能含有Ca(OH)2_______。
【设计方案】(1)维靖同学在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,取上层清液加入__________________,没有白色沉淀,说明水垢中无Ca(OH)2。
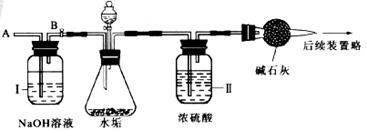
(3)林硕同学设计了下列实验装置,进一步确定水垢中含有碳酸盐的成分,其主要实验步骤如下:
①按图组装仪器,将
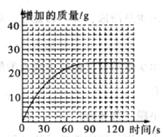
②测量一定时间内干燥管内物质增加的质量(见下列曲线);
③待锥形瓶中不再产生气泡时,打开活塞B,从导管A处缓缓鼓入一定量的空气;
④再次称量干燥管内物质增加的质量;
⑤重复③和④的操作,直至干燥管内物质质量不变。
讨论:
a.步骤①加入样品前还应检查____________________,所加的酸溶液是____________;
b.装置Ⅱ的作用是_____________________________;从导管A处缓缓鼓入一定量的空气时,装置Ⅰ的作用是_______________________________________________________;
c.研究性小组的同学通过简单计算,认为水垢中一定含有MgCO3,理由是___________。
【实验结论】通过上述研究可知:水垢的主要成分有____________________。
五、计算题(本题包括2道小题,共6分)
25.(分)四川汶川抗震救灾期间,为防止灾后疫情的发生,每天需要喷洒大量消毒液。欲配制
26.(5分)在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,加足量水溶解,制成溶液。向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:
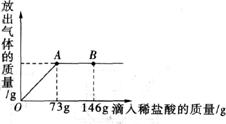
请根据题意回答问题:
(1)当滴加了
(2)当滴加稀盐酸至图中B点时,烧杯中溶液里的溶质是(写化学式)_______________。
(3)当滴加了