2008-2009学年度潍坊市诸城第一学期九年级期末考试
化学试卷
可能用到的相对原子质量:
K:39 N:14 O:16 Na:
一、选择题:(每小题只有一个选项符合题意。每小题2分,共40分)
1.“果导片”是一种常用缓泻剂,主要成分是酚酞。小聪同学欲将其作为酚酞指示剂的替代品,他将“果导片”研成粉末放入酒精中,搅拌、静置,取上层清液滴入氢氧化钠溶液中,则溶液显
A.红色 B.蓝色 C.无色 D.都不正确
2.下列物质中,不属于有机物的是
A.葡萄糖 B.纯碱 C.酒精 D.淀粉
3.小明奶奶在小明进行期末考试时制定了如下食谱:米饭、红烧鸡块、蛋汤、糖醋鱼、麻辣豆腐,为使营养均衡,你觉得最好还要补充
A.牛肉 B.河虾 C.青菜 D.雪糕
4.氮肥能使绿色植物枝繁叶茂,长势旺盛。下列化肥中属于氮肥的是
A.K3PO4 B.K2SO
5.绿色植物的光合作用在合成葡萄糖时,一般不需要
A.水 B.二氧化碳 C.太阳光 D.酶
6.根据你学过的化学知识,下列说法错误的是
A.“请往菜里加点盐”中的盐特指食盐NaCl
B.体温表中的水银不是银,是金属汞
C.发酵粉的主要成分是小苏打Na2CO3
D.生活中常用的铁制品都是铁的合金
7.下列物质中属于合成材料的是
A.陶瓷 B.聚乙烯塑料 C.生铁 D.钢筋混凝土
8.“候氏制碱法”生产过程中涉及的化学反应如下:
①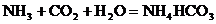
②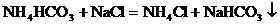
③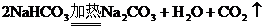
其中属于复分解反应的是
A.① B.② C.③ D.①③
9.不会加剧酸雨、臭氧层空洞、温室效应等环境问题的是
A.使用太阳能热水器 B.燃烧煤
C.超音速飞机排放尾气 D.使用氟利昂做致冷剂
10.2008年9月全国各地出现千余婴儿患肾结石病例,经确认是食用添加三聚氰胺的三鹿奶粉所致。三聚氰胺的化学式为C3N3(NH2)3,则下列有关三聚氰胺的说法错误的是
A.三聚氰胺是由三种元素组成的化合物
B.三聚氰胺的相对分子质量是126
C.三聚氰胺中的C、H、N三种元素的质量比是1┱2┱2
D.一个三聚氰胺的分子中含有15个原子
11.草木灰的主要成分是碳酸钾,某同学为检验它含有的碳酸根离子,应选择的试剂是
A.氢氧化钙溶液 B.稀盐酸和氢氧化钙溶液
C.水 D.稀盐酸
12.加酶洗衣粉易除去衣服上的汗渍、血渍及油渍。现有下列衣物:①羊毛织品②棉花织品③化纤布料④蚕丝织品。其中不宜用加酶洗衣粉洗涤的是
A.②③ B.③④ C.①② D.①④
13.某工厂拟选用下列物质处理含硫酸的废水,想花最少的钱中和等量的废水应选择
物质
氯化钠
碳酸钙
熟石灰
氢氧化钠
市场参考价(元/千克)
1.2
1.8
2.0
11.5
A.氯化钠 B.碳酸钙 C.熟石灰 D.氢氧化钠
14.玻璃中含有二氧化硅,该物质在一定条件下能与氢氧化钠反应,生成具有粘合性的硅酸钠溶液(俗称水玻璃)。下列说法正确的是
A.水玻璃属于纯净物
B.水玻璃和玻璃属于同种物质
C.二氧化硅和氢氧化钠发生化合反应
D.氢氧化钠溶液不能用带有磨口玻璃塞的试剂瓶盛装
15.小明想除去卫生间瓷砖上的铁锈痕迹,在用清水洗涤之前,他从家中选择了一种最合适的物质对铁锈进行处理,这种物质是
A.汽油 B.食盐水 C.白醋 D.米酒
16.下列哪组溶液相互混合后,溶液的pH可能等于7
A.pH=3 pH=4 B.pH=3 pH=10
C.pH=7 pH=11 D.pH=1 pH 7
17.为了增强市民的环保意识,实行垃圾回收。以下废弃物可以回收利用的是
①干电池 ②口香糖 ③菜叶 ④果皮 ⑤易拉罐
A.②③④ B.①③④⑤ C.①⑤ D.①④⑤
18.量取8mL水稀释浓硫酸的下列操作错误的是
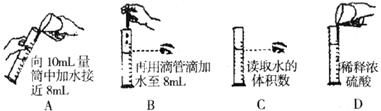
19.蛋白质、糖类、油脂是重要的营养物质。已知每克蛋白质、糖类、油脂完全氧化时,分别约放出18kJ、15.6kJ、39.3kJ的热量。产生相同热量时,消耗这三种物质的质量由大到小的顺序是
A.蛋白质、糖类、油脂 B.蛋白质、油脂、糖类
C.糖类、蛋白质、油脂 D.油脂、蛋白质、糖类
20.化学学习中常用燃烧法测定有机物的组成。
A.含有C、H元素 B.含有O元素
C.有机物可能是CH3OH D.有机物可能是C2H5OH
二、填空简答题(25分)
21.生活中处处有化学:
(1)国家提倡食用的加碘盐,是在食盐中加入一定量的碘酸钾。已知碘酸钾受热不稳定,你认为炒菜时宜__________(填“早”或“迟”)加入碘盐更有利于健康。
(2)厨房中有下列6种物质:①面粉②鸡蛋③食用油④食盐⑤青菜⑥食醋。其中富含糖类的是__________(填序号,下同),富含油脂的是__________。
(3)许多蔬菜中富含人体所需的维生素C,其化学式为C7H9O2,维生素C在pH<5的环境下稳定,为减少维生素C的损失,在炒黄瓜时应加入少量的__________。维生素C片保存时,应注意避光、避热、密封,请你据此推测维生素C的化学性质__________________________________________________。
22.“假酒中毒”事件时有发生。“假酒”一般由工业酒精加水配制而成,它含有一定量的甲醇(CH3OH),而饮用甲醇会使人的视力迅速下降、失明,甚至死亡。试回答:
(1)甲醇的工业制法为: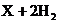

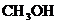 ,则X的化学式为__________。
,则X的化学式为__________。
(2)工业酒精的主要成分是乙醇,乙醇是一种重要的化工原料,现在已应用于无铅汽油。请写出乙醇燃烧的化学方程式_____________________________________。
(3)与甲醇、乙醇结构相似的化合物还有丙醇(C3H7OH)、丁醇(C4H9OH)等,这类物质称为醇类。请问:其名称中的“甲、乙、丙、丁”与其分子中的__________有关;含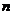 个碳原子的醇的化学式为__________。
个碳原子的醇的化学式为__________。
23.制豆腐是我国古代的一项重要发明,现在豆腐在全球已成为颇受欢迎的食品,其制作的主要工艺流程通常如下:
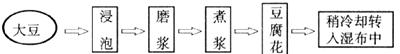
资料:下表是豆腐中主要成分的平均质量分数:
成分
水
蛋白质
脂肪
糖类
钙
磷
铁
维生素B1
维生素B2
质量分数%
89.3
4.7
1.3
2.8
0.24
0.064
1.4
0.00006
0.00003
(1)上述工艺流程中,磨浆属于__________变化,由豆腐花制豆腐的过程就是将豆腐与水分离,该设计利用的操作是__________。
(2)除水、无机盐和维生素外,豆腐中还含有的营养素中比较丰富的是__________,含人体所需的微量元素有__________。
(3)除大豆外,很多食物也能提供丰富的蛋白质。下列食物中能提供丰富蛋白质的有__________。
A.萝卜 B.鱼 C.大米 D.奶制品 E.花生油 F.苹果
24.陶是人类最早利用化学反应制造的人造材料,青铜是人类最早利用化学反应制造的金属材料,陶器、青铜器及铁器的广泛使用,极大地促进了人类社会的发展。请回答:
(1)陶、铜、铁等材料的生产离不开火,火即所谓的燃烧,其实质是一种_______(填“氧化”或“还原”)反应;而铁和铜的冶炼,主要是利用_________(填“氧化”或“还原”)反应把铁和铜从其化合物中转化出来。制陶的原料是黏土,其主要成分是二氧化硅、氧化镁、氧化铝和碳酸钙。当温度达到
(2)在①黏土②二氧化硅③氧化镁④碳酸钙⑤氧化铝⑥硅酸镁⑦硅酸铝⑧硅酸钙这8种物质中,属于混合物的有__________(填代号,下同);属于金属氧化物的有__________,属于盐的有__________,二氧化硅和碳酸钙反应的化学方程式为__________________________________________________。
(3)在生产和生活中,大量使用的不是纯金属,而是它们的合金。合金与纯金属相比,其优越的性能有_____________(答出一条即可),原因是__________________。
(4)材料常常成为一个时代的标志,如陶器时代、青铜器时代、铁器时代。在信息时代,你认为对社会有重大影响的一种人造材料是__________。
(5)地壳中铁、铝的含量分别位列金属的第二位和__________位,远多于铜,但铜却是人类最早冶炼出的金属,已有6000多年的历史,而冶铁比铜晚了3000多年,至于冶炼铝则只有200多年的历史。根据金属的性质,你认为关键的因素是_________
________________________________________。
三、实验探究题(20分)
25.请设计简单的实验解决下列问题。
(1)验证肥皂水呈碱性。
(2)验证土豆中是否含有淀粉。
(3)验证某病人是否患有糖尿病。
26.由于大量使用一次性塑料方便袋造成的白色污染已成为一个严重的社会问题。某化学兴趣小组的同学欲对某种塑料袋的组成进行分析探究(资料显示该塑料袋只含C、H两种元素),他们设计了如下图所示的实验装置,使该塑料袋在纯氧中燃烧,观察实验现象,分析有关数据,推算元素含量。
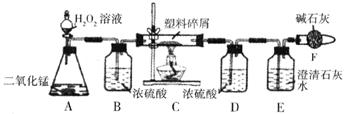
(1)仪器A中所发生反应的化学方程式____________________________________。
(2)仪器B的作用是____________________________________________________。
(3)仪器E中的现象是__________________________________________________。
(4)若仪器C的玻璃管中放入的塑料试样质量为Wg,塑料试样充分燃烧后,若仪器D增重a g,Wg该塑料试样中含氢元素的质量为________g(结果可用分数表示)。
(5)若装置中没有连接仪器B,将使该塑料试样中含氢元素的质量测算结果________(填偏小、偏大或无影响)。
27.某化学实验小组的同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡冒出。这一现象激起同学们探究的欲望,生成的气体是什么气体?
提出猜想:从物质组成元素的角度,生成的气体可能是SO2、O2、H2。
查阅资料:SO2易溶于水,能与氢氧化钠溶液反应,生成Na2SO3。
方案设计:依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是氧气,则检验方法是____________________________________。
(2)乙同学认为是SO2,则只需将放出的气体通入盛有氢氧化钠溶液的洗气瓶中,称量通入气体前后洗气瓶的质量。写出SO2与氢氧化钠反应的化学方程式________ ________________________________________。
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。
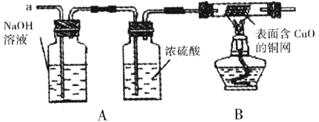
如果放出的是氧气和氢气,你认为方案中的安全隐患是____________________。丙同学认为,为确保安全,实验前应先收集一试管气体,用拇指___________。若不发出__________,方可采用上面的装置进行实验。
实验探究:经丙同学确认安全后,小组同学首先对装置A进行称量,再将收集到的气体从a通入,过一会点燃B处酒精灯,一段时间后,发现表面含CuO的铜网由黑色变为光亮的红色,停止通气,再次称量装置A,发现质量无增减。结论:产生的气体是__________。
思维拓展:
(1)由上述实验可以推出,硫酸铜溶液中可能含有__________物质。
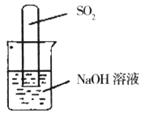
(2)不通过称量,如何判断SO2与氢氧化钠溶液发生了反应呢?有一同学设计了如下图所示装置进行实验,发现试管内液面上升,就得出SO2与氢氧化钠溶液反应的结论。其他同学认为该方案不严谨,理由是______________________________。要得到科学严谨的结论,仍利用该装置,需要补做的实验是___________________。
四、计算题:(10分)
28. 。请计算:
。请计算:
(1)参加反应的碳酸钾的质量。
(2)过滤后所得溶液的溶质质量分数。