2008-2009学年度湛江市第二中学第一学期初三年级12月月考
化学试卷
可能用到的相对原子质量:H
一、选择题:(本题共12题,每小题只有一个正确选项,每小题3分,共36分)
1.下列变化过程中,其中一种与其它三种有本质不同的是( )
A.将煤隔绝空气加强热可制得焦炭、煤焦油、焦炉气等
B.粗盐发生潮解过程
C.净化水时用活性炭除去水中的异味、色素等
D.舞台上释放干冰看到云雾缭绕的幻境
2.下列物质中,前者为化合物,后者为溶液的一组是( )
A.液氧、稀硫酸 B.氯化氢气体、盐酸
C.澄清的石灰水、二氧化碳 D.糖水、海水
3.下列实验操作中,不正确的是( )
A.稀释浓硫酸时,将浓硫酸缓慢注入水中
B.测某溶液的pH,用玻璃棒蘸一滴待测液到干燥的pH试纸上,跟比色上卡对照
C.把鼻孔凑到容器口闻浓盐酸的气味
D.不慎将浓碱溶液沾到皮肤上,立即用大量水冲洗,再涂上硼酸溶液
4.常见食物pH的近似值范围如下:
常见食物
橘子汁
泡菜
酸牛奶
鸡蛋清
pH(近似值)
3.0~4.0
3.2~3.6
6.3~6.6
7.6~8.0
下列说法中,不正确的是( )
A.鸡蛋清显碱性 B.胃酸过多的人应少吃泡菜
C.橘子汁能使石蕊溶液变红 D.酸牛奶比橘子汁的酸性强
5.生活中的下列现象,不能说明气体溶解度随温度升高而减少的是 ( )
A.烧开水时,沸腾前有气泡逸出 B.喝下汽水感到气体冲到鼻腔
C.揭开啤酒盖,有大量的泡沫溢出 D.夏季黄昏,池塘里的鱼常浮出水面
6.下面各组金属用硫酸亚铁溶液,就能比较它们的活动性强弱的是( )
A.铜和银 B.铜和锌 C.汞和铜 D.铅和汞
7.一些国家在试用碳酸水浇灌某些植物,这样做不能起到的作用是( )
A.改良酸性土壤 B.促进植物的光合作用
C.提高作物的产量 D.改良碱性土壤

A.滴加稀盐酸 B.滴加硝酸银溶液
C.品尝味道 D.加热
9.一瓶接近饱和的硝酸钾溶液中,逐渐加入硝酸钾固体。符合加入固体硝酸钾质量(m)和溶液中溶质质量(n)的关系图像是
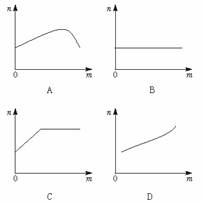
10.下图是盐酸滴入氢氧化钠溶液中有关粒子之间反应的示意图。下列说法错误的是( )
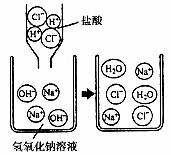
A.盐酸中含有氢离子和氯离子
B.氢氧化钠溶液中含有钠离子和氢氧根离子
C.两种溶液混合时,氢离子与氢氧根离子结合生成了水分子
D.两种溶液混合时,钠离子与氯离子结合生成了氯化钠分子
11.下列化肥与熟石灰混磨时会产生有刺激性气味气体的是( )
A.过磷酸钙 B.硫酸钾 C.氯化钾 D.硫酸铵
12.某工厂排出的废水pH小于7,并含有较多的Cu2+,对环境污染严重。从环保及回收利用考虑,较切合实际的治理方案是应加入
A.食盐和盐酸 B.石灰石和金属 C.烧碱和纯碱 D.生石灰和铁粉
二、不定项选择题(本大题包括3小题,每小题4分,共12分。每小题有一个或二个选项符合题意,全部选对的得4分,漏选得2分,错选不选得0分)
13.如下图,锥形瓶内盛有气体X,滴管内盛有液体Y。若挤压胶头滴管的胶头,使液体滴入瓶中,振荡,套在玻璃管一端的小气球慢慢 鼓起,则气体X和液体Y可能是( )
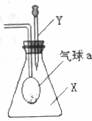
A.X是O2,Y是Ca(OH)2溶液 B.X是CO,Y是Ca(OH)2溶液
C.X是SO2,Y是NaOH溶液 D.X是CO2,Y是硫酸溶液
14.
A.蒸发掉一半的溶剂 B.蒸发掉
C.加入
15.鉴别下列各组物质,括号内选用的试剂或方法不合理的是( )
A.硫酸钾和氯化钾(观察颜色) B.碳酸氢铵和硝酸钾(闻气味)
C.生石灰和石灰石(稀盐酸) D.稀盐酸和稀硫酸(氢氧化钠溶液)
三、填空与简答题(本大题共5小题,共35分)
16.按要求用恰当的化学用语填写下列内容:(5分)
水银 ;2个硫酸根离子 ;保持氧气化学性质的最小粒子 ;
碱中的阴离子 稀盐酸中的阳离子
17.某校“酸雨”(pH<5.6)测量小组取刚降落的雨水水样,每隔几分钟测一次pH,其数据如下表(6分)
测定时刻
5:05
5:10
5:15
5:20
pH
4.95
4.94
4.88
4.86
所降雨水是否为酸雨?_____ ,在测定的期间内,雨水的酸性是增强还是减弱?________。
经调查,这一地区有一个硫酸厂(生产过程中产生SO2),这地区的工厂和生活燃料主要是煤。请你分析造成这一地区酸雨的主要原因是______________________________,你认为应采取的措施是________ 。
18.用化学方程式回答下列问题:(8分)
(1)胃酸过多时为什么可服用胃舒平(含有氢氧化铝)来减轻症状?
(2)为什么可以用稀盐酸来清洗长期盛放石灰水的试剂瓶?
(3)为什么可以用稀硫酸来清除铁锈?
(4)长期存放的氢氧化钠溶液,为什么容易发生变质?
19.(6分)下图是A、B、C三种物质的溶解度曲线,据图回答:
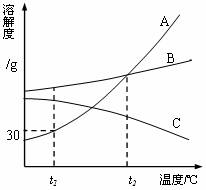
(1)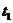 °C时A、B、C三种物质的溶解度由大到小的顺序是 (填写序号,下同)。
°C时A、B、C三种物质的溶解度由大到小的顺序是 (填写序号,下同)。
(2)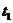 °C时30gA物质加入到
°C时30gA物质加入到
(3)将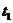 °C时A、B、C三种物质饱和溶液的温度升高到
°C时A、B、C三种物质饱和溶液的温度升高到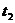 °C时,三种溶液的溶质质量分数由大小关系是
。
°C时,三种溶液的溶质质量分数由大小关系是
。
20.(10分)已知家庭常用的发酵粉主要成分为小苏打(NaHCO3)受热易分解为Na2CO3和两种氧化物A、B,且其中一种为植物光合作用所需要的气体,一种为生活中常见的无色液体。请根据下列图示关系回答下列问题:
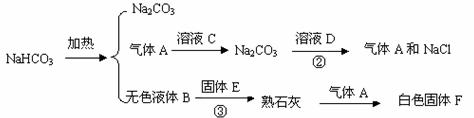
(1)请你从上述图示中推断出A、B、D、F各是什么物质?(写化学式)
A_________B D_________ F____________
(2)反应②③的化学方程式为:
②__________________________________反应的基本类型为_____________________
③__________________________________反应的基本类型为_____________________
四、实验与探究题(本大题包括3小题,共24分)
21.(10分)以下是老师提供的一些实验装置。请结合下图回答问题:
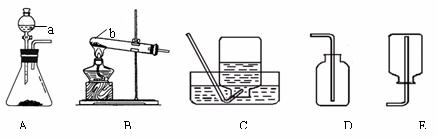
(1)写出图中标号的仪器名称:a ;b 。
(2)写出实验室用A装置制取氧气的化学方程式 。
(3)通过查阅资料得知:①氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水;②氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体。小芳同学加热氯化铵和氢氧化钙的固体混合物制取氨气,她应选择的反应的发生装置是 ,收集装置是 。(填字母编号)
(4)小芳将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是
, 。
(5)请写出氨气和氧化铜反应的化学方程式
22.下图是某同学配制
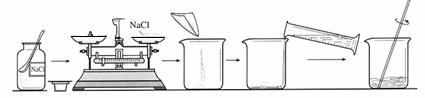
(1)请找出图中的两处错误:
① ②
(2)若其它操作正确(
(3)如果配制的盐水中,NaCl的质量分数小于5%,则可能造成误差的原因有(至少举出一条)
23.(10分)小强为探究氢氧化钠溶液中到底是哪一种粒子(H2O、Na+、OH-)能使酚酞指示剂变色,设计了一组实验,实验步骤如下:
(1)在第一支试管中加入约2ml蒸馏水,滴入几滴无色酚酞试液,观察现象。
(2)在第二支试管中加入约2mlNaCl溶液(PH=7),滴入几滴无色酚酞试液,观察现象。
(3)在第三支试管中加入约2mlNaOH溶液,滴入几滴无色酚酞试液,观察现象。
通过上述试验探究,小强得到的结论应是:
实验(1)看到的现象是无色酚酞试液不变色,得出的结论是H2O 使酚酞变色,
实验(2)看到的现象是 ,得出的结论是Na+离子 。
实验(3)看到的现象是 ,得出的结论是 。
五、计算题(本大题包括2小题,共13分)
24.(4分)尿素是一种优质的氮肥,其化学式为CO(NH2)2 ,据此进行计算:
(1)尿素的相对分子质量是 ;
(2)一袋
25.(9分)烧杯中盛有不纯的锌粒
①参加反应的锌的质量。(2分)
②所用的稀硫酸中溶质的质量分数。(3分)
③生成的溶液中溶质的质量分数。(4分)