2007-2008学年度无锡惠山区初三模拟考试
化学试卷
相对原子质量:C―12 H―1 O―16 Cl―35.5 Mg―24 Na―23 S―32 Zn―65
一、选择题(本题包括20小题,每小题1分,共20分。每小题只有l个选项符合题意)
1.下列物质的变化中,没有化学变化发生的是
A.二氧化碳使紫色石蕊溶液变红 B. 海水晒盐
C.蛋白质水解转变为氨基酸 D. 石墨在一定条件下转化为金刚石
2.下列生活中常见的“水”属于纯净物的是
A.矿泉水 B.蒸馏水 C.硬水 D.生理盐水
3.为了提醒人们注意车船上严禁携带、存放易燃品,在火车站内应张贴的图标是
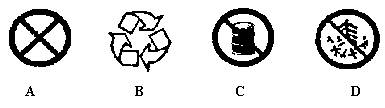
4.关于下列实验现象的描述,错误的是
A.蜡烛在氧气里燃烧生成二氧化碳和水,并放出热量
B.细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
C.镁带在空气中燃烧,发出耀眼的白光,生成白色粉末
D.红磷在氧气中燃烧产生大量白烟
5.下列物质不属于溶液的是
A.生理盐水 B.消毒酒精 C.液氮 D.碘酒
6、氯离子在人体中能够促生胃酸, Cl?和Cl属于同种元素是因为它们具有相同的
A.相对原子质量 B.核外电子数 C.最外层电子数 D.质子数
7.林强家里种的花出现叶子发黄的现象,他应该施用以下肥料中的
A.NH4HCO3 B. Ca3(PO4)
8.下列产品的开发和利用与环境保护无关的是
A.无氟冰箱 B.无铅汽油 C.无糖口香糖 D.无磷洗衣粉
9.下图所示实验操作不正确的是
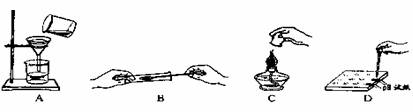
10.根据实践经验,你认为下列家庭小实验不能成功的是
A.用食品干燥剂加入水中制取石灰水 B.用6B铅笔芯做导电性实验
C.用缝衣针淬火处理后制钓鱼钩 D.用报纸与保险膜研究透气性
11.2007年2月,国家科技部通过的一项研究报告明确指出,开发新材料是国民经济和社会发展的关键。下列有关材料的说法正确的是
A.涤纶和羊毛可以通过灼烧的方法鉴别 B.任何塑料袋都可以长期盛放食品
C.橡胶都是人工合成材料 D.合成材料的使用有百利而无一害
12.
R + 5O2 3CO2 + 4H2O ,则R的化学式为( )
3CO2 + 4H2O ,则R的化学式为( )
A. C3H4 B.C3H
13.翡翠是人们喜爱的一种装饰品,翡翠的主要成份是硬玉 [化学式为NaAl(Si2O6)]。则硬玉中硅元素的化合价是
A.-4
B. +
14.在学习过程中,总结规律要严谨、全面、科学。下列总结出的规律符合这一要求的是
A.能使酚酞变红色的溶液一定呈碱性
B.根据酸碱盐的溶解性表,可判断酸、碱、盐的溶解度
C.根据常见元素的相对原子质量表,查某元素原子的中子数
D.有单质生成的反应一定是置换反应
15.鉴别下列各组物质,括号中选用的试剂或方法,不合理的是
A.C2H5OH和NaCl溶液(闻气味) B.NaOH溶液和稀H2SO4(酚酞试液)
C.Ca(OH)2溶液和NaOH溶液(稀盐酸) D.KMnO4和KClO3(观察颜色)
16.由解放军总装备部军事医学研究所研制“小分子团水”是航天专用水,具有饮水量少,在人体内储留时间长、排放量少等特点。一次饮用125毫升小分子团水,可维持人体6小时正常需水量。下列关于小分子团水的说法正确的是
A.水分子的化学性质被改变了 B.小分子团水中水分子间没有间隔
C.小分子团水中的水分子停止运动 D.小分子团水的部分物理性质与普通水有所不同
17.下图是某同学鉴别NH4HCO3、NH4Cl、KCl三种化肥的过程,其中试剂甲和乙分别可能是
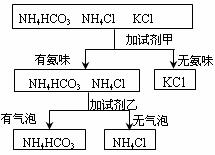
A.甲:熟石灰; 乙:稀盐酸
B.甲:水; 乙:氢氧化钠溶液
C.甲:氯化钠溶液; 乙:稀硫酸
D.甲:稀盐酸; 乙:氯化钠溶液
18.如下图所示,打开止水夹,将液体A滴人试管②中与固体B 接触。若试管①中的导管内液面上升,则液体A和固体B的组合可能是下列中的
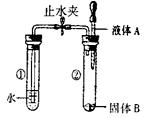
A.过氧化氢溶液和二氧化锰 B.水和硝酸铵
C.水和氢氧化钠 D.水和生石灰
19.下列物质不能发生复分解反应的是
A 氧化镁和盐酸溶液 B 氨水溶液和稀硫酸
C 碳酸钡和稀盐酸 D 氢氧化钠溶液和氯化钡溶液
20.化学中常常出现“1+1≠
A.
B.
C.
D.
二、选择题(本题包括5小题,每小题2分,共10分。每小题有1―2个选项符合题意。按题意选对给2分;错选、多选不给分;少选且选对给1分)
21.下列各组物质敞口暴露在空气中,容易发生变质的是
A.生石灰 B.浓硫酸 C.氢氧化钠溶液 D.精制食盐
22.根据你所学知识判断,下列各组物质间的转化不能一步实现的是
A.CH4 →C B.Ca(OH)2 →NaOH C. Cu →Cu(NO3)2 D.KNO3 →KCl
23.你认为下列实验方案中,可行的是
A. 按溶解、过滤、蒸发、干燥的操作顺序可以分离CaCl2、CaCO3的混合物
B. 向某种未知固体中加入盐酸,有气泡产生,则该固体一定是碳酸盐
C. 用硫在密闭容器中燃烧,除去密闭容器内空气中的氧气
D. 将pH试纸润湿后,用玻璃棒蘸取食用白醋滴在试纸上,测定其pH
24.下列所示的图象能反映相对应实验的是
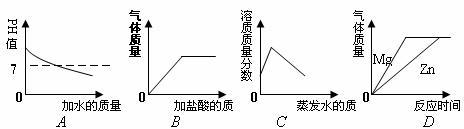
A.向PH=13的NaOH溶液中不断加水稀释;
B.向碳酸氢钠溶液中逐滴加入稀盐酸至过量;
C.将
D.将足量的金属镁片和锌片分别和等质量、相同质量分数的稀硫酸混合。
25.已知碳酸钠稳定而碳酸氢钠(NaHCO3)不稳定,受热易分解,反应的化学方程式为:
2NaHCO3加热 Na2CO3
+ CO2 ↑+H2O。现取碳酸氢钠和碳酸钠的混合物
A.反应后生成CO2的质量为3.
C.反应后生成CO2和H2O的质量比是22:9 D.原混合物中Na2CO3的质量分数为16%
三、(本题包括5小题,共26分)
26.用数字和化学符号填空:
⑴贫血患者应补充的元素 ; ⑵3个硝酸根离子 ; ⑶n个酒精分子 ;
⑷硫化钙中硫元素为-2价 ; ⑸保持氯化氢气体化学性质的最小粒子 。
27.从Ca、Na、O、C、H、N五种元素中,选用上述元素写出符合下列要求的化学式:
⑴最简单的有机物 ; ⑵可用做建筑材料的碱 ;
⑶制作汽水时常用的盐 ;⑷可用做化肥、易挥发的碱 ;
⑸厨房中常用做的甜味剂 。
28.写出下列反应的化学方程式,并在括号里注明反应的基本类型:
⑴氯酸钾与二氧化锰共热制氧气
⑵二氧化碳与水反应 , ( )反应
⑶铝丝浸入硫酸铜溶液中 , ( )反应
⑷碳化钙(CaC2)与水反应生成氢氧化钙和乙炔(C2H2)气体 。
29.以下列举的是生活和学习中可能遇到的某些情况,根据你所学知识与掌握的技能回答:
(1)“沙里淘金”说明黄金在自然界中主要以 (填:单质、化合物)形式存在。
(2)消灭柑橘害虫的“波尔多液”是用熟石灰浆与硫酸铜溶液混合而成,该混合过程中反应的化学方程式为: ;把“波尔多液”喷射到柑橘上呈现的蓝色斑点可以用厨房调料 洗净。
(3)人被昆虫叮咬后皮肤红肿起泡,这是由于昆虫在皮肤内注入了少量甲酸,此时应选择下表所列的______(填字母编号)涂在被咬的皮肤上。
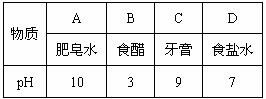
(4)走进加油站,你会发现除了各种型号的汽油之外,还多了乙醇汽油,至2007年1月,包括我市在内推广使用乙醇汽油已经一周年,提倡使用乙醇汽油的目的是 。最近,国务院颁布了“节能减排”方案,作为中学生,我们应该有节能的意识,从身边的小事做起,请你提出一条具体的节能建议 。
30.如图所示为A、B、C三种固体物质的溶解度曲线:
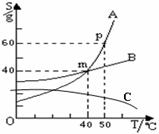
(1)曲线A和B的交叉点m表示的含义是 ;
(2)
〔3〕
(4)若将A物质从溶液中分离出来,一般采用的方法是
四、(本题包括3小题,共15分)
31.ABCD四种元素,A元素是空气中含量最多的元素,B元素是海水中含量最多的金属元素,C元素的阳离子C+是酸溶液中都含有的离子,D元素的单质是植物进行光合作用的产物,试通过分析回答:
(1)A、C两种元素的名称或符号:A ,C ;D元素的单质的化学式 。
(2)B、C、D三种元素组成的化合物的俗名是 ,A、C、D三种元素组成的酸的化学式是 。
32. 下图“五连环”中的每一环表示一种物质,相连环物质间能发生反应,不相连环物质间不能发生反应。请按照要求在环内填入不同类别的物质(填化学式):

上述“五连环”中物质间发生的反应,没有涉及的基本反应类型是_____________。
33.草酸钙(化学式为CaC2O4)在加热到
请你通过仔细观察和分析回答下列问题。
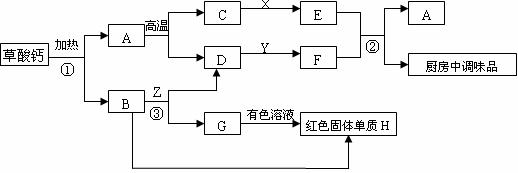
(1)写出下列物质的化学式:C ,Y , H 。
(2)写出下列反应的化学方程式:① ;
② ;③ 。
五、(本题包括4小题,共20分)
34.请回答下列问题:(在下列⑴⑵两小题中任选一题回答,若两小题都回答,则以第⑴小题的答案评定分数。)
⑴写出两种方法将饱和的硝酸钾溶液变成不饱和溶液。
⑵有两种无色溶液,分别是氢氧化钠溶液和石灰水。请你设计简单的实验加以鉴别。
35. 下图所示为实验室常用的实验装置:
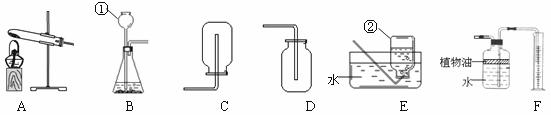 据此回答下列问题:
据此回答下列问题:
(1)实验室用加热高锰酸钾制取氧气,反应的化学方程式是 ,应选用的发生装置是 (填序号,下同),收集装置是 ;
(2)实验室通常用稀盐酸和石灰石反应制取CO2,应选择的发生装置是 ,该反应的化学方程式为 ; F装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是 ,植物油上方原有的空气对实验的结果 (填“有”或“没有”)明显影响。
36.通过“金属和金属材料”和 “燃烧”的复习,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑。在老师的帮助下,用金属钠来探究下列问题:
[问题]
1、金属钠能否置换出硫酸铜溶液中的铜?
2、金属钠能否在其他气体(如:CO2)中燃烧?
[查阅资料]金属Na性质活泼,常温下,它极易与氧气反应生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠。金属钠还可以与水剧烈反应放出氢气。
[实验一]:①在实验室中,金属钠保存在煤油中;②用镊子从煤油中取出一小块金属钠,用滤纸吸干表面煤油后投入硫酸铜溶液中,观察到溶液中出现蓝色沉淀,但没有红色的物质析出;③按照步骤②将金属钠投入水中,待反应结束后滴加酚酞溶液,发现溶液变红。
[实验二]:将燃烧的钠迅速伸入盛有CO2的集气瓶中,观察到钠在CO2中继续燃烧,反应后冷却,瓶内附着黑色颗粒,并粘附着白色物质。
[问题讨论]
(1)金属钠保存在煤油中的原因 ① 。
(2)根据上述资料和实验一中的现象写出钠块投入硫酸铜溶液所发生的反应方程式:
② ; ③ 。
(3)实验二中生成的黑色颗粒是__ ④ __,而白色物质可能是什么呢?
①同学们围绕白色物质可能是什么产生如下猜想:甲认为白色物质是氧化钠,乙认为是碳酸钠,丙认为是氧化钠和碳酸钠的混合物,丁认为是氢氧化钠。
我认为丁的猜想是错误的,理由是____________⑤ ____。
②对白色物质是什么进行实验再探究,方案设计如下:
方案1:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入无色酚酞试液,观察到溶液变成红色,结论:白色物质中一定有氧化钠。
方案2:取该样品少量于试管里,滴加足量稀盐酸,溶液中有气泡冒出,结论:白色物质中一定有 ⑥ 。
方案3:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入过量的 ⑦ 溶液(供选试剂:A.石灰水B.氯化钙溶液 C.硫酸铜溶液),出现白色沉淀,然后过滤,再向溶液里滴加无色酚酞试液,无明显现象出现。则 ⑧ _(在甲、乙、丙中选)的猜想成立。
③评价与反思:小娟同学认为实验方案1得出的结论不正确,其理由是______⑨__ __。
④结论:金属钠在二氧化碳中燃烧的化学方程式为 ⑩ 。
[应 用]实验室中的金属钠着火时,你的灭火方法是____________ __。
六、(本题包括2小题,共9分)
37.2008年北京奥运会绝对禁止运动员服用兴奋剂。乙基雌烯醇是一种蛋白同化雄性类固醇兴奋剂,其化学式为C20H32O 。试计算:
(1) 乙基雌烯醇的相对分子质量为 。
(2) 乙基雌烯醇中C、H、O三种元素的质量比 。
(3) 克乙基雌烯醇含有
38.现有HCl和MgCl2的混合溶液共
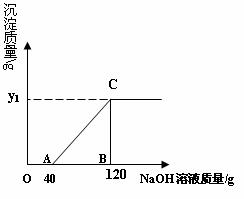
(1) 与混合溶液中的盐酸恰好完全中和时消耗的氢氧化钠溶液的质量为 克;
(2)上述反应中生成的氢氧化镁沉淀的质量;
(3)反应至C点时溶液中溶质的质量分数。