2007年内江市初中毕业会考暨高中阶段招生考试
理科综合化学部分
本试卷分为第I卷(选择题)和第Ⅱ卷(非选择题)两部分。
第1卷选择题
可能用到的相对原子质量:H―l O―
选择题(每小题3分.共36分)
13.潜水员在深水下呼吸所用的人造空气,是由氦气和下列哪一种气体混合而成
A.氧气 B.氢气 c.二氧化碳 D.天然气
14.下图所示变化属于化学变化的是

15.保护我们的环境,就是保护我们的家园――地球。下列气体排入大气中能形成酸雨而污染环境的是
A.CO2 B.SO
16.随着科学的进步。化学与人类健康的关系越来越密切了。下列说法错误的是
A.糖、蛋白质、无机盐等都是人类维持生命和健康所必需的营养物质P
B.生活中,可以用无毒的聚乙烯薄膜包装食品
C.人体内如果缺少铁元素易患缺铁性贫血
D.为提高粮食产量。应大量使用化肥和农药
17.下列安全常识中.不正确的是
A.稀释浓硫酸――将水倒入浓硫酸中
B.在加油站附近―一禁止吸烟
C.煤气、天然气等可燃性气体泄露――严禁开关电器
D.逃离火灾现场――用湿毛巾捂住口鼻
18.极少数青少年有吸烟的恶习,香烟的主要成份很复杂,经燃烧产生的烟气中含有许多强致癌物质和有害物质,其中对人体危害最大的是尼古丁(化学式为C10H14N2:)、焦油、一氧化碳等,下列说法错误的是
A.吸烟严重危害人的身心健康
B.尼古丁由碳、氢、氮元素组成
C.尼古丁属于单质
D.CO能与血液中的血红蛋白结合,故有毒
19.下列食品显碱性的是

A.牛奶 B.苹果 C.豆制品 D.蕃茄
20.北京市正在实施“人文奥运文物保护计划”,其中修缮长城使用了大量的氢氧化钙。下列关于氢氧化钙的说法中错误的是:
A.可用生石灰和水反应制得 B.使酚酞试液变红色
c.可与CO2反应 D.其钙元素的化合价为+l价
21.我国国产芯片“龙芯二号”的核心部件是以高纯度的单质硅为原料制造的,Si的制备原理之一是:SiClx + 2H2  Si+yHCl。该反应式中的x, y分别是
Si+yHCl。该反应式中的x, y分别是
A.2、4 B.4、
22.下列图示的化学实验基本操作中,正确的是

23.下图形象地表示了氯化钠的形成过程。下列相关叙述中不正确的是

A.钠原子在化学反应中容易失去电子 B.钠原子与钠离子都不显电性
C.氯原子得到电子形成氯离子 D.氯化钠由钠离子和氯离子构成
24.下列化学方程式书写正确的是
A.铁丝在氧气中燃烧:Fe + O2 FeO2
FeO2
B.电解水:2H2O H2 + O2
H2 + O2
C.铁加入硫酸锌溶液中:Fe+ZnSO4 ==== FeSO4+Zn
D.碳酸钠与稀盐酸反应:Na2CO3+2HCl===2NaCI+CO2↑+H2O
第Ⅱ卷非选择题
化学(共64分)
一、填空【本大题包括7小题,共32分)
1.有下列物质:①O2 ②CO2 ③H2 ④氦气 ⑤硬水 ⑥软水 ⑦淀粉。请用序号填空。
(1)能使带火星的木条复燃的是________;
(2)遇碘水变蓝色的是________;
(3)加入肥皂水发生反应产生白色垢状物的是________;
(4)化学性质不活泼,可作焊接金属的保护气的是________;
(5)能使燃着的木条熄灭且其固体可用于人工降雨的是________;
(6)在空气中能点燃且产生淡蓝色火焰的是________。
2.1958年毛主席到我市某炭黑厂视察。炭黑(即单质碳)是用天然气(CH4)与空气不完全燃烧制得,写出此反应的化学方程式____________,其反应类型为________反应。
3.我市某县有较丰富的煤炭和石灰岩资源,当地利用这些资源进行炼焦、炼铁。写出在炼铁过程中涉及到的以下两个反应的化学方程式。
(1)石灰石(主要成分为CaCO3)高温分解________;
(2)赤铁矿(主要成分为Fe2O3)在高温下与一氧化碳反应______。
4.医疗使用的生理盐水的溶质质量分数约为0.9%,若要配制
5.下图是A、B两种物质的溶解度曲线。

(1)由此曲线你获得的信息有(任写一点) ____________________________________。
(2)把t
a.溶液仍然是饱和溶液
b.溶液变成了不饱和溶液
c.溶剂的质量一定变小
d.溶液中溶质的质量不变
6.欲除去下列物质中的少量杂质(括号内是杂质),从水、碳酸钠溶液、碳酸钙、硝酸银溶液中选择必要的试剂,将所选试剂填写在横线上。
(1)NaNO3 溶液[NaCl] (2)NaOH溶液[Ca(OH)2]。
7.处理胶片的废液中含大量AgNO3、Zn(NO3)2:和Fe(NO3)2,若随意排放不仅会造成严重的污染,而且造成资源浪费。某同学从上述的废液中回收金属银并得到副产品绿矾(FeSO4?7H2O),其回收流程如下:
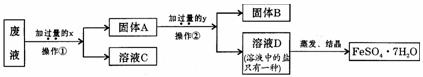
(1)操作②是____________,(2)固体A中含____________,y是____________。
二、简答题(本大题2小题,共6分)
8.袋装食品通常采用在食品袋内充入氮气,这是为什么?
9.(1)酒精灯不使用时,为什么要用灯帽将酒精灯盖住?
(2)如下图所示,在酒精灯灯杆内插入一节粗的铜丝,点燃酒精灯,酒精燃烧比未插铜丝时燃烧更旺,这是为什么?

三、实验探究题(本大题包括2个小题,共18分)
10.某同学设计了如下图所示的装置,欲进行多种实验的探索。
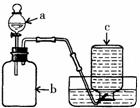
(1)仪器a的名称是____________
(2)用此装置及实验室的常见试剂可制取的气体有:____________(填序号)
A.H2 B.CO
(3)若用此装置及实验室常见仪器从集气瓶b中“捕捉”约30ml空气于集气瓶c中的操作是____________
11.某化学兴趣小组的同学用纯锌粒与稀盐酸反应制氢气时,发现产生气泡的速度较慢。就采用补加浓度更大的盐酸来提高反应速度,但不小心误加了CuSO4溶液,结果产生气泡的速度也大大加快,于是他们对此问题进行实验探究。
[提出问题]:此反应速度明显加快的原因是什么?
[猜想]:①加入的CuS04溶液中的SO42-使反应速度加快
②加入的CuSO4溶液中的H2O使反应速度加快
③加入的CuSO4溶液中的Cu2+ 使反应速度加快
④加入CuSO4溶液后,锌置换出的少量铜使反应速度加快
你认为最不可能的猜想是__________ (填序号,下同)。
[实验验证]:用a、b、c、d四支干净试管取等质量且过量的纯锌粒后,再分别向试管中加入同体积同溶质质量分数的稀盐酸。向试管中加锌粒的操作为:________________________
____________________________________________________________。
锌与稀盐酸反应的化学方程式为:____________________。请继续完成下表:
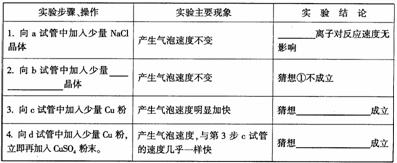
[结论]:在锌和稀盐酸反应时,当加入可溶性铜盐或铜粉,可加快化学反应速度。
四、计算题(本题8分)
12.某环保小组监测到一工厂向河水中排放的酸性废液中含有CuSO4。
(1)CuSO4是重金属盐,能与蛋白质发生__________变化(选填“物理”、“化学”),使蛋白质失去原来的生理功能,所以CuSO4有毒。
(2)为了测定废液中CuSO4的质量分数,该小组取了
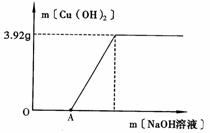
①说明图中的OA段未生成Cu(OH)2沉淀的原因。
②计算废液中CuSO4的质量分数(写出计算过程,结果保留1位小数)。
③如果仍取l