2007-2008学年度淄川区第一学期期末考试
初四化学试题
可能用到的相对原子质量:
H:1 C:l2 O:16 S:32 Ca:40 C1:35.5
第Ⅰ卷(选择题,共40分)
一、选择题(本题包括20道小题,每小题只有一个正确答案,每题2分,共40分。)
1.下列变化过程中,没有新物质生成的是( )
A.高炉炼铁 B.土壤酸化 C.汽油挥发 D.瓦斯爆炸
2.下列气体中,不能用固体氢氧化钠作干燥剂的是( )
A.氢气 B.氧气 C.二氧化碳 D.一氧化碳
3.下列说法正确的是( )
A.生铁就是钢,因为主要成分都是铁 B.人和动物体内都含有铁
C.纯铁是很硬、很脆的金属
D.铁的密度为7.
4.葡萄糖的化学式为C6H12O6,下列说法错误的是( )
A.含有三种元素,分别是碳、氢、氧元素
B.该分子的相对分子质量为180
C.该分子中有6个氧原子、l2个氢分子、6个碳原子
D.葡萄糖中C、H、O元素的质量比为6┱1┱8
5.人体通过食物获得蛋白质的主要作用是( )
A.与水发生一系列反应,最终变成葡萄糖
B.在肠胃道里与水发生反应,生成氨基酸
C.调节新陈代谢、预防疾病
D.维持恒定体温提供能量
6.有一块农田不长庄稼,经测定是酸性太强,可以适当施入( )
A.石灰石 B.熟石灰 C.草木灰 D.氮肥
7. 一次性就能将澄清石灰水、稀硫酸、食盐水三种溶液区分开的试剂是( )
A.二氧化碳气体 B.无色酚酞试液 C.氯化钡溶液 D.碳酸钠溶液
8.下列说法中不正确的是( )
A.用铅笔芯的粉末可使锁的开启变得灵活
B.在煤炉上放一盆水可防止煤气中毒
C.用盐酸和澄清石灰水可以证明鸡蛋壳的主要成分中含有碳酸根
D.食醋和纯碱反应所生成的气体可使燃着的蜡烛熄灭
9.下列实验操作,错误的是( )

A.蒸发 B.稀释浓硫酸
C.点燃酒精灯 D.检查装置的气密性
10.我国发射的“嫦娥I号”卫星,卫星运载火箭的动力由高氯酸铵(NH4ClO4)分解提供。高氯酸铵分解有可能排入大气的物质是( )
A.H2O B.SO2 C.CO2 D.CO
11.金属X、Y、Z分别是Fe、Al、Cu、Ag中的一种,其中X能与稀H2SO4反应生成X2(SO4)3,而Y、Z不能与稀H2SO4反应;Y能与AgNO3溶液反应,而Z不能与AgNO3溶液反应,则X、Y、Z依次为( )
A.Fe、Ag、Cu B.Fe、Cu、Ag C.Al、Cu、Ag D.Al、Ag、Cu
12.下列各组离子,能大量共存且形成无色溶液的是( )
A.H+、Ag+、 、
、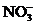 B.
B. 、Fe3+、
、Fe3+、 、
、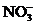
C.H+、Na+、 、
、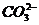 D.H+、Na+、
D.H+、Na+、 、
、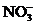
13.下列说法中正确的是( )
A.不饱和溶液降温不一定会变成饱和溶液
B.饱和溶液一定是浓溶液
C.溶液中溶质质量分数的大小只由所含溶质质量决定
D.相同温度下,饱和溶液一定比不饱和溶液浓
14.下列各种情况下,埋在地下的铸铁输气管道被腐蚀速度最慢的是( )
A.在潮湿、疏松、透气的土壤中 B.在呈酸性的土壤中
C.在干燥、致密、不透气的土壤中 D.在含沙粒较多、潮湿透气的土壤中
15.下列关于实验操作中先后顺序的叙述错误的是( )
A.实验室制取气体时,先装药品,再检查装置气密性
B.用托盘天平称量药品时,先调节天平平衡,再称量
C.实验室用CO与Fe2O3反应制取铁时,先通CO,再点燃酒精灯
D.稀释浓硫酸时,先在烧杯内倒入水,再缓慢注入浓硫酸,并不断搅拌
16.
A.积极开发可再生能源
B.大力推广使用一次性餐具
C.严格控制企业排污
D.尽量杜绝自来水的跑、冒、滴、漏现象
17.下列说法不正确的是( )
A.纯碱属于碱类,可用于玻璃、造纸、纺织、洗涤剂的生产
B.小苏打是制造发酵粉的主要成分之一,还可以治疗胃酸过多
C.大理石、石灰石的主要成分相同,都是重要的建筑材料
D.胃液中含有适量的盐酸,帮助消化,增加食欲
18.生活中的下列物质,都含有对人体健康构成威胁的有毒成分。其中,通过呼吸导致中毒的是( )
A、煤气(一氧化碳) B、假酒(甲醇)
C、霉米(黄曲霉毒索) D、假盐(亚硝酸钠)
19.小红观察在不同酸碱度下紫甘蓝(见下图)汁液所显示的颜色,记录如下:
pH
1
2~3
4~6
7~9
10
11
12~14
颜色
深红
紫红
浅紫
蓝
绿
黄绿
黄

下列物质中,能使紫甘蓝汁液变黄的是( )
A.水 B.食盐溶液 C.硫酸溶液 D.氢氧化钠溶液
20.化学的发展对改善人们的生存环境和推进现代社会文明有着积极的作用,下列各项利用化学变化与其所要达到的目的不相符的是( )
A.合成药物 抑制细菌和病毒
B.生产化肥、农药 增加粮食产量
C.开发新材料、新能源 改善生存条件,提高生活质量
D.合成食品添加剂 增进人体健康
第Ⅱ卷(非选择题,共60分)
二、理解与应用(每空1分,方程式2分,共29分)
21.(5分)在碳、氢、氧、钠、氯五种元素中选择适当元素,组成符合下列要求的物质,将其化学式填入空格中。
(1)侯氏联合制碱法中的“碱”是 (2)食醋中含有的酸
(3)能引起温室效应的气体是
(4)具有还原性的气态氧化物
(5)从人类生存环境角度考虑,比较理想的气体燃料是 。
22.(4分)家庭厨房实际上就是一个化学世界,“柴米油挂酱醋糖”等都是化学物质。让我们一起走进厨房,用你学过的化学知识解答下列问题:
(1)部分城市家庭厨房中的“柴”是“天然气”,写出天然气主要成分能化学式 。
(2)米中含有淀粉,可用于酿酒。在酿酒过程中,淀粉先转化为 ,再发酵生成酒精;
(3)加碘食盐所含碘酸钾(KIO3)中,I元素的化合价是 ;
(4)食醋不慎滴在大理石台面上,会使其失去光泽,变得粗糙。这是因为食醋中的醋酸与大理石中的 发生了化学变化。
23.(4分)“无土栽培”是一项利用化学试剂配成的营养液来栽培植物的新技术。下表是某实验小组的两种营养液的配方。请你回答有关问题:
配方Ⅰ
配方Ⅱ
KCl
KNO3
KH2PO4
Ca(NO3)2
MgSO4
(NH4)3PO4
CaSO4
MgSO4
FeCl3
备注:①各用
(1)配方Ⅰ中属于复合肥料的物质是 ;
(2)判断所用的水是否是硬水的方法: ;
(3)从均衡养分的角度分析,选用 (填“配方Ⅰ”或“配方Ⅱ”)种植的同种植物在其他条件相同时长势会更好,其理由是 。
24.(5分)下图是A、B、C三种固体物质的溶解度曲线示意图,试回答下列问题。

(1)
(2)
(3)将
(4)
25.(3分)化学与人体健康密切相关。食糖中的主要营养成分如:糖类、油脂、蛋白质、维生素等,对人类的生命活动具有重要意义。作为处在身体生长发育关键时期的中学生,不能偏食、挑食,每天都要摄入足够、均衡的营养。
(1)某向学平时不吃饭,只吃菜,结果出现乏力、疲倦甚至昏迷等症状,他缺少的营养成分是 ;
(2)某同学在毕业体检时,检查出蛋白质摄入量不足。假如你是一名医生,你会建议他在平时的饮食中应该多吃的食物是 ;(任填一种)
(3)根据你所学过的知识,利用家庭生活用品也可以对食品中的主要营养成分进行检验。下列实验能完成的是 。
A、葡萄中是否含有葡萄糖 B、检验豆油中是否掺有少量花生油
C、检验土豆中是否含有淀粉
26.(4分)商代的司母戊方鼎标志着我国在3000多年前青器铸造已达到一个较高的水平。西汉时期,我国首开“湿法炼钢”之先河,西汉刘安所著的《淮南万毕术》中已有“曾青得铁化为铜”的记载。试回答下列问题;
(1)青铜属于 (填“高分子材料”、“合金”“复合材料”)中之一。
(2)“湿法炼铜”的原理可用一个化学方程式表示为:
(3)上述化学反应属于 反应。
27.(4分)某无色混合气体中,可能含有H2、N2、CO、CO2、HCl中的几种,现将该气体经下列处理(假设每步反应或作用都是完全的)。请回答下列问题:
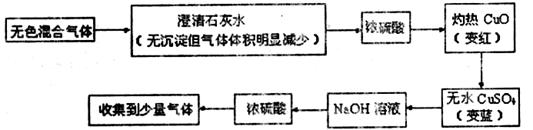
(1)通过澄清石灰水时,无沉淀但气体体积明显减少,说明原混合气体中一定含有 ;写出该反应的化学方程式 。
(2)通过无水硫酸铜变蓝,说明原混合气体中一定含有 。
三、实验与探究(共21分)
28.(13分)请你参与某学习小组的探究活动,并回答相关问题。某化学兴趣小组的同学把氢氧化钠的片状固体放在表面皿中,离开实验室。三天后进行观察。
发现问题:三天后片状圆体变成白色粉末状固体了
提出问题:“白色粉末固体物质是什么?”
建立假设:
设计实验:请你来完成以下实验,把相关内容填写在表格中。
实验方法及操作
可能观察到的现象
实验结论
反思与应用:
我们学过的哪些物质还具有这样的性质?
应如何保存这些物质
写出有关反应的化学方程式 ; ; 。
29.(8分)某课外小组的同学们收集了含一氧化碳和二氧化碳的废气,为了确认这种废气的组成,他们在实验室按如下装置进行了实验。
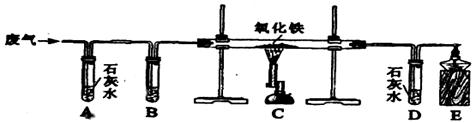
(1)B装置中盛放足量浓氢氧化钠溶液,其作用是 。
(2)C装置中发生反应的化学方程式是 。
(3)A装置和D装置完全相同,其作用的不同之处 。
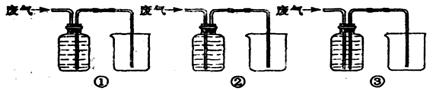
(4)该小组同学认为废气中的一氧化碳可以利用,于是设计如下装置除去废气中的二氧化碳,并收集一瓶一氧化碳,准备进行后续地探究。其中最合理的装置是 (填序号,瓶内为氢氧化钠溶液)。
四、分析与计算(共10分)
30.(3分)制作“叶脉书签”需要
(1)配制时需要氢氧化钠固体的质量是 g,水的质量是 g;
(2)若用20%的氢氧化钠溶液和水配制,需要20%的氮氧化钠溶液质量是 g。
31.(7分)鸡蛋壳的主要成分是碳酸钙,为了测定蛋壳中碳酸钙的质量分数,小刚和小勇同学进行了如下实验:
(1)他俩将蛋壳洗净、干燥并捣碎放在烧杯里,然后往烧杯中加入足量盐酸(假设除碳酸钙外,其他成分不与盐酸反应)。
(2)实验过程和测定的相关实验数据如图所示。

①小刚根据“蛋壳残渣质量为
②小勇根据“反应过程中减少的质量”为(
(3)小刚和小勇根据不同的数据求得蛋壳中碳酸钙的质量分数有明显差别,请你分析其中可能的原因。