2007-2008学年度滕州市第一学期期末考试暨九年级第一次调研考试
理科综合化学试题
第Ⅰ卷(选择题,共24分)
可能用到的相对原子质量:H.1 C.12 N.14 O.16 Na.23 Mg.24 S.32
一、选择题(本大题包括12个小题。每题2分,共24分。每小题只有一个选项符合题意。)
1.下列药品中,不需要密封保存的是
A.浓盐酸 B.浓硫酸 C.烧碱 D.食盐
2.下列说法中,正确的是
A.若药品无毒,可以品尝药品的味道
B.用剩的药品要放回原试剂瓶,不能浪费
C.加热试管里的液体时,试管口不能朝着人
D.稀释浓硫酸时,把水注入浓硫酸中,并不断搅拌
3.下列物质在日常生活中都遇到过,其中能使紫色石蕊试液变红的是
A.食盐水 B.白醋 C.肥皂水 D.石灰水
4.葡萄糖(C6H12O6)供给人体活动和维持体温所需能量的反应可表示为:C6H12O6+6O2 CO2+6H2O,下列分析错误的是
CO2+6H2O,下列分析错误的是
A.医疗上可用一定质量分数的葡萄糖溶液给病人输液以补充能量
B.葡萄糖缓慢氧化转变成二氧化碳和水,同时产生能量
C.人呼出的气体和吸人的空气的成分相比,CO2和H2O的含量增加,O2的含量减少
D.葡萄糖氧化产生的CO2如不能及时排出人体,则血液的pH将增大
5.用pH试纸测定白醋的酸碱度时,如果先将试纸用蒸馏水湿润,再把白醋滴到试纸上,则测得的结果与白醋实际的pH比较
A.偏低 B.偏高 C.相等 D.无法比较
6.某工厂排放的废水经测定pH为3,为治理废水,需将pH调至8。为此,可向该废水中加入适量的
A.生石灰 B.硫酸 C.食盐 D.氢氧化钠
7.能把氧气、二氧化碳和甲烷三种气体区分出来的方法是
A.用燃着的木条 B.滴人紫色石蕊试液
C.用水 D.滴人澄清石灰水
8.t℃时,将某硝酸钾溶液第一次蒸发掉10g水,冷却至原温度析出晶体1g;第二次蒸发掉10g水,冷却至原温度析出晶体3g;第三次再蒸发掉10g水,冷却至原温度析出的晶体应
A.等于3 g B.大于或等于3 g
C.不等于3 g D.小于或等于3 g
9.结晶是分离可溶性固体混合物的一种常用方法。我国北方有许多盐湖,湖水中溶有大量的碳酸钠和氯化钠,那里的农民冬天捞碱(碳酸钠),夏天晒盐(氯化钠)。请你判断下图中能反映氯化钠溶解度变化的曲线是
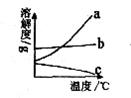
A.a B.b C.c D.无法判断
10.现将40℃时的一杯硝酸钾溶液降温至20℃,结果有少量晶体析出,则下列说法错误的是
A.40℃时的溶液一定为饱和溶液 B.20℃时溶液中溶质的质量比40℃时小
C.20℃时的溶液一定为饱和溶液 D.溶剂的质量没有改变
11.在粗盐提纯实验中,滤液放在蒸发皿里用酒精灯加热,当蒸发皿里( )时,就要停止加热
A.水分全部蒸去 B.滤液开始沸腾
C.出现大量固体 D.出现少量固体
12.海水提取金属镁的过程为:海水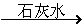 Mg(OH)2
Mg(OH)2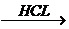 MgCl2
MgCl2 Mg,Mg在空气中放置可生成MgO保护膜。上述过程中没有发生的反应类型是
Mg,Mg在空气中放置可生成MgO保护膜。上述过程中没有发生的反应类型是
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
第Ⅱ卷(选择题,共26分)
二、填空与简答题(本大题包括4个小题,共15分)
13.(3分)根据下图信息回答下列问题:
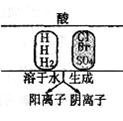
(1)上图中三种酸溶于水时生成的阳离子全部是____________。
(2)由上图可以推出,它们具有相似的化学性质。请写出氢溴酸(HBr)与Ca(OH)2溶液反应的化学方程式__________________________________________________________________。
14.(3分)已知A、B分别是盐酸溶液和NaOH溶液中的一种,下图表示向A中加入B时溶液pH变化的曲线。请写出你从曲线图中获得的信息:
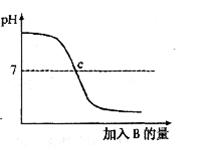
(1)A是_______________________________________________________;
(2)B是_______________________________________________________;
(3) _______________________________________________________。
15.(3分)t℃时,分别向盛有10g水的A、B两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如下图1所示的现象。
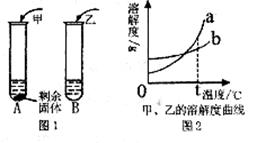
(1)t℃时,___________ (填“A”或“B”)试管中的溶液一定是饱和溶液。
(2)上图2中可表示甲物质的溶解度曲线的是___________ (填“a”或“b”)。要使A试管中剩余的固体继续溶解可采用___________的方法。
16.(6分)小新在网上查知牙膏的主要成分后,他将一定比例的极细的碳酸钙粉末和食盐倒入小烧杯中,然后加入适量的保湿剂甘油、甜味剂和香精等,搅拌均匀后即得自制牙膏。
(1)牙膏是___________ (填纯净物、混合物)。
(2)小新测得自制牙膏的pH为8.1,显___________ (填酸性、碱性、中性),自制牙膏可使紫色石蕊试液变成___________色。
(3)牙膏中的碳酸钙粉末作摩擦剂,提高洁齿效果。这种碳酸钙是将二氧化碳通入石灰浆制得的,请写出反应的化学方程式___________________________________________;往这种牙膏中滴加稀盐酸,发生的现象是___________,反应的化学方程式是______________________________。
三、实验与计算题(本大题包括1个小题.共11分)
17.(11分)某同学探究酸碱中和反应是放热反应,他进行了下列实验操作:取稀硫酸30mL(密度为1.14 g/cm3),用温度计测出温度为13℃。然后向其中加人5.6 g NaOH固体,恰好完全反应。再用温度计测出温度为22℃。由此,该同学得出NaOH与稀硫酸发生的中和反应是放热反应的结论。请回答下列问题:
(1)该同学所得结论的依据是否科学? ___________ (选填“科学”或“不科学”)理由是_________________________________。
(2)根据本实验的目的,该实验需要控制的变量是______________________;请你改进他的实验操作____________________________________________。
(3)求算稀硫酸的溶质的质量分数。(精确到0.01)