2007年江西省南昌市初中毕业暨中等学校招生考试
化学试卷
说明:1.本卷共有4大题,24小题。全卷满分60分,考试时间为80分钟。
2.本卷可能用到的相对原子质量:H―
一、选择题(本大题包括15小题,其中第1―10小题每小题1分,第11―15小题每小题2分,共20分。每小题只有一个选项符合题意。)
1.下列能量的转化过程中,主要发生了化学变化的是
A.电热器取暖 B.蜡烛照明 C.水力发电 D.太阳能供热
2.下列物质分别加入适量水中充分搅拌,不能得到溶液的是
A.小苏打 B.食盐 C.火碱 D.茶油
3.下列属于复分解反应的是
A.Fe+CuSO4===FeSO4+Cu B.CaCO3====CaO+CO2↑
C.H2SO4+2NaOH====Na2SO4+2H2O D.CH4+2O2 CO2+2H2O
CO2+2H2O
4.钛铁矿主要成分的化学式为Fe TiOx,其中铁元素和钛元素的化合价均显+3价。则x为
A.2
B.
5.下列物质的用途,是利用其物理性质的是
A.干冰用于人工降雨 B.盐酸用于除铁锈
C.氧气用于医疗急救 D.熟石灰用于改良土壤酸性
6.下列粒子结构示意图中表示离子的是

7.某饮品的主要成分为:脂肪、鸡蛋蛋白粉、钾、钙等。该饮品不能为人体补充的营养素是
A.无机盐 B.油脂 C.蛋白质 D.维生素
8.我们的生活需要化学。日常生活中的下列做法,不正确的是
A.用甲醛浸泡海产品杀菌和保鲜 B.发酵后的面团中加入纯碱做馒头
C.液化气泄漏时关闭阀门并开窗通风 D.用洗洁精洗去餐具上的油污
9.据报道,江西南昌被美国《新闻周刊》评选为2006年“全球十大最有活力的城市”,这将掀起又一轮南昌投资热。为避免投资办厂引起的环境污染,下列措施可行的是
A.对工厂的烟囱加高处理 B.工厂废水直接排放
C.对工厂的固体废弃物进行无害化处理 D.化工厂建在居民区
10.虾青素(C40H52O4)是一种具有极强的抗肿瘤、抗氧化性能的物质,可增强动物免疫力。下列有关它的说法正确的是
A.虾青素是由96个原子构成 B.虾青素是一种氧化物
C.虾青素的相对分子质量是596 D.虾青素中碳、氢、氧元素的质量比为10┱13┱1
11.下图是某品牌服装标签。下列有关错误的是

A.羊毛属于合成纤维
B.该服装面料不耐高温
C.羊毛和涤纶可用燃烧法区别
D.加入涤纶可增强面料的耐磨性
12.下表记录了物质X的溶液分别加入到另外三种物质的溶液中产生的现象。则物质X的化学式可能是
氢氧化钠
碳酸钠
石蕊
物质X
无明显现象
产生气泡
溶液变红
A.Ca(OH)2
B.CuSO
13.对容器口进行磨砂处理可提高容器的密封性。下列仪器中队容器口没有进行磨砂处理的是

14.下列说法不正确的是
A.铵态氮肥一定不能与碱同时施用 B.原子中质子数一定等于中子数
C.PH>7的溶液一定是碱性物质 D.酸溶液中一定含有氢离子
15.下列图象能正确反映其对应操作中各量变化关系的是
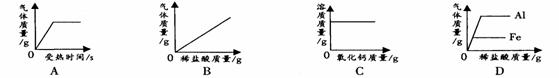
A.用一定质量的高锰酸钾加热制氧气
B.向一定质量的石灰石中加入过量的稀盐酸
C.向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体
D.分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量
二、填空题(本大题包括5小题,每空1分,共18分)
16.(4分)请将下列短文中带点的部分,用恰当的化学用语填写在横线上:
太阳镜具有保护眼睛的功能。它的镜脚一般是由塑料(其中含有碳元素 )制成的,玻璃镜片的主要成分是二氧化硅 ,且变色玻璃中含有银离子 ,铜制镜框使用时间过长会生成铜绿[Cu2(OH)2CO3],铜绿中氢氧根离子的化合价显―1价 。
17.(2分)毕业联欢会上,小明表演了一个小魔术:将一根铜丝绕成线圈,罩在蜡烛火焰上(如右图所示),观察到火焰立即熄灭;再将铜圈加热后罩在蜡烛火焰上,观
察到蜡烛照常燃烧。请你分析产生上述现象的原因:
、 。
18.(3分)用化学方程式解释下列问题:
(1)铝具有良好的抗腐蚀性能,其原因是 ;
(2)氢氧化钠露置在空气中会变质,其原因是 ;
(3)食品包装袋内常用生石灰做干燥剂,其原因是 。
19.(5分)甲、乙、丙三种物质的溶解度曲线如右图所示。据图回答:
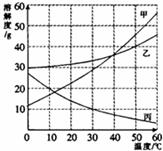
(1)
(2)
(3)要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是 ;
(4)
20.(4分)A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,它们的转化关系如图所示。请回答:
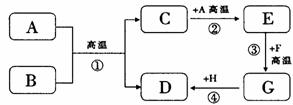
(1)物质B的化学式为 ;
(2)反应①的化学方程式为 ;
写一个能实现反应④的化学方程式 ;
(3) 反应①、③的反应基本类型是否相同? 。
三、实验题(本大题包括3小题,每空1分,共16分)
22.(6分)我省某市中考化学实验操作考试有四个考题:①粗盐提纯②酸的化学性质③二氧化碳的制取、收集和验满④氧气的制取、收集和验满。考试的方法是由考生抽签确定考题,小凯同学抽签后被监考老师引导至准备了下列仪器和药品的实验台前:
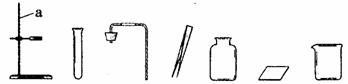

请回答:
(1)指出上图中仪器a的名称: ;
(2)由实验台上提供的仪器和药品,你认为小凯抽到的是第 个考题;
(3)以下是小凯完成该实验主要操作过程的示意图。按评分标准,每项操作正确得1分,
满分5分,实验完毕后小凯得了3分。请找出他失分的操作并说明原因: 、 ;

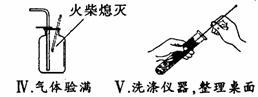
(4)仅用上述仪器(药品另选),也能完成另一种常见气体的实验室制取,化学方程式为:
;若增加 (填一种玻璃仪器名称)还能组装成高锰酸钾制氧气的发生装置。
22.(4分)在整理实验室时,发现有一瓶失落标签的白色粉末,可能是碳酸钠,也可能是氢氧化钙。白色粉末是哪种物质呢?请你提出猜想并设计实验进行探究。
我的猜想
操作步骤
实验现象
结论
23.(6分)小婧同学学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体。但她在空气中点燃镁条时,却发现在生成的白色固体中还夹杂着少量的淡黄色固体。
[提出问题]为什么会生成淡黄色固体?
[查阅资料]小婧查阅资料,记录了下列几种物质的颜色:
物 质
MgO
MgCl2
Mg3N2
Mg(NO3)2
MgCO3
Mg(OH)2
颜 色
白色
白色
淡黄色
白色
白色
白色
其他同学认为不必查阅氯化镁的颜色,理由是 ;
[提出猜想]分析资料,小婧认为淡黄色固体可能是由镁与空气中的 反应生成的;
[实验探究川、婧设计实验证实了自己的猜想,她的方案可能
;
[实验结论]根据小婧的实验结果,写出镁条在空气中燃烧时两个反应的化学方程式:
、
[反思与评价]通过上述实验,你对燃烧有什么新的认识? 。
四、计算题(本大题包括1小题,共6分)
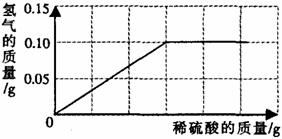
24.(6分)为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品
(1)样品中铜的质量分数;
(2)反应所消耗的硫酸溶液质量;
(3)反应后所得溶液质量。