2007年广东省汕头市初中毕业生学业考试
化学试卷
可能用到的相对原子质量:C-12 H-1 0-16 N-14 Fe-56
第一卷
一、选择题(本大题14小题。l一8题每小题2分,9―14题每小题3分。共34分。在每小题列出的四个选项中。只有一个是正确的。请将答题卡上对应题目所选的选项涂黑)
2.日常生活中的下列变化,只发生了物理变化的是
A.蔬菜腐烂 B.面包发霉 C.灯泡通电后发亮 D.菜刀生锈
3.下图是某葡萄糖酸锌口服液的标签。标签上的含锌6.5mg是指锌

A.单质 B.元素 C.分子 D.原子
4.某同学不小心被黄蜂蛰了(黄蜂毒液呈碱性),为了减轻疼痛可以涂抹
A.浓硫酸 B.食醋(pH=3)
C.食盐水(pH=7) D.苏打或肥皂水(pH=9-10)
5.下列食品中主要是为人体提供维生素的是
A.植物油 B.鸡蛋 C.大米 D.西红柿
6.下图是A、B、C三种物质的溶解度曲线。下列说法不正确的是
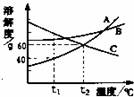
A.A的溶解度大于C的溶解度
B.t
C.t
D.A和B的饱和溶液从t
7.出土的古文物中,金器保存完好,铜器表面有锈迹,而铁器锈迹斑斑。这表明金、铜、铁的金属活动性从强到弱的顺序是
A.金、铜、铁 B.铁、金、铜 C.铁、铜、金 D.铜、金、铁
8.锗酸铋(Bi4Ge3O12)是我国研制的一种闪烁晶体材料。已知锗酸铋中锗(Ge)的化合价为+4价,则锗酸铋中铋(Bi)的化合价为
A.+4
B.+
9.下列做法或认识科学的是
A.厨房煤气泄漏,立即打开排气扇电源 B.煤气中毒应大量喝牛奶
C.用硬水洗衣服比用软水洗效果好 D.垃圾经分类回收处理可转化为资源
10.下表中对部分化学知识的归纳,有错误的一组是
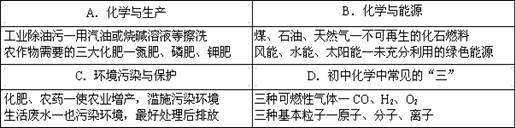
11.“神舟6号”太空舱利用NiFe2O4将航天员呼出的CO2转化为O2,而NiFe2O4的质量和化学性质都不变。则NiFe2O4在该过程中是
A.反应物 B.生成物 C.催化剂 D.消毒剂
12.下列有关灭火方法错误的是
A.家用电器着火时,立即用水扑灭 B.扑灭森林火灾时,设置隔离带
C.炒菜时油锅着火,立即盖上锅盖 D.图书资料着火,用压缩二氧化碳灭火
13.下列实验能利用厨房中的食盐、食醋、纯碱三种物质做成功的是
①检验自来水中是否含有氯离子;②检验鸡蛋壳能否溶于酸;③除去热水瓶中的水垢。
A.①②③ B.②③ C.①③ D.①②
14.下列图像能正确反映所对应叙述关系的是
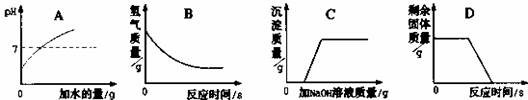
A.向pH=3的溶液中不断加水 B.一定量的稀硫酸与锌粒反应
C.向H2SO4和CuSO4混合液中滴加NaOH溶液 D.煅烧一定质量的石灰石
2007年广东省汕头市初中毕业生学业考试
化学试卷
第二卷
二、填空题(本大题5小题,共24分)请把下列各题的正确答案填写在横线上。
15.(3分)化学符号的序号填入相应的横线上:
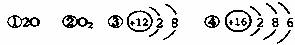
(1)表示两个氧原子的是 ;
(2)表示离子结构示意图的是 。
16.(3分)下列实验操作中,正确的是

17.(6分)人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。请回答:
(1)地壳中含量最多的金属元素是 。
(2)根据下图的应用实例,试说出金属具有的两点物理性质

(3)早在春秋战国时期,我国古代人民已经开始炼铁。
①写出磁铁矿(Fe3O4)与CO反应的化学方程式 。
②钢铁防腐十分重要!请写出一种防止钢铁生锈的方法 。
18.(6分)现有碳酸钠、氯化钠、氢氧化钠、熟石灰、高锰酸钾、氢气、干冰、甲烷、一氧化碳、氧气等物质,请按要求选择:舞台常用 固体的气化,产生烟雾弥漫的感觉;使用燃气热水器时,若通风不畅,容易产生一种有毒的气体是 ;资源广、燃烧值高、无污染的新型能源是 ;沼气的主要成分是 ;生活中可用于调味、防腐的是 ;常用来改良酸性土壤的碱是 。
19.(6分)元素周期表是化学学习和研究的重要工具。下图是元素周期表的一部分。
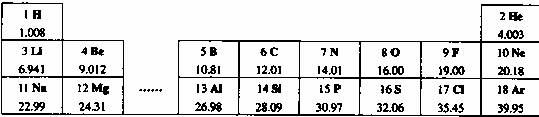
(1)从表中查出硅(Si)元素的相对原子质量为 ;
(2)6~11号元素中属于金属的有 (填元素符号);
(3)表中不同种元素最本质的区别是 (填序号):
A.质子数不同 B.中子数不同 C.相对原子质量不同
(4)年前,科学家宣布已人工合成了第116号元素,则此元素的核电荷数为 ;
(5)仅由l、6、7、8号元素中的三种组成的一种盐的化学式为 。
三、(本大题2小题,共18分)
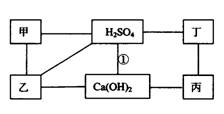 20.(10分)下图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种。
20.(10分)下图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种。
(1)写出乙和丙的化学式:
乙 ,丙 。
(2)写出下列化学方程式:
甲和乙:
丙和丁:
(3)图中反应①属于基本反应类型中的 反应,又称为 反应。

(1)加入活性炭的作用是 ;在乡村没有活性炭,常加入 来净水。
(2)实验室中,静置、吸附、过滤、蒸馏等操作中可以降低水硬度的是 。
(3)若该地区源水中含有较多的MgCl2,请写出在源水处理流程中加入CaO时有关化学方
程式:① ;
② 。
四、(本大题2小题。共27分)
22.(14分)请根据下列装置图回答:
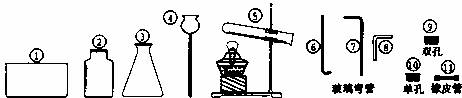
(1)写出下列仪器的名称:① ,④ 。
(2)如果用大理石和稀盐酸制取并收集CO2,应选用上图中的 (填序
号);其化学方程式为 。
(3)若用加热固体KmnO4来制取并用排水法收集一瓶O2,应选用上面图中的
(填序号),其化学方程式为 。
(4)已知乙炔(C2H2)气体可用水和CaC2反应制取。请你完成制取乙炔的化学反应方程式:
CaC2+ === + C2H2↑。
乙炔气中常含酸性杂质气体CO2和H2S,请在右边方框中补画出除杂装置(导气管用直线表示),并标注必要的试剂。
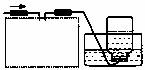
23.(13分)某小组同学对废干电池筒内的黑色固体(内含有MnO2、NH4Cl、ZnCl2等)进行了如下图所示的实验:
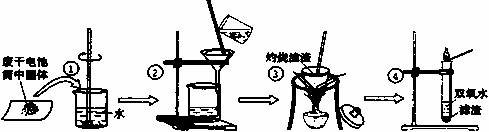
(1)操作②的名称是 ,该操作中玻璃棒的作用是 。
(2)操作③灼烧滤渣黑色固体时,会产生一种使澄清石灰水变浑浊的气体,由此推测滤渣
中除含有MnO2外,还存在的物质是 。
(3)操作④的试管中产生的气体使带火星的木条复燃,则该气体为 。
(4)请你写出用pH试纸检测滤液酸碱性的具体操作:
。
(5)已知在氯化锌溶液中逐滴滴入稀氨水,先生成Zn(OH)2白色沉淀,然后溶解生成可溶
于水的Zn(NH3)4Cl2。同学们对操作②的滤液中的成分进行探究。
验证方法
现象
判断
猜想I:主要成分
为氯化铵
取少量滤液加入
NaOH固体,并加热
未闻到明显的氨的
刺激性气味
猜想Ⅱ:主要成分
为氯化锌
猜想Ⅱ成立
由上述实验得出的结论是:滤液中
五、(本大题2小题。共17分)
24.(7分)蛋白质在人体胃肠内与水反应,最终生成氨基酸被人体吸收。丙氨酸(化学式为
C3H7O2N)就是其中的一种。请回答下列问题:
(1)丙氨酸分子中C、H、O、N各原子个数比为 。
(2)丙氨酸的相对分子质量是 ,氮元素的质量分数为 (计算
结果精确到0.1%)。
(3)合格奶粉每
定某奶粉每
奶粉。
25.(10分)某化学兴趣小组用化学方法测定一种钢样品中铁的含量。同学们称取了
样品,投入装有
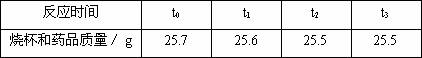
(1)反应中产生氢气 克,这种钢样品中铁的含量是多少?(精确到0.1%)
(2)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;
0.6%~2%为高碳钢。假设残留在烧杯中的黑色固体全部是炭,则这种钢属于 。
(3)有同学提出:灼烧可使钢中的炭变为CO2挥发掉,灼烧后钢样品质量会减轻。可是他
们将一定量的钢样品灼烧后,发现质量反而增加了很多。原因是
。