2007-2008学年度烟台市海阳第一学期期中考试
九年级化学试题
可能用到的相对原子质量:H:l C:12 N:14 O:16 Na:23 Ca:40 C1:35.5 Fe:56 Cu:64 Zn:65 Hg:
一、选择题(本题包括10个小题,每小题1分,共10分、每小题只有一个选项符合题意。)
1.某学校组织学生进行水资源情况调查,调查结果报告中的下述观点错误的是
A.地球表面约71%被水覆盖着,可以利用的淡水资源十分丰富
B.水的污染加重了淡水危机
C.可以考虑海水淡化解决淡水危机,蒸馏法是海水淡化的方法之一
D.节约用水是每个公民应尽的义务
2.常发生将工业用盐当作食盐而引起中毒现象,该工业用盐对人有致癌作用,这种盐的化学式是
A.MgCl2 B.KCl C.NaNO2 D.MgSO4
3.下列说法正确的是
A.从海水中提取镁的过程中,涉及的反应类型有分解、化合和置换反应
B.“可燃冰”是在低温、高压条件下形成的冰状固体,是一种化合物
C.蒸馏法和干馏一样,都能将海水淡化
D.“可燃冰”燃烧后不产生任何残渣或废弃物
4.金属和金属材料的性质在很大程度上决定了它们的用途,下列说法中不正确的是
A.不锈钢抗腐蚀性好,常用制造医疗器械
B.铝合金轻而坚韧,可作汽车、飞机和火箭的材料
C.铅锑合金的熔点较低,电阻率大,常用于制成发热体
D.用铁锅炒菜可使食物中增加微量元素
5.蒸馒头时在发酵的面团里加入一些纯碱,其作用是
A.使馒头变白 B.既除去生成的酸,又使馒头松软
C.加快面团的发酵速率 D.产生的CO2气体使馒头质量增大
6.下列关于金属说法中正确的是
A.各种金属在常温时都不能与氧气反应
B.各种金属在高温时都能与氧气反应
C.根据金属与氧气反应的难易程度可以初步比较一些金属的活动顺序
D.各种金属都能与盐酸反应放出氢气
7.厨房是同学们的家庭实验室,同学们可以利用家庭生活用品来做化学实验对化学现象进行探究,下列实验不能利用厨房中的物品来完成的是
A.探究铁制品在什么条件下生锈 B.制取无壳鸡蛋
C.鉴别食盐和纯碱
D.检验自来水中是否含有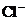
8.某工厂排放的酸性废水中含有较多CuSO4,这种废水对农作物和人畜有害。为了降低废水的酸性并且回收铜,通常需要在此废水中加入适量的
A.熟石灰 B.铁和生石灰 C.铁和石灰石 D.氢氧化钠
9.t℃时,欲使一接近饱和的溶液变成饱和溶液,分别采取下列措施:①降低温度 ②升高温度 ③加水 ④加入足量的溶质,其中能达到目的的是
A.只有① B.只有④ C.①③ D.②④
10.有X、Y、Z三种金属,把Y投入到X(NO3)2溶液中,Y表面有X析出,得到Y(NO3)2溶液的质量比X(NO3)2溶液的质量大;把X投入到Z(NO3)2溶液中,Z析出后,溶液质量减小。下列判断错误的是
A.元素的相对原子质量可能是:Z>Y>X
B.X、Y、Z可能依次是:Hg、Zn、Cu
C.金属的活动顺序是:Y>X>Z
D.X、Y、Z可能依次是:Cu、Zn、Hg
二、选择题(本题包括l0个小题,每小题2分,共20分。每小题有l―2选项符合题意,少选、错选均不得分。)
11.生产、生活实际中的下列做法,不科学的是
A.为防止自行车生锈,经常用湿抹布擦拭
B.为提高粮食产量,大量使用化肥
C.海底矿物(如可燃冰、锰结核等)虽储量丰富,也应科学规划、合理开采
D.新装修的房屋,经充分通风后再入住
12.下列有关金属和金属材料的说法不正确的是
A.铁有良好的导热性,常用来做炊具
B.铜的化学性质不活泼,在潮湿的空气中不会锈蚀
C.废旧电池中汞的回收可减少对环境的污染
D.铝表面易形成致密的氧化膜可阻止铝进一步被氧化
13.2005年5月,益阳市资阴区的虎形山出土了一批战国青铜器,其实我国早在商代就能制造出精美的青铜器,到了战国时期已经能冶铁和炼钢。人类开发利用下列金属单质的时间与金属活动强弱有着上述某种内在的联系。由此推断,人类开发利用下列金属的时间由先到后的顺序是
A.Cu、Fe、Al、Zn B.Cu、Zn、Fe、Al
C.Cu、Fe、Zn、Al D.Al、Zn、Fe、Cu
14.甲、乙、丙、丁分别是NaCl、Ba(NO3)2、Na2CO3、HCl 四种溶液。已知甲和丙可以反应,甲和丁也可以反应,则下列说法正确的是
A.丁不可能是Ba(NO3)2 B.甲一定是Na2CO3
C.丙一定是HCI D.甲一定是NaCl
15.海底蕴藏着大量天然气的水合物,俗称“可燃冰”。“可燃冰”是一种晶体,晶体中平 均每46个水分子构建8个笼,每个笼可容纳1个甲烷分子或游离的水分子。若晶体中每8个笼有6个容纳了甲烷分子,另外2个被游离的水分子填充,则“可燃冰”的平均组成可表示为
A.3CH4?H2O B.CH4?3H2O C.CH4?6H2O D.CH4?8H2O
16.下列除杂质的方法中(括号内的物质为杂质)错误的是
A.CaCl2溶液(HCl);加入过量的CaCO3,过滤
B.NaOH溶液(Ca(OH)2);加入过量的Na2CO3,过滤
C.FeCl2溶液(CuCl2);加过量的Fe粉,过滤
D.CH4(H2O);通过盛有浓H2SO4的洗气瓶
17.如下图所示,试管中盛有某种液体,将气球中的某种固体小心地倒入试管中,不能观察到气球逐渐变大的一组物质是

A.氯化钠和水 B.铁粉和稀硫酸
C.生石灰和水 D.碳酸钠和稀盐酸
18.在
A.溶液的质量不变 B.溶质的质量减少
C.溶质的质量分数减少 D.溶质的质量分数变大
19.将质量相等的,A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的盐酸中,反应生成H2质量与反应时间关系如图所示。根据图中所提供的信息得出的结论正确的是(已知A、B、C在生成物中均显+2价)
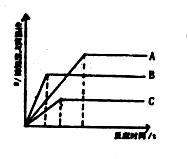
A.放出H2的质量是A>B>C B.金属的活动性顺序是A>B>C
C.反应速度最快的是A D.相对原子质量是C>B>A
20.利用铝热反应 中所产生的热量,可在野外快速将铁轨上的 裂缝修补好。关于此反应的说法,错误的是
中所产生的热量,可在野外快速将铁轨上的 裂缝修补好。关于此反应的说法,错误的是
A.铝是还原剂,发生氧化反应 B.氧化铁具有氧化性,发生还原反应
C.铝是还原剂,发生还原反应 D.氧化铁是氧化剂,发生氧化反应
三、填空题(本题包括5个小题,共26分)
21.在硫酸铜、碳酸氢铵、大理石、活性炭四种物质中,可用作建筑材料的是______;可用于制波尔多液的是_______;可用作化肥的是_______;可用作冰箱除臭剂的是______。
22.松花蛋又名皮蛋,微山湖出产的松花蛋因色味俱佳享誉齐鲁。松花蛋的制作工艺一般是将灰料[主要成分是生石灰(CaO)、草木灰(成分中含K2CO3)、纯碱(Na2CO3)、食盐(NaCl)等]调成糊状,涂于新鲜鸭蛋的表面,密封保存一段时间后,即可得到松花蛋,请根据以上信息回答:
(1)松花蛋腌制过程中发生的化学反应有________个
(2)剥除松花蛋外边的灰料后,常常发现蛋壳上有一些坚硬的白色斑点,这斑点的主要成分是________。
(3)食用劣质松花蛋时往往有麻涩感,可能的原因是________________________。
23.(1)请按(2)小题要求在下表中各填入一种相应类别物质的化学式。
类别
单质
酸
碱
盐
化学式
(2)用上表的四种具体物质,各写出一个符合下列要求的化学方程式:
①置换反应________________________________________;
②复分解反应______________________________________。
24.由海水蒸发制得的食盐中,常含有Na2SO4、CaCl2、MgCl2等杂质,这些杂质对后续生产有害需要除去。将海水晒盐得到的食盐溶于水:
(1)Na2SO4、CaCl2、MgCl2在溶液中能形Na+、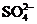 、Ca2+、
、Ca2+、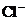 、Mg2+五种离子,要除去Ca2+一般使用________溶液;要除去
、Mg2+五种离子,要除去Ca2+一般使用________溶液;要除去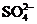 一般使用________溶液;要除去Mg2+一般可使用________溶液。
一般使用________溶液;要除去Mg2+一般可使用________溶液。
(2)在工业除杂质中,为了将杂质除净往往加入稍过量的试剂,请将(1)中所用试剂排序加入________________________;然后进行一步操作________________,这样又会在溶液中带进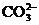 、
、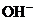 ,要同时除去这两种杂质离子,用最简单的方法是加入适量的________________并用________________测定溶液的酸碱度。
,要同时除去这两种杂质离子,用最简单的方法是加入适量的________________并用________________测定溶液的酸碱度。
25.以下是同学们在学习溶液知识时实验报告中的部分内容,分析后请回答:
试管编号
加入液体
加入物质
现象
1
10ml水
少量食盐
不溶
2
10ml乙醇
少量食盐
溶解
3
10ml水
几小颗粒碘
不溶
4
10ml乙醇
几小颗粒碘
溶解
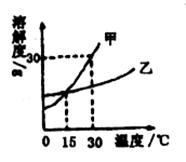
(1)在同一条件下,物质的溶解能力与________和________有关。
(2)除(1)中因素外,你认为固体物质的溶解能力还与外界条件________有关。如果外界条件和溶剂的种类确定,要比较硝酸钾和氯化钠的溶解能力,实验中需要控制的因素是________________________。
(3)根据上图甲、乙两种固体物质的溶解度曲线,你能获得的信息是(答出两条即可)________________________________;________________________________。
四、简答题(本小题包括2个小题,共15分)
26.某活动小组从工厂收集到了一些含有AgNO3的废液以及铁屑和锌屑的混合物。在回收银时他们将一定量的上述金属混合物加入到AgNO3的溶液中,充分反应后过滤,得到固体和浅绿色滤液(所含其它杂质不考虑)。为了探究滤液中溶质的组成,他们做出下列猜想:
①溶液为Fe(NO3)2; ②溶液为Fe(NO3)2和AgNO3;
③溶液为Zn(NO3)2和Fe(NO3)2; ④溶液为Zn(NO3)2、Fe(NO3)2和AgNO3
(1)上述猜想中,错误的是(填序号)________,其原因是________________________。
(2)有的同学认为滤液中溶质只有Zn(NO3)2,你认为是否正确?________________其原因是________________________________。
(3)某同学将一铜片放入滤液中,目的是________________________________。一段时间后铜片没有变化,上述正确猜想中可排除的是(填序号)_______________。
27.我国化学家
(1)用上述方法进行生产时所用的起始原料________(写出它们的化学式,下同。)
(2)最终产品是________________。
(3)①有关反应的化学方程式是______________________;______________________;________________________。
②在第二步反应中加入的是细小的食盐粉末,食盐磨细的目的是_______________。
(4)该生产过程中没有涉及的基本反应类型是________________。
(5)有人认为“候氏制碱法”的优点有四:
A.生产过程中部分产品可选为起始原料使用
B.副产品是一种可利用的氮肥
C.反应不需要加热
D.副产品不会造成环境污染
你认为其中正确的是________(用序号回答)。
五、实验与探究(本题包括2个小题,共22分)
28.小林同学发现铜制的眼镜框表面出现了绿色物质,通过化学学习知道该物质为铜锈,俗称铜绿,主要成分是Cu2(OH)2CO3。
【提出问题】:铜是在什么条件下锈蚀的?
【猜 想】:根据铜锈的化学式,猜想铜生锈可能是铜与水、________、 ________共同作用的结果。
【设计与实验】:借鉴“铁钉锈蚀条件的探究”实验,小林设计了“铜片锈蚀条件的探究”实验.如图所示:
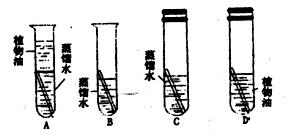
(1)实验较长时间后,发现________试管中的光亮铜片最先生锈(填序号)
(2)从优化实验的角度考虑,A实验他只考虑了水这个单一条件,C试管中除光亮的铜片、蒸馏水外,还有另外一种物质为________;
(3)B试管中除光亮的铜片外,还有另外两种物质________________;从B 试管的试验中,获得的结论是________________________________________;反应的化学方程式是____________________________________________________________。
【评价与改进】:我认为小林设计的“铜片锈蚀条件的探究”实验还不够完善,要得出正确结论,还要补充一个实验是________________________。
【反思与小结】通过铜片锈蚀条件的探究实验,我获得的启示是____________________。
写出一种防止铁、铜等金属制品的生锈的具体办法_______________________________。
请你提出一条延长食品保质期的建议__________________________________________。
29.甲同学在某食品包装袋内,发现有一个装有白色颗粒固体A的小纸袋,上面写着“生石灰干燥剂,请勿食用”。甲同学随手将小纸袋拿出来放到空气中,经过一段时间后,发现纸袋内的白色颗粒粘在一起成为块状固体B。请你与甲同学一起对块状固体B的成分进行探究。
(1)猜想一:块状固体B中除氧化钙外还可能有__________、_______。写出白色颗粒固体A在空气中转化为块状固体B的化学反应方程式________________________、________________________________。
(2)猜想二:块状固体溶于水可能有________现象(填“放热”或“吸热”)。请你设计实验验证你这一猜想_____________________________________________。
(3)取适量固体B加入盛有一定量水韵试管中,振荡、静置、过滤,得到白色固体C,就白色固体C的成分,甲、乙两同学进行讨论一起猜想。
甲:白色固体C可能是Ca(OH)2; 乙:白色固体C可能是CaCO3;
你认为白色固体C还可能是________________________。
设计实验证明你的猜想(写出有关的实验步骤、现象和结论)
实验步骤
现象及结论
六、计算题(本题包括1个小题,共7分)
钙(以Ca计)(0.5~1.3)%
碘(以I计)(20~500)mg/kg
(1)包装标签上钙含量指________。
(填“单质钙”、“碳酸钙”、“钙元素”中的一种)
(2)为了检验此食盐中是否含有碳酸钙,在家庭厨房里可选用的物质是________。
(3)为了测定此盐中钙元素含量,取