2006年大连市初中毕业升学统一考试化学试卷
相对原子质量:
H-
一、选择题(本题共18小题,每小题1分,共18分)
1.下列变化中,属于化学变化的是( )
A.冰雪融化 B.矿石粉碎 C.蜡烛燃烧 D.干冰升华
2.空气中含量较多且化学性质比较活泼的气体是( )
A.氮气 B.氧气 C.二氧化碳 D.水蒸气
3.下列四种元素中,属于非金属元素的是( )
A.C2 B.N
4.我们身边常见的下列物质中,属于氧化物的是( )
A.氧气 B.水 C.空气 D.食盐
5.亚硫酸钠(Na2SO3)是一种重要的化工原料,大量用于染料工业。亚硫酸钠中硫元素的化合价是( )
A.-2 B.+2 C.+4 D.+6
6.实验室里用氯化钾固体配制一定溶质量分数的氯化钾溶液时,下列仪器中,不必用到的是( )
A.托盘天平 B.烧杯 C.量筒 D.漏斗
7.随着社会的发展,环境问题已经引起人们关注。从环保的角度看,下列燃料中最理想的是( )
A.沼气 B.酒精 C.氢气 D.煤
8.下列材料中,属于有机合成材料是( )
A.尼龙 B.棉花 C.羊绒 D.蚕丝
9.人体中化学元素含量的多少,会直接影响人体健康。下列人体所缺元素与健康关系错误的是( )
A.缺铁会引起贪血 B.缺碘会引起龋齿
C.缺钙会引起老年人骨质疏松 D.缺锌会引起食欲不振、发育不良
10.生活中的下列物质放入水中,能形成溶液的是( )
A.蔗糖 B.纯水冰块 C.豆油 D.面粉
11.下列物质的化学式,书写正确的是( )
A.氧化锌-ZnO2 B.氯化镁-MgCl C.氢氧化钾-KOH D.硫酸铝-AlSO4
12.下列关于水的叙述中,错误的是( )
A.自然界中水的pH均为7 B.工农业生产需要大量的淡水
C.地球上总储水量很多,但淡水量很少 D.水能以固态、液态、气态三种状态存在
13.下列实验操作中,正确的是( )
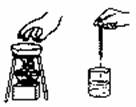
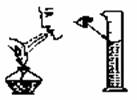
A.熄灭酒精灯 B.读取液体体积 C.移动加热的蒸发皿 D.滴加液体
14.小华到医院检查完身体后,医生建议他多吃水果。则小华需要补充的营养成分是( )
A.糖类 B.油脂 C.蛋白质 D.维生素
15.下列关于分子、原子的叙述中,错误的是( )
A.分子是由原子结合而的 B.分子在化学变化中不可再分
C.原子失去电子形成阳离子 D.原子是由原子核和核外电子构成的
16.汽车尾气含有的下列气体,在空气中易形成酸雨的是( )
A.一氧化碳 B.二氧化碳 C.二氮化氮 D.碳氢化合物
17.下列物质露置在空气中,能与氧气、水蒸气同时发生反应的是( )
A.铁粉 B.生石灰 C.浓硫酸 D.氢氧化钠固体
18.二氧化氯(CO2)已被世界卫生组织确认为一种安全、高效、广谱的强力杀菌剂,二氧化氯的制取可通过下列反应完成:
2N2ClO2+4HCl(浓) Cl2↑+2ClO2↑+2NaCl+2X。则X的化学式为( )
Cl2↑+2ClO2↑+2NaCl+2X。则X的化学式为( )
A.O2 B.H2O C.H2 D.N2ClO
二、填空题(本题共9小题,每空1分,共27分)
19.世界上的物质都是由微粒构成的。仿照示例填表(所填物质不能与示例重复):
物质名称
示例:水
铁
氯化钠
构成物质的微粒
分子
分子
 20.化学与生活密切相关,用化学知识能解决很多生活中的问题。写出用化学方法鉴别下列两组物质所需的药品:软水与硬水( );硫酸铵与硝酸钾(
)。
20.化学与生活密切相关,用化学知识能解决很多生活中的问题。写出用化学方法鉴别下列两组物质所需的药品:软水与硬水( );硫酸铵与硝酸钾(
)。
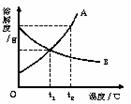
21.A、B两种物质的溶解度曲线如图所示。
(1)A、B两种物质的溶解度相等时的温度为( )°C。
(2)B物质在t2°C时的溶解度(填“>”“=”或“<”=( )在t1°C时的溶解度。
(3)某温度下,当A、B两种物质形成的溶液均接近饱和状态时,通过增加溶质、蒸发溶剂或降低温度的方法,都可以达到饱和状态的是( )物质形成的溶液。
22.反应条件在化学反应中起着重要的作用,反应物相同但条件不同,生成物可能不同。
(1)将二氧化碳通入水中,生成( ),为证明二氧化碳与水发生了反应,应加入的试剂是( )。
(2)绿色植物通过光合作用,将二氧化碳和水合成为( ),同时生成的气体是( )。
23.炼油厂常用氢氧化钠溶液洗涤石油产品中的残余硫酸,以达到精炼石油的目的。写出该反应的化学方程式:( ),该化学反应的基本类型是( )反应。
24.在化学学习中,我们会遇到一些因化学性质相似而某方面用途相同的物质。根据此结论将适当的物质名称填在空白处。
(1)稀有气体和( )都可以作为焊接金属的保护气。
(2)稀盐酸和( )都可以用于除去铁制品表面的铁锈。
25.某溶液的pH为13,该溶液能使无色酚酞试液变成( )色。加水稀释后溶液的pH将(填“变大”、“变小”、或“不变”)( ),其原因是( )。
26.煤、石油、天然气被称为化石燃料,是不可再生的能源。
(1)天然气的主要成分是( ),写出该主要成分在空气中充分燃烧的化学方程式;( )。
(2)分别写出一种煤、石油加工后可以用作燃作的产品:煤( );石油( )。
27.按要求写出下列反应的化学方程式,并说明该反应在实际中的一种应用。
化学方程式
实验中的就用
有红磷参加的化合反应
有氧化钙生成的分解反应
三、回答下列问题(本题共6小题,共22分)
28.(4分)人的一生大部分时间在室内度过,相对于外界环境污染,室内空气污染对身体健康的影响更为显著。
(1)新装修的房屋,室内空气中通常含有较多的甲醛(HCHO)、苯(C6H6)、甲醇(CH3OH)等有毒物质。这三种物质都属于(填“无机物”或“有机物”)( )。在搬入新装修的房屋之前,应该采取的措施是(写出两点即可)( );( )。
(2)写出引起室内环境污染的另一种情况:( )
29.(3分)某干洗剂的主要成分是四氯乙烯(C2Cl4),它是一种易挥发、可至癌的有毒物质。
(1)干洗后的衣服刚取回时,往往需要挂在室外通风处一段时间。请用微粒的观点解释这样做的原因。
(2)有些干洗店用装有活性炭的新款干洗机取代旧款的干洗机,可将有毒物质大约降至原来的1/30。这一做法利用了活性炭的( )性。
30.(4分)铁是工农业生产和人们生活离不开的重要金属材料之一,人类每年要从自然界获取大量的铁矿资源。
(1)写出工业上用一氧化碳和赤铁矿(主要成分Fe2O3)反应冶炼铁的化学方程式。
(2)通过上述方法得到的是生铁,请写出另一种铁合金的名称( )。
(3)铁矿石的种类很多,例如磁铁矿(主要成分Fe3O4)、黄铁矿(主要成分FeS2)及上述的赤铁矿等。请分析用于炼铁的优质铁矿石应该具有哪些主要特点(写出两点即可)。
31.(3分)在一次失火后的现场处理中,消防人员发现某种易燃物质保存了一种阻燃剂。当火情出现时,这种阻燃剂发生化学反应,吸收热量,生成的产物覆盖在易燃物质表面。这些都起到了阻止该物质燃烧的作用。
(1)从燃烧条件分析,这种易燃物质没有燃烧的原因。
(2)推测这种阻燃剂发生化学反应后,生成的产物应具有的化学性质(写出一点即可):( )。
8.92
铝
61
2.70
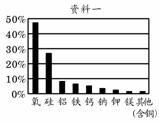 资料二
资料二
通过对上述资料的分析,说明高压电缆用铝制而不用铜制的原因。
(2)铝在常温下就能与氧气反应,但铝制的高压电缆却很耐腐蚀。说明其原因。
33.(4分)20世纪80年代,有人曾制造了一个“水变油”的骗局:
(1)骗局制造者称:只要在一盆清水中加入一些“神秘”的液体作催化剂,清水就可以变成能燃烧的汽油。请用学过的化学知识解释:水不能变成汽油。
(2)骗局制造者的手段是在水中加入一定量的汽油,再加入辅料黑色肥皂,使原本不相溶的水和汽油混合在一起,好像是变成了黑糊糊的油,并称之为“水基燃料”。这里黑色肥皂起( )作用,而使细小油滴均匀悬浮在水中。
(3)在进行“水基燃料”燃烧演示时,由于燃烧后没有水留下,所以许多人认为其中的水已全部转变为能燃烧的汽油,从而受到蒙蔽。请解释为什么“水基燃料”燃烧后没有水留下。
四、实验题(本题共4小题,共20分)
34.(6分)根据实验室时制取氧气的装置(如图所示),回答下列问题:
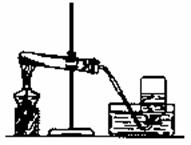
(1)写出大试管中发生反应的化学方程式:( )。
(2)该装置中收集氧气的方法是( ),说明氧气具有( )的性质。
(3)除该装置中收集氧气的方法外,还可以用( )法收集,用此方法收集氧气,检验是否收集满的操作是( )。
(4)在实验室里,还可以利用过氧化氢浴液和二氧化锰制取氧气,写出该反应的化学方程式:( )。
35.(4分)根据下列实验报告回答问题:
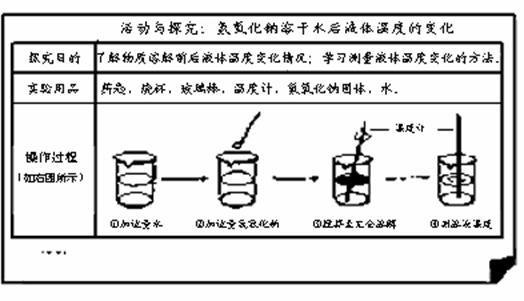
上图中文字信息如下:
活动与探究:氢氧化钠溶于水后液体温度的变化
探究的目的:了解物质溶解前后液体温度变化情况:学习测量液体温度变化的方法。
实验用品:药匙、烧杯、玻璃棒、温度计、氢氧化钠固体、水。
操作过程(如图所示)
①加适量水 ②加适量氢氧化钠 ③搅拌至完全溶解 ④测溶液温度
(1)使用氢氧化钠固体时必须注意安全,其原因是( )。
(2)图示③中的操作存在一处错误,应改正为( )。
(3)图示③中错误操作改正后,上述实验能否测得氢氧化钠固全溶解的前后,液体温度的变化范围?为什么?
36.(4分)某化学探究小组为了验证铁、铜、锌、银的金属活动性顺序,设计了如下实验方案:
①将铁片加入到稀盐酸中;②将铜片加入到销酸银溶液中;③将锌片加入到稀盐酸中;④将金属片X加入到Y中。
(该方案中所有金属均已打磨,有形状、大小以及稀盐酸的溶质质量分数均相同)
试回答下列问题:
(1)写出①中反应的化学方程式:( )。
(2)通过上述实验,可以判断锌的金属活动性比铁强,依据的现象是( )。
(3)要得出这四种金属的活动必顺序,如果④中Y表示硫酸铜溶液,则X表示的一种金属是( );如果X表示铜,则Y表示的一种溶液是( )。
37.(6分)某同学在实验结束进行废液处理时,将碳酸钠溶液、稀盐酸倒入到指定的洁净容器中,看到有气泡产生,待不再产生气泡时,又倒入了氢氧化钙溶液,发现该容器中有白色沉淀产生,这一现象引起了他的注意。为了解以上三种物质之间的反应情况,他决定从反应后溶解中的溶质组成人手进行探究。
(1)他对反应后溶液中的溶质组成作出了两种猜想(猜想①和猜想②)。请你再补充一种猜想(猜想③)。
猜想①:溶质为氯化钠、氢氧化钠;
猜想②:溶质为氯化钠、氢氧化钠、氢氧化钙;
猜想③:溶质为( )。
(2)比较三种猜想,说明该同学作出猜想①的理由。
(3)比较三种猜想的异同,如果猜想②成立,设计实验,用两种方法加以证明。按相关要求填写下表。
实验操作
实验现象
方法一
方法二
五、计算题(本题共2小题,共13分)
38.(6分)食醋中含有3%~5%的醋酸,醋酸的化学式为CH3COOH0试计算:
(1)一个醋酸分子中共含有( )个原子。
(2)醋酸的相对分子质量为( )。
(3)醋酸中碳、氢、氧三种元素的质量比(化成最简整数比)为( )。
39.(7分)现有10g某种钾肥样品,其成分为碳酸钾、硫酸钾及少量不含钾元素的质量分数,过程如下:
[反应原理]
K2CO3+H2SO4=K2SO4+H2O+CO2↑
[方法及数据]①将10g该钾肥样品溶于水,过滤出难溶性杂质,得到滤液。
②将溶质质量分数为20%的硫酸溶液逐滴加入到滤液中,至恰好完全反应,测得消耗硫酸溶液的质量为24.5g。
③将反应后的溶液蒸干,称量所得白色固体质量为11.2g。
[数据处理]根据实验数据计算(整个过程的损失忽略不计;计算结果精确到0.1):
(1)样品中碳酸钾的质量;
(2) 样品中钾元素的质量分数。