2004年山东省聊城市中等学校招生考试
第一卷
一、选择题(本题包括10小题,每小题2分,共20分。每小题只有一个选项符合题意)
1. 下列说法错误的是( )
A. 洁净的空气是混合物 B. 硝酸既是化合物又是氧化物
C. 含氢的化合物不一定是酸 D. 冰水混合得到的是纯净物
2. 有一种能源,被称为“21世纪的理想能源”,它燃烧的产物只有一种,且该产物通常状况下呈液态,它不会产生烟雾或酸雨等。这种能源是( )
A. 太阳能 B. 氢能 C. 电能 D. 地热能
3. 下列说法不正确的是( )
A. 物质在微观上都是由粒子构成的 B. 物质的结构决定物质的化学性质
C. 化学变化中元素的种类发生了变化 D. 化学反应都是有条件的
4. 在空气中点燃镁条,镁与氧气反应的同时,还可以与空气中的氮气、二氧化碳反应。镁与二氧化碳反应的化学方程式如下:
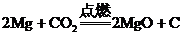
该反应属于( )
A. 分解反应 B. 化合反应 C. 置换反应 D. 复分解反应
5. 抗氧化剂能吸收氧气,降低食品内部及周围的含氧量,阻止氧气和食品发生氧化反应,从而延长食品的保质期。小明发现新买来的高级月饼的包装盒内有一个印有“抗氧化剂”的小包,内盛灰黑色粉末,该灰黑色粉末可能是( )
A. 铁粉 B. 氢氧化钠 C. 二氧化锰 D. 生石灰
6. 下列有关实验操作的叙述中正确的是( )
A. 将pH试纸浸入试剂瓶中,测定溶液的pH
B. 用排水法收集气体时,导管口刚出现气泡便立即开始收集
C. 向燃着的酒精灯内添加酒精
D. 点燃可燃性气体前,要检验气体的纯度
7. 2004年奥运圣火传递于6月9日抵达北京。火炬用的可燃物是丁烷(用X表示),它燃烧时火苗明亮,燃烧的化学方程式可表示为:
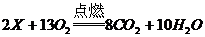
则丁烷的化学式为( )
A. 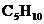 B.
B. 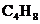 C.
C. 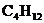 D.
D.
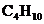
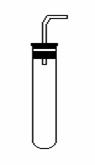
8. 下图为实验室常用的实验装置。利用该装置不能进行的实验是( )
A. 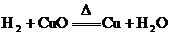
B. 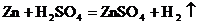
C. 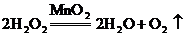
D. 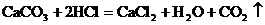
9. 下列各组中所选鉴别试剂正确的是( )
A. Zn和Fe用MgCl2溶液鉴别
B. HCl溶液和H2SO4溶液用AgNO3溶液鉴别
C. KOH溶液和Ba(OH)2溶液用Na2SO4溶液鉴别
D. K2SO4溶液和BaCl2溶液用NaOH溶液鉴别
10. 下列四个图像分别表示4种操作过程(图1)。其中正确的是( )
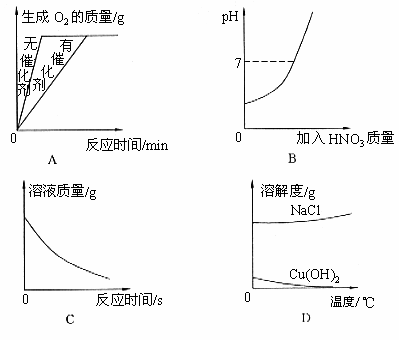
图1
A. 加热氯酸钾制取氧气
B. 向pH=12的NaOH溶液中逐滴加入稀硝酸
C. 向硫酸溶液中加入镁粉
D. 测定不同温度下NaCl和Ca(OH)2的溶解度
第二卷
二、填空题(本题包括4小题,共14分)
11. (2分)东昌湖是聊城旅游的一大亮点,荡漾在风光秀美的湖面上令你心旷神怡。
(1)水的净化有多种方式,市场上出售的一种活性炭净水器可以除去水中的难溶性杂质,同时利用活性炭的___________作用除去水中的异味。
(2)有些游人随意将用过的废电池投入湖中。研究表明,一节含汞、镉、铅等金属的电池可使600t水无法饮用,相当于一个人一生的饮水量。为了避免湖水受到污染,防止废旧电池造成的危害,作为一名学生,你应该怎样做_________________________________(写出一条)。
12. (4分)下表是核电荷数3~18的元素原子的核外电子排布示意图:
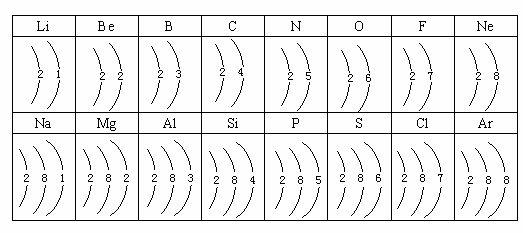
(1)上表中每一横行的元素核外电子排布的特点是______________________,每一纵行的元素核外电子排布的特点是____________________________________________。
(2)若将氢、氦元素也排入上表,已知氦元素的核外电子排布为___________,可得到以下两种形式:
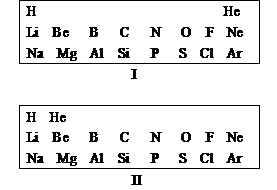
你同意____________种排列方式,针对氦元素说明你选择的理由是__________________________
____________________________________________________________________________________________________________________________________。
13. (4分)溶液与人类的生活息息相关,溶液的配制是日常生活和化学实验的常见操作。下表是硫酸溶液和氨水的密度与其溶质质量分数对照表(20℃)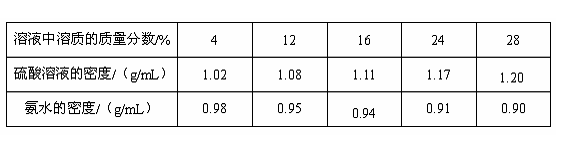 请仔细分析上表后回答:
请仔细分析上表后回答:
(1)20℃时,随着溶液中溶质质量分数的逐渐增大,硫酸溶液的密度逐渐____________(填“增大”、“减小”或“不变”);氨水的密度逐渐____________(填“增大”、“减小”或“不变”)。
(2)取16%的硫酸溶液100g配制成8%的溶液,则向100g 16%的硫酸溶液中,加水的质量应
____________(填“大于”、“小于”或“等于”)100g。
(3)向100g 24%的氨水中加入100g水,摇匀所得溶液的体积是____________mL(保留到0.1)。
14. (4分)在实验室用氧化铜、硫酸和氢氧化钠溶液制备氢氧化铜。
(1)小芳取少量氧化铜和一定量溶质质量分数较大的硫酸,略微加热后得到蓝色溶液;接着滴入几滴氢氧化钠溶液,结果没有氢氧化铜蓝色沉淀生成。请你帮助小芳分析未得到蓝色沉淀的原因____________________________________,并写出滴入氢氧化钠溶液后发生反应的化学方程式____________________________________。
(2)小刚取少量氧化铜和一定量的稀硫酸,经过较长时间加热,氧化铜全部溶解后,立即加入氢氧化钠溶液,结果也没有得到蓝色沉淀,试管中却意外出现了黑色固体。请写出该黑色固体的化学式
_______________________________________________________。
三、实验题(本题包括2小题,共8分)
15. (2分)用实验证明一包黑色粉末是由氧化铁和炭粉混合而成的。甲、乙两同学设计的实验方案如下:
甲:黑色粉末
乙:黑色粉末
你认为____________同学的实验方案更好,理由是_______________________________________
__________________________________________________。
16. (6分)某学生用如图2所示的装置进行实验,点燃酒精灯后,观察到小试管内棉花球上沾有的无水硫酸铜粉末变蓝,烧杯A中溶液仍保持澄清,烧杯B中溶液变浑浊。试回答下列问题:
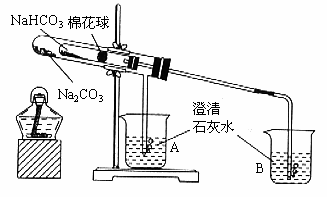
图2
(1)应该用酒精灯火焰的____________部分给试管加热。
(2)若试管口向上倾斜,可能出现的后果是____________________________________________
______________________________________。
(3)经检验,完全反应后,小试管内剩余的物质为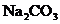 ,试写出小试管中发生反应的化学方程式____________________________________________________________。
,试写出小试管中发生反应的化学方程式____________________________________________________________。
(4)该实验结束时,在操作上需要特别注意的问题是_______________________________________
____________________________________。
(5)通过该实验可以得出的结论是____________________________________。
四、计算题(本题包括2小题,共8分)
17. (2分)劣质奶粉因蛋白质含量偏低而严重影响儿童的发育成长。蛋白质是生命的物质基础,在人体内降解为氨基酸。儿童生长必需的10种氨基酸中有一种叫精氨酸,其化学式为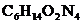 。请计算:
。请计算:
(1)精氨酸的相对分子质量为____________;
(2)精氨酸中碳、氢、氧、氮元素的质量比为____________。
18. (6分)一氧化碳能在高温下还原铁矿石中的氧化铁。现用200t含氧化铁80%的铁矿石炼铁,可炼出含铁95%的生铁多少吨?
(1)请你根据化学方程式进行计算。
(2)本题还有其他解法吗?若有,只要求说明依据并列出算式。若没有,可不回答此问。