2006年中考化学模拟考试一
第Ⅰ卷(共30分)
可能用到的相对原子质量:H-1 C-12 O?16 Na?23 S?32 N?14
一、(本题包括15小题,每题2分。每小题只有一个选项符合题意)
2.下列物质属于纯净物的是 ( )
A.波尔多液 B.葡萄糖 C.钢 D.石油
3.目前我国电力供应仍然紧缺,需开发各种资源发展电力工业。以下利用化学能发电的是
A.水力发电 B.火力发电 C.风力发电 D.核能发电
4.复合材料集中了合成材料的优点,具有综合性能更优异的特点。下列材料中不属于复合材料的是 ( )
A.机动车轮胎 B.玻璃钢 C.有机玻璃 D.钢筋混凝土
5.科学家计划用质子数为20的钙离子,轰击核电荷数为98的锎元素靶,使两元素的原子核合并在一起,合成核电荷数为118的新元素。对此理解正确的是 ( )
A.新元素的原子核外电子数为116
B.新元素的原子序数为118
C.新元素的相对原子质量为118
D.变化过程中元素种类没有发生改变
6.近年用红外激光技术研究液氢,发现液氢中含有H3+。则H3+属于 ( )
A.单质 B.分子 C.原子 D.离子
7.以下实验操作错误的是 ( )

A. B. C. D.
8.小玲同学对所学部分化学知识归纳如下,其中有错误的一组是 ( )

9.甲、乙、丙三种物质在不同温度下的溶解度见下表:

下列有关说法正确的是 ( )
A.甲、乙、丙三种物质的溶解度大小顺序是甲>乙>丙
B.30℃时,三种物质的饱和溶液溶质质量分数甲<乙<丙
C.降低温度可使丙的饱和溶液变为不饱和溶液
D.使甲物质从一定温度下的饱和溶液中析出,一般采用蒸发溶剂的方法
10.如下图是某广口瓶的标签,已经部分被污损和腐蚀。小明想探究其成分,他取一支洁净的试管,加入少量广口瓶中的固体,滴入少量盐酸,有无色无味气泡产生。该气体能使澄清石灰水变浑浊,则该固体 ( )

A.一定是Na2CO3 B.一定是NaHCO3
C.可能是Na2CO3,也可能是NaHCO3 D.一定是Na2CO3和NaHCO3的混合物
11.下列各项比较中说法正确的是 ( )
A.食盐水的沸点比蒸馏水高
B.武德合金的熔点比其成分金属高
C.硝酸铵的溶解热比氢氧化钠高
D.木条的着火点比木炭高
12.下列四个图象分别对应四种操作(或治疗)过程,其中正确的是 ( )

A.服用胃舒平[主要成分Al(OH)3]治疗胃酸过多
B.向硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液直至过量
C.常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
D、将一定质量的硝酸钾不饱和溶液恒温蒸发水份,直至有少量晶体析出
13.除去下表中各物质(A~C为溶液)中的少量杂质,所选用的试剂、方法正确的是 ( )

14.某学生设计了下图所示的四套装置来制取CO2,其中在制取时不能使反应随时发生或停止的装置为 ( )

15.下列离子能在pH=1的无色溶液中大量共存的是 ( )
A.Cu2+、SO42-、Cl-、Na+ B.OH-、K+、NO3-、Ba2+
C.Mg2+、SO42-、Al3+、NO3- D.Na+、CO32-、Ca2+、Cl-
第Ⅱ卷(共70分)
二、(本题包括6小题,共27分)
16.(7分)(1)某元素原子结构示意图为 该元素原子核内有________个质子,
该元素原子核内有________个质子,
最外电子层上有__________个电子,在化合物中可以表现的负价为 。
(2) 用化学符号表示:2个氨分子__________,一个硝酸根离子__________,氦气 ;
铁置于过量稀盐酸充分反应后所得溶液中的溶质
17.(5分)现有①人造革 ②鱼肝油丸 ③蚕丝 ④大米 ⑤色拉油 ⑥福尔马林(甲醛溶液)
⑦聚乙稀 ⑧橡胶 ⑨不锈钢 ⑩玻璃等生活中常见的物品,根据下列内容选取填合适的序号:
(1) 富含糖类,习惯上被称为碳水化合物;
(2) 属于无机非金属材料的是 ;
(3) 蛋清中加入 后会出现凝固现象;
(4) 灼烧后会嗅到烧焦羽毛味;
(5) 常制成食品袋,但废弃后易形成“白色污染”。
18.(4分)在10%的硫酸溶液中存在着自由移动的微粒是 (填微粒符号),它能和10%的氢氧化钠溶液发生 反应(填反应类型),反应过程中不断减少的微粒是 (填微粒符号)。当两者恰好完全反应时,两种溶液中溶质的计量数之比等于___(用恰当的符号式表示)。
19.(3分)用所学的化学知识解释下列现象:(在下面4个问题中任选3个回答,若都回答,则按前3个答案计分。)
⑴ 下雪天为防止车轮打滑,道路维护人员在路面铺洒工业盐。
_____________________________________________________________________
⑵ 硫粉在酒精灯火焰上引然后发出微弱的淡蓝色火焰,伸入盛有氧气的集气瓶后发出明亮的蓝紫色火焰。
_____________________________________________________________________
⑶在古代,人们把烧红的生铁放在铁砧上反复锤打,最终将生铁转化为钢。
_____________________________________________________________________
⑷伪劣奶粉(主要用米粉、菊花精、糖调和而成)几乎不含蛋白质,严重影响婴幼儿的大脑发育。用滴加碘水的方法可以简便地识别这种“奶粉”。
_____________________________________________________________________
20.(5分)A是海水中含量最多的元素,B是太阳中含量最多的元素,C是空气中含量最多的元素,D是有机物中都含有的元素。由A、B、C、D四种元素组成的一种常见化学肥料是________(写化学式),它________(填“是”或“不是”)复合肥。当这种化肥与改良酸性土壤的________(填俗名)在研钵中混合研磨后,会闻到________气味。这种气味的气体也可使湿润的红色石蕊试纸变________。
三、(本题包括3小题,共21分)
21.(13分)小强和几位同学在实验室用下列装置制取几种气体。

⑴ 写出图中标有①、②的仪器名称:①________________②________。
⑵ 小强想用高锰酸钾制取纯净的氧气,他应选择上述装置中的A和________(填字母)进行
组装。你认为A装置中还缺少________________。写出该反应的化学方程式为______。当氧气收集满并取出集气瓶后,停止该实验的正确操作步骤是先_________后_________。
(3) 小张选用B和C装置可制取的气体是_________(答一种),写出实验室制取该气体
的化学方程式_________________,他应如何检查B装置的气密性__________________。
(4)小陈想用双氧水和二氧化锰混合制取氧气,写出该反应的化学方程式_________,其中二氧化锰_________和_________在反应前后保持不变。为控制反应的剧烈程度,他应将B装置中的长颈漏斗改为_________(填仪器名称)。
22.(4分)我们已经知道,常见金属按其活动性强弱可排成如下顺序:
K、Ca、Na、Mg、Al、Zn、Fe、 、 、(H)、Cu、 、Ag、 、Au
(1) 请用相应的元素符号完成上述金属活动性顺序表。
(2) 向硝酸银和硝酸铜的混合溶液中加入一些镁粉,完全反应后过滤。若向残渣中滴加稀盐酸后有气泡冒出,则残渣中含有的金属是 ;若残渣中无气泡生成,则滤液中一定含有的金属离子是 。(填符号)
四、(本题包括3小题,共12分)
23.(4分)据2006年3月24日的《苏州日报》报道,“玉米衣服”亮相太仓。所用的玉米纤维是由玉米中提炼出的淀粉经发酵变成乳酸、乳酸再聚合为聚乳酸、聚乳酸纺丝变成的纤维。然后再将玉米纤维和竹纤维混纺,生产出各项性能指标与涤纶纤维相近的“玉米纱”。这项技术已列入年内申报国家级火炬项目。查阅有关资料后得知,聚乳酸的化学式为(C3H6O3)n。
(1) 聚乳酸 (填“是”或“不是”)高分子化合物?
(2) 玉米纱属于 ;(选填“合成纤维”或“人造纤维”或“天然纤维”)
(3) 聚乳酸中各元素的质量比为 m( ):m( ):m( )== ;
24.(4分)在t℃时,有94g饱和硝酸钾溶液,当蒸发掉25g水,再冷却到t℃时,剩余溶液的质量为41.5g,求:
(1) 硝酸钾在t℃时的溶解度;
(2) 剩余溶液中溶质的质量分数。
25.(4分)向盛有12.60g碳酸氢钠固体的烧杯中,加入100.5g硫酸溶液恰好反应。反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如图所示。烧杯连同药品的起始质量为200.0g。反应的化学方程式为: 2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑
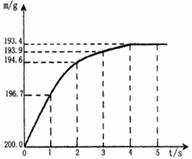
回答下列问题:
(1) 当碳酸氢钠与硫酸溶液恰好完全反应时,所需的时间约为 。
(2) 当碳酸氢钠与硫酸溶液完全反应时,所产生二氧化碳的质量为 。
(3) 反应后,所得硫酸钠溶液的溶质质量分数为多少?
五、(本题包括2小题,共10分)
26.(4分)某化学兴趣小组想探究二氧化硫的水溶液是否呈酸性,先用在氧气中燃烧硫粉的方法收集了一瓶充满二氧化硫的气体,倒入10mL蒸馏水后振荡静置,然后按下面步骤实验:
①倒出5mL这种“水”于一支试管中;
②将3滴紫色石蕊试液滴入这种“水”;
③另取一支试管,倒入5mL稀盐酸,滴3滴紫色石蕊;
④再取一支试管,倒入5mL蒸馏水,滴3滴紫色石蕊。
请回答:
⑴ 实验②与③实验对比是为了说 ;
⑵ 实验④的作用是 ;
⑶ 实验②、③、④中滴加相同滴数的紫色石蕊其目的是 。
27.(6分)食品包装盒中常放一小袋粉末状物质,该物质对食品同时具有防潮和防氧化作用。某同学从超市购买的食品包装盒中取出装有粉末状物质的小袋,撕开发现袋里有板结的红褐色固体,就近嗅到铁锈味。
(1) 试推测粉末状物质可能是 ;其作用原理 。
(2) 查阅资料得知:铁锈中铁元素呈正三价,Fe3+ 和硫氰化钾溶液反应后能生成血红色的化合物。
(3) 设计一个实验,证明你的猜想。(药品和仪器自选,实验方案可用绘图或文字叙述)
实验方案
实验现象
结论或解释