2005年山东省青岛市模拟试题一
第I卷(选择题)
相对原子质量 H-1 O-16 C-12 Na-23 Cl-35.5 Mg-24 Ca -40
一、选择题(本题共16道小题,每题各有一个正确答案,共16分)
1. 现代人正进入以“室内空气污染”为标志的第三个污染时期。以下不属于室内空气污染的是( )
A 烹饪时产生的油烟
B 二氧化碳含量过高造成的温室效应
C 石才释放出的有害放射性气体
D 劣质黏合剂释放出的甲醛等有害物质
2. 自然界发生的下列变化中,属于物理变化的是( )
A、水在自然界的循环
B、二氧化碳在自然界的循环
C、人和动物的呼吸
D、酸雨的形成
3.现有一瓶工业酒精和一瓶食盐水,区分它们的最简便的方法是( )
A、闻气味 B、品尝味道 C、取少量点燃 D、用硝酸银溶液检验
4. 继发现C60 后C70也已制得。下列有关C70的说法中正确的是
A 它是一种化合物 B 它是一种单质
C 它是由原子构成的 D 它的相对分子质量是70g
5. 遇到下列情况,采取的措施正确的是( )
A 发现家中的天然气泄漏,立即打开吸排油烟机
B 酒精灯不慎打翻起火,立即用水浇灭
C 电线短路引起电器着火时,可用水烧灭
D 炒菜时油锅中的油着火时,可用锅盖盖灭
6.人体中含量最多的元素是( )
A 钙 B 碳 C 氧 D 氮
7. 一些食物的近似pH如下:葡萄汁3.5~4.5;苹果汁2.9~3.3;牛奶6.3~6.6;鸡蛋清7.6~8.0。则下列说法中,不正确的是
A 胃酸过多的人应饮葡萄汁 B 苹果汁能使石蕊试液变红色
C 鸡蛋清为碱性食品 D 牛奶比苹果汁的酸性弱
8. 电池污染日益受到人们的关注,科技人员相继发明了一些环保电池,你认为下列属于环保电池的是 ( )
A.太阳能电池 B.镍汞电池 C.锌锰干电池 D.铅酸电池
9. 某有机物X在氧气中充分燃烧的化学方程式是:2X+5O2=4CO2+4H2O,则X的化学式是( )
A、C2H4 B、C4H8 C、C2H4O D、C2H4O2
10. 现有X、Y、Z三种金属,根据下列有关反应方程式可知,三种金属的活动性顺序是( )
①Z+YSO4==ZSO4+Y ②X+YSO4==XSO4+Y
③Z+H2SO4==ZSO4+H2↑ ④X+H2SO4不发生反应
A、Z>X>Y B、Z>Y>X C、X>Y>Z D、X>Z>Y
11. 下列各组中的两种物质,在一个化学反应中不能同时生成的是( )
A、H2 O2 B、BaSO4 Cu(OH)2 C、Cu Zn(NO3)2 D、FeCl3 H2
12. 科学探究是学习化学的重要而有效的学习方式。它包括:
① “建立假设”② “交流评价”③“获得结论”④“提出问题”⑤“收集证据”等基本环节。合理的探究顺序是( )
A ①②③④⑤ B ④⑤①②③ C ④①⑤③② D ①④⑤②③
13. 中华民族在世界冶金史上曾谱写过辉煌的篇章,右图即为我国东汉晚期所铸的青铜奔马(马踏飞燕)。早在2000多年前的西汉时期就有“曾青得铁则化为铜”的记载,从现代化学的观点理解,这句话的含义是

A 木炭还原氧化铜生成单质铜
B 氧化铜在单质铁的催化作用下,分解成铜
C 氢氧化铜和铁的化合物反应生成铜
D单质铁从铜盐溶液中置换出铜
14. 关于O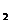 表示的意义有以下几种说法①表示氧气这种物质,②表示氧元素,③表示两个氧原子,④表示一个氧分子,⑤表示一个氧分子里有两个氧原子,⑥表示氧气是一种无色气体,其中正确的是( )
表示的意义有以下几种说法①表示氧气这种物质,②表示氧元素,③表示两个氧原子,④表示一个氧分子,⑤表示一个氧分子里有两个氧原子,⑥表示氧气是一种无色气体,其中正确的是( )
A、 ①④⑤ B 、①④⑤⑥ C、 ①③④⑤ D 、③④⑤
15.、要使不饱和溶液变为饱和溶液,不改变其质量分数的方法是( )
A、加热蒸发溶剂后,再降至原温度
B、加入一定量的硝酸钾晶体
C、降温至溶液刚好饱和
D、降温后使其析出部分晶体
16.已知同温同压下等体积的不同气体含有相同的分子数,天然气、液化石油气燃烧的化学方程式分别为:CH4+2O2=CO2+2H2O; C3H8+ 5O2=3CO2+4H2O。现有一套以天然气为燃料的灶具,要改为以液化石油气为燃料的灶具应采取的措施是( )。
A.燃料气和空气的进入量都减少
B.燃料气和空气的进入量都增加
C.减少燃料气进入量或增大空气进入量
D.增大燃料气进入量或减少空气进入量
二、选择题(本题共8道小题,每题各有一个或两个正确答案,共16分)
17. 下列有关溶液的认识中,错误的是
A.析出晶体后的溶液是该温度下的饱和溶液
B.在溶液里进行的化学反应,通常是比较快的
C.同种溶质的饱和溶液,一定比它的不饱和溶液的浓度大
D.食物里的营养成分经消化变成溶液,容易被人体吸收
18. 下列有关单质的叙述中,正确的是( )
A.单质不能用分解反应制取
B.单质可以参加化合反应
C.单质不能参加复分解反应
D.单质只能用置换反应制取
19. 现有烧杯、试管、量筒、带铁圈铁夹的铁架台、酒精灯、集气瓶、玻片、水槽、药匙、带导管的橡皮塞、玻璃棒,仅有这些仪器(所需化学药品可任选),不能完成的实验是( )
A.用高锰酸钾加热制氧气 B.粗盐提纯
C.制取二氧化碳 D.用氯化钠晶体配制100g 5%的氯化钠溶液
20.现有50mL质量分数为20%的硫酸溶液,它的密度为1.14g/cm ,下列说法正确的是( )
A、该溶液含溶质10g B、溶质质量:溶液质量==1:6
C、溶质质量:溶剂质量==1:5 D、溶液质量:溶剂质量==5:4
21. 在杠杆的两端分别挂着质量和体积都相同的铁球和铝球,这时杠杆平衡。将两球分别浸泡在质量相同、溶质的质量分数也相同的稀硫酸中(如右图),直至两个烧杯中均没有气泡产生为止。两球的外形变化不大且无孔洞出现。下列推测中,正确的是( )。
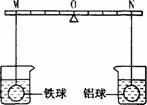
A.铁球一定是空心的
B.拿掉烧杯后,杠杆仍然平衡(金属球上附着的液体忽略不计,下同)
C.拿掉烧杯后,要想使杠杆平衡,支点应向N移动
D.拿掉烧杯后,要想使杠杆平衡,支点应向M移动
22. 下列各组气体按一定的质量比或体积比混合点燃,经充分反应后能得到纯净物的是( )
A、质量比为2:1的氢气和氧气
B、质量比为7:4的一氧化碳和氧气
C、质量比为1:4的甲烷和氧气
D、体积比为2:1的氢气和空气
23. 在托盘天平的两边各放一只烧杯,调节天平至平衡。向烧杯中分别注入等质量等质量分数的稀盐酸,然后分别放入质量相等的镁和铝。待充分反应后,镁有剩余,则还可观察到的现象是( )
A.天平仍平衡 B.天平指针偏向放镁的一方
C 天平指针偏向放铝的一方 D 铝也有剩余
24.某固体物质由氢氧化钠和氯化镁组成,取一定量的该混合物溶于水,有沉淀生成,在所得混合物中逐滴加入10%的盐酸时,发现沉淀质量(Y)与加入盐酸质量(X)有如图关系,则沉淀a的质量等于( )
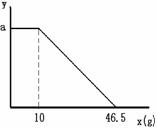
A、0.795g B.3.69g C. 2.9g D. 4.49g
第II卷(非选择题)
三、填空题
25.K2MnO4中锰元素的化合价为__________,细铁丝在氧气中燃烧的现象是 ,”3H2”中的”3”表示 ;”NH3”中的”3”表示 ,.地壳中含量最多的金属元素与含量最多的非金属元素组成化合物的化学式是 ;空气中含量第二位的气体单质是 。
26.判断下面4个观点正误。如果正确,请在题后空格处打“√”,如果错误,请写出化学式或化学方程式,否定错误观点:
观点
化学式或化学方程式
含氧的化合物就是氧化物
两种化合物生成另外两种化合物的反应都是复分解反应
酸与碱发生的是中和反应
氧化反应一定是化合反应
27.木炭、镁条、氢气都能在氧气中燃烧,其变化的本质和现象有不少共同之处,如反应都需要点燃、生成物都是氧化物.请你再归纳出它们的三个共同点:
(1) _;
(2) _;
(3) _.
28.现有一氧化碳和氧气的混合气体5g,点燃使之充分反应,将气体通入足量的澄清的石灰水中,生成白色沉淀10g,则原混合气体中氧气最多不超过 g;反应后气体的成分可能是 或 。
29.某无色混合气体可能含有氮气、一氧化碳、二氧化碳、氢气四种气体,使该气体依次通过紫色石蕊试液,没有颜色变化,再将该气体通过固体烧碱、灼热的氧化铜、澄清的石灰水和白色硫酸铜,依次观察到黑色粉末变红色、石灰水变浑浊、白色固体变蓝。则该混合气体中,一定含有 ;一定不含有 。
四、简答题
30.在焊接和电镀金属时,常用到稀盐酸,其作用是 ;
在点燃甲烷等可燃性气体之前要先检验其纯度,其目的是 。
31.机动车排放的尾气中,含有碳氢化合物、一氧化碳、二氧化碳、氮的氧化物(如NO)等物质,是城市空气的污染源之一。
(1)尾气中的 能引起酸雨,尾气中的 能与人体中的血红蛋白结合而使人中毒。
(2)治理尾气的方法之一是在汽车的排气管上装一个“催化转化器”(用铂、钯合金作催化剂)。它的作用是使一氧化碳与一氧化氮反应,生成两种气体,其中一种可参与植物的光合作用,另一种是空气中含量最多的气体。请写出一氧化碳与一氧化氮反应的化学方程式 。
32.浓硫酸在工厂里常用铁制或铝制容器密封贮存,但近有报道,一些个体修理厂里未经专业培训的电焊工人,在焊接用水清洗盛过浓硫酸的铁罐时,却发生了多起爆炸事故。请分析问题:(1)浓硫酸可用铁制或铝制容器贮存的事实说明在常温下浓硫酸 (填“能”或“不能”)溶解金属铁或铝。(2)常温下稀硫酸_____(填“能”或“不能”)用上述方法贮存。这是因为硫酸和稀硫酸尽管_____相同,但它们在常温下化学性质 (填“有”或“没有”)差别。(3)用化学知识简述爆炸事故发生的原因。
五、实验题
33.有两瓶无色气体,他们分别是二氧化碳和氧气,有多种方法可将他们区别开来。请你模仿示例要求,列举两种鉴别方法:
示例:用带火星的木条分别插入瓶口下,复燃的是氧气,熄灭的是二氧化碳。
方法1:____________________________________________;
方法2:____________________________________________。
34.根据装置图回答下列问题(装置用代号表示):

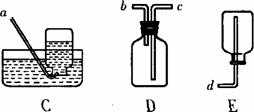
(1)写出有编号仪器的名称:① ,② 。
(2)实验室制取氧气的发生装置可选用 ;
(3)下表是三种气体的密度(在0℃、101 kPa条件下测定)和溶解度(在20℃、101 KPa条件下测定)。
气体性质
H2
CO2
SO2
密度(g/L)
O.08987
1.975
2.716
溶解度(g)
0.0001603
O.1688
11.28
实验室要收集SO2气体,可选用 装置收集,气体由 (导管口代号)导入集气瓶,排出的尾气还需要用氢氧化钠溶液吸收,以防止污染环境。此反应的化学方程式为: 。如果用D装置做尾气吸收装置装有氢氧化钠溶液,气体由 (导管口代号)导入该装置。
35.为了避免试验失败甚至造成严重后果,有些化学实验必须严格遵循操作的顺序,例如,点燃氢气前必须先验纯,再点燃。请你仿照示例填写下表1、2中的空格,再举出1个必须严格遵循操作顺序的实验,填写下表3中的所有空格。
必须严格遵循操作顺序的实验
先做什么
再做什么
示例:点燃氢气
先验纯
再点燃
1、铁丝在氧气中燃烧
先
再把系有燃着火柴棒的铁丝伸入集气瓶中
2、制取O2、CO2等气体
先
再
3、
先
再
36.用两种方法验证Fe、Cu、Ag三种金属的金属活动性由强到弱的顺序,可选用的试剂有AgNO3溶液、稀HCl、洁净的铜丝、铁丝、银丝、Cu(NO3)2溶液、FeSO4溶液。
实验步骤
实验现象
实验结论
方法(1)
金属活动性:Fe>Cu>Ag
方法(2)
六、计算题
37.配制500mL 10%的氢氧化钠溶液(密度为1.1 g/cm3),需氢氧化钠 g,需加水 g。
38.某省盛产石灰石,其中含有的杂质为二氧化硅(不溶于水、高温下难以分解的酸性氧化物)。某中学初三化学研究性学习小组的同学为了测定某矿山石灰石的纯度,取2.0 g该矿山石灰石样品,将20.O g盐酸平均分成4份,分4次加入到样品中,充分反应后测定剩余固体的质量,数据见下表。试求:
次 数
1
2
3
4
加入盐酸质量/g
5.O
5.O
5.O
5.O
剩余固体质量/g
1.3
O.6
O.2
O.2
(1)2.0 g石灰石样品中杂质的质量。
(2)石灰石样品中碳酸钙的质量分数。
(3)加入的盐酸中溶质的质量分数是多少?