题目内容
10.因环境污染,有人设想用瓶装纯净空气推向市场.设瓶装纯净空气的容积为500mL,所装空气的压强为2atm,空气的摩尔质量M=29×10-5kg/mol,NA=6.0×1023mol-1,标准状况下气体的摩尔体积为22.4L/mol.现按标准状况计算:(结果均保留1位有效数字)(1)瓶中空气在标况下的体积;
(2)瓶中空气的质量;
(3)瓶中空气的分子数.
分析 (1)根据理想气体的状态方程即可求出瓶中空气在标况下的体积.
(2)根据瓶子的体积求出瓶中气体的摩尔数,结合摩尔质量求出一瓶纯净空气的质量.
(3)然后根据瓶中气体的物质的量结合阿伏伽德罗常数求出分子数.
解答 解:(1)标准状况下:P=P0=2atm,V=?
瓶中气体:P′=2atm,V′=500mL=0.5L
由于温度相等,所以得:PV=P′V′
代入数据得:V=1L
(2)一瓶纯净空气的物质的量为:n=$\frac{1}{22.4}$mol.
则瓶中气体的质量为:m=nM=$\frac{1}{22.4}×29×1{0}^{-3}$kg=1×10-3 kg.
(3)分子数为:N=nNA=$\frac{{V}_{瓶}}{{V}_{m}}$•NA=$\frac{6×1{0}^{23}}{22.4}$个=3×1022个.
答:(1)瓶中空气在标况下的体积是1L;
(2)瓶中空气的质量是1×10-3 kg;
(3)瓶中空气的分子数是3×1022个.
点评 解决本题的关键知道摩尔质量、质量、摩尔数之间的关系,知道分子数等于质量与分子质量的比值.分子数也可以通过摩尔量与阿伏伽德罗常数的乘积求解.

练习册系列答案
相关题目
3.A物体的质量是B物体质量的5倍,A从h高处、B从2h高处同时自由落下,在落地之前,以下说法正确的是( )
| A. | 下落1s末,它们的速度相同 | |
| B. | 各自下落1m时,它们速度不同 | |
| C. | A加速度大于B加速度 | |
| D. | 下落过程中同一时刻A速度大于B速度 |
20.如图所示的情形中,涉及牛顿第三定律原理的有( )


| A. | 气垫船靠旋转的螺旋桨获得动力 | B. | 战斗机在行进途中抛弃副油箱 | ||
| C. | 喷水龙头自动旋转使水喷得均匀 | D. | 玩具火箭靠喷出火药飞上天空 |
5.两个分别带有电荷量-Q和+3Q的相同金属小球(均可视为点电荷),固定在相距为r的两处,它们间库仑力的大小为F,两小球相互接触后将其固定距离变为$\frac{r}{2}$,则两球间库仑力的大小为( )
| A. | $\frac{3}{4}$F,排斥力 | B. | $\frac{3}{4}$F,吸引力 | C. | $\frac{4}{3}$F,排斥力 | D. | $\frac{4}{3}$F,吸引力 |
15. 在光电效应实验中,某同学用同一光电管在不同实验条件得到了三条光电流与电压之间的关系曲线(甲光、乙光、丙光),如图所示,则下列说法正确的是( )
在光电效应实验中,某同学用同一光电管在不同实验条件得到了三条光电流与电压之间的关系曲线(甲光、乙光、丙光),如图所示,则下列说法正确的是( )
 在光电效应实验中,某同学用同一光电管在不同实验条件得到了三条光电流与电压之间的关系曲线(甲光、乙光、丙光),如图所示,则下列说法正确的是( )
在光电效应实验中,某同学用同一光电管在不同实验条件得到了三条光电流与电压之间的关系曲线(甲光、乙光、丙光),如图所示,则下列说法正确的是( )| A. | 甲光的频率大于乙光的频率 | |
| B. | 乙光的波长大于丙光的波长 | |
| C. | 甲光对应的光电子最大初动能大于丙光的光电子最大初动能 | |
| D. | 若该金属的逸出功为2.3eV,这意味着这种金属受到光照时若有电子逸出,则电子离开金膜表面时的动能至少等于2.3eV |
2.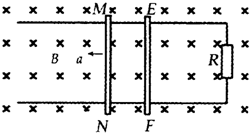 如图所示,相距为L的两条足够长的平行金属导轨右端连接有一定值电阻R,整个装置被固定在水平地面上,整个空间存在垂直于导轨平面向下的匀强磁场,磁感应强度大小为B,两根质量均为m,电阻都为R,与导轨间的动摩擦因数都为μ的相同金属棒MN、EF垂直放在导轨上.现在给金属棒MN施加一水平向左的作用力F,使金属棒MN从静止开始以加速度a做匀加速直线运动,若重力加速度为g,导轨电阻不计,最大静摩擦力与滑动摩擦力相等.则下列说法正确的是( )
如图所示,相距为L的两条足够长的平行金属导轨右端连接有一定值电阻R,整个装置被固定在水平地面上,整个空间存在垂直于导轨平面向下的匀强磁场,磁感应强度大小为B,两根质量均为m,电阻都为R,与导轨间的动摩擦因数都为μ的相同金属棒MN、EF垂直放在导轨上.现在给金属棒MN施加一水平向左的作用力F,使金属棒MN从静止开始以加速度a做匀加速直线运动,若重力加速度为g,导轨电阻不计,最大静摩擦力与滑动摩擦力相等.则下列说法正确的是( )
 如图所示,相距为L的两条足够长的平行金属导轨右端连接有一定值电阻R,整个装置被固定在水平地面上,整个空间存在垂直于导轨平面向下的匀强磁场,磁感应强度大小为B,两根质量均为m,电阻都为R,与导轨间的动摩擦因数都为μ的相同金属棒MN、EF垂直放在导轨上.现在给金属棒MN施加一水平向左的作用力F,使金属棒MN从静止开始以加速度a做匀加速直线运动,若重力加速度为g,导轨电阻不计,最大静摩擦力与滑动摩擦力相等.则下列说法正确的是( )
如图所示,相距为L的两条足够长的平行金属导轨右端连接有一定值电阻R,整个装置被固定在水平地面上,整个空间存在垂直于导轨平面向下的匀强磁场,磁感应强度大小为B,两根质量均为m,电阻都为R,与导轨间的动摩擦因数都为μ的相同金属棒MN、EF垂直放在导轨上.现在给金属棒MN施加一水平向左的作用力F,使金属棒MN从静止开始以加速度a做匀加速直线运动,若重力加速度为g,导轨电阻不计,最大静摩擦力与滑动摩擦力相等.则下列说法正确的是( )| A. | 从金属棒MN开始运动到金属棒EF开始运动经历的时间为t=$\frac{3μmgR}{{{B^2}{L^2}a}}$ | |
| B. | 若从金属棒MN开始运动到金属棒EF开始运动经历的时间为T,则此过程中流过电阻R的电荷量为q=$\frac{{BLa{T^2}}}{6R}$ | |
| C. | 若从金属棒MN开始运动到金属棒EF开始运动经历的时间为T,则金属棒EF开始运动时,水平拉力F的瞬时功率为P=(ma+μmg)aT | |
| D. | 从金属棒MN开始运动到金属棒EF开始运动的过程中,两金属棒的发热量相等 |
19.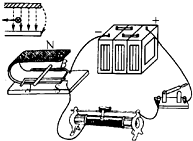 观察实验.选出正确答案,在如图所示的实验装置中,接通电源,导体AB受磁场力的作用而发生运动,然后改变电流方向或磁感线方向.则( )
观察实验.选出正确答案,在如图所示的实验装置中,接通电源,导体AB受磁场力的作用而发生运动,然后改变电流方向或磁感线方向.则( )
 观察实验.选出正确答案,在如图所示的实验装置中,接通电源,导体AB受磁场力的作用而发生运动,然后改变电流方向或磁感线方向.则( )
观察实验.选出正确答案,在如图所示的实验装置中,接通电源,导体AB受磁场力的作用而发生运动,然后改变电流方向或磁感线方向.则( )| A. | 在上述实验现象中,是机械能转化为电能 | |
| B. | 改变电流方向,通电导体所受磁场力的方向不变 | |
| C. | 改变磁感线方向(磁铁N、S极对调)通电导体所受 磁场力的方向不变 | |
| D. | 同时改变电流和磁感线的方向(磁铁N、S极对调),通电导体所受磁场力方向不变 |
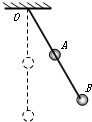 在长为L的轻杆中点和末端各固定一个质量为m的小球,杆可在竖直面内转动,如图所示,将杆拉至某位置释放,当其末端刚好摆到最低点时,下半段受力恰好等于球重的2倍,求:
在长为L的轻杆中点和末端各固定一个质量为m的小球,杆可在竖直面内转动,如图所示,将杆拉至某位置释放,当其末端刚好摆到最低点时,下半段受力恰好等于球重的2倍,求: