题目内容
13.已知铜的密度为8.9×103 kg/m3,铜的原子量为64,质子和中子的质量约为1.67×10-27 kg,则铜块中平均每个铜原子所占的空间体积为多少?铜原子的直径约为多少?分析 根据铜的摩尔质量求出摩尔体积,结合阿伏伽德罗常数求出铜原子的体积.将铜原子看出球形,结合球的体积求出铜原子的直径.
解答 解:(1)铜的原子量为64,即每摩尔铜的质量为64 g,其摩尔体积:Vmol=$\frac{M}{ρ}$=$\frac{6.4×1{0}^{-2}}{8.9×1{0}^{3}}$ m3 ①
每个铜原子的体积V0=$\frac{{V}_{mol}}{{N}_{A}}$ ②
由①②得V0=1.19×10-29 m3
(2)把铜原子作为球形模型,其直径设为d,则 $\frac{4}{3}$π($\frac{d}{2}$)3=V0
代入数据,解得d=2.83×10-10 m.
答:铜块中平均每个铜原子所占的空间体积为1.19×10-29 m3,铜原子的直径约为2.83×10-10 m
点评 本题关键要建立物理模型:把固体分子(或原子)当作弹性小球.并假定分子(或原子)是紧密无间隙地堆在一起,知道阿伏伽德罗常数是联系宏观物理量和微观物理量的桥梁.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
10.将一小球竖直向上抛出,小球在运动过程中所受到的空气阻力不可忽略.a为小球运动轨迹上的一点,小球上升和下降经过a点时的动能分别为Ek1和Ek2.从抛出开始到小球第一次经过a点时重力所做的功为W1,从抛出开始到小球第二次经过a点时重力所做的功为W2.下列选项正确的是( )
| A. | Ek1=Ek2,W1=W2 | B. | Ek1>Ek2,W1=W2 | C. | Ek1<Ek2,W1<W2 | D. | Ek1>Ek2,W1<W2 |
18.设r=r0时分子间作用力为零,则在一个分子从远处以某一动能向另一个分子靠近的过程中,下列说法正确的是( )
| A. | r>r0时,分子力做正功,动能不断增大,势能减小. | |
| B. | r=r0时,动能最大,势能最小. | |
| C. | r<r0时,分子力做负功,动能减小,势能增大. | |
| D. | 以上均不对 |
5.恒星的颜色取决于恒星的( )
| A. | 体积 | B. | 温度 | ||
| C. | 质量 | D. | 体积和温度以及它与地球的距离 |
2.关子质点概念,下列说法正确的是( )
| A. | 质点是一种理想化模型,实际并不存在 | |
| B. | 体积很大的物体,不能视为质点 | |
| C. | 研究运动员的跳水动作时,可以将运动员看成质点 | |
| D. | 研究火车通过某一路标的时间时,可以将火车看成质点 |
3.下列说法中正确的是( )
| A. | 聚变反应有质量亏损,所以质量数不守恒 | |
| B. | 结合能是由于核子结合成原子核而具有的能 | |
| C. | 比结合能越大,原子核中的核子结合的越牢固,原子核越稳定 | |
| D. | 铀核裂变的核反应方程为${\;}_{92}^{238}$U→${\;}_{56}^{141}$Ba+${\;}_{36}^{92}$Kr+2${\;}_{0}^{1}$n |
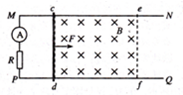 如图所示,MN、PQ为水平放置的足够长的平行光滑导轨,导轨间距L=1.0m,导轨左端连接一个R=0.2Ω的电阻和一个理想电流表A,导轨的电阻不计,整个装置放在磁感强度B=1T的有界匀强磁场中,磁场方向垂直于导轨平面向下.一根质量m=1.0kg、电阻r=1.0Ω的金属棒与磁场的左边界cd重合.现对金属棒施加一水平向右F=0.4N的恒定拉力,使棒从静止开始向右运动,已知在金属棒离开磁场右边界ef前电流表的示数已保持稳定.
如图所示,MN、PQ为水平放置的足够长的平行光滑导轨,导轨间距L=1.0m,导轨左端连接一个R=0.2Ω的电阻和一个理想电流表A,导轨的电阻不计,整个装置放在磁感强度B=1T的有界匀强磁场中,磁场方向垂直于导轨平面向下.一根质量m=1.0kg、电阻r=1.0Ω的金属棒与磁场的左边界cd重合.现对金属棒施加一水平向右F=0.4N的恒定拉力,使棒从静止开始向右运动,已知在金属棒离开磁场右边界ef前电流表的示数已保持稳定. 如图所示,PN与QM两平行金属导轨相距1m,电阻不计,两端分别接有电阻R1和R2,且R1=6Ω,ab杆的电阻r=2Ω,质量m=0.2kg,在导轨上可无摩擦地滑动,垂直穿过导轨平面的匀强磁场的磁感应强度为1T.现ab杆以恒定加速度a=1m/s2从静止开始向右移动(PN足够长),这时ab杆上消耗的电功率与R1、R2消耗的电功率之和相等,求:
如图所示,PN与QM两平行金属导轨相距1m,电阻不计,两端分别接有电阻R1和R2,且R1=6Ω,ab杆的电阻r=2Ω,质量m=0.2kg,在导轨上可无摩擦地滑动,垂直穿过导轨平面的匀强磁场的磁感应强度为1T.现ab杆以恒定加速度a=1m/s2从静止开始向右移动(PN足够长),这时ab杆上消耗的电功率与R1、R2消耗的电功率之和相等,求: