题目内容
现有m=0.90kg的硝酸甘油(C3H5(NO3)3)被密封于体积V0=4.0×10-3m3的容器中,在某一时刻被引爆,瞬间发生激烈的化学反应,反应的产物全是氮、氧…等气体.假设:反应中每消耗1kg硝酸甘油释放能量U=6.00×106J/kg;反应产生的全部混合气体温度升高1K所需能量Q=1.00×103J/K;这些混合气体满足理想气体状态方程 (恒量),其中恒量C=240J/K.已知在反应前硝酸甘油的温度T0=300K.若设想在化学反应后容器尚未破裂,且反应释放的能量全部用于升高气体的温度.求器壁受到的压强.
(恒量),其中恒量C=240J/K.已知在反应前硝酸甘油的温度T0=300K.若设想在化学反应后容器尚未破裂,且反应释放的能量全部用于升高气体的温度.求器壁受到的压强.
 (恒量),其中恒量C=240J/K.已知在反应前硝酸甘油的温度T0=300K.若设想在化学反应后容器尚未破裂,且反应释放的能量全部用于升高气体的温度.求器壁受到的压强.
(恒量),其中恒量C=240J/K.已知在反应前硝酸甘油的温度T0=300K.若设想在化学反应后容器尚未破裂,且反应释放的能量全部用于升高气体的温度.求器壁受到的压强.3.4×108Pa
化学反应完成后,硝酸甘油释放的总能量 W=mU,
设反应后气体的温度为T,根据题意,有 W=Q(T-T0),
器壁所受的压强 p=CT/V0.
解以上三式并代入数据进行计算,得 p=3.4×108Pa.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
 ,阿伏加德岁常数为M,则该种物质的分子体积为
,阿伏加德岁常数为M,则该种物质的分子体积为



 =2S,SB=S,容器上端开口,下端有一小孔C与外界相通,B的正中有一个厚度和质量都可忽略的活塞N,它与器壁有摩擦,最大静摩擦力为f,已知大气压强为p0,当时温度为T0,先把小孔C封住,再在活塞N上放一个砝码,砝码的重力大小等于f,当容器内气体的温度缓慢变化时,活塞有可能缓慢移动,为保证活塞在移动过程中不离开B筒,筒内气体温度最低和最高值各是多大?
=2S,SB=S,容器上端开口,下端有一小孔C与外界相通,B的正中有一个厚度和质量都可忽略的活塞N,它与器壁有摩擦,最大静摩擦力为f,已知大气压强为p0,当时温度为T0,先把小孔C封住,再在活塞N上放一个砝码,砝码的重力大小等于f,当容器内气体的温度缓慢变化时,活塞有可能缓慢移动,为保证活塞在移动过程中不离开B筒,筒内气体温度最低和最高值各是多大?
 .当阀门
.当阀门 闭锁时,三个恒温箱内气体状态分别如图所示,大气压强恒为P0.今将阀门
闭锁时,三个恒温箱内气体状态分别如图所示,大气压强恒为P0.今将阀门
 =0.5atm,
=0.5atm,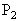 =1.5atm,外界大气压
=1.5atm,外界大气压 =1atm.初温均为27℃,
=1atm.初温均为27℃, =30cm,
=30cm, =16cm,
=16cm, =8cm.活塞处于静止.忽略一切摩擦.求:
=8cm.活塞处于静止.忽略一切摩擦.求:
 =?
=?