题目内容
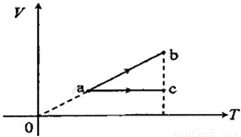
[物理-选修3-3](1)带有活塞的气缸内封闭一定量的理想气体.气体开始处于状态a,然后经过过程ab到达状态b或经过过程ac到达状态c,b、c状态温度相同,如V-T图所示.设气体在状态b和状态c的压强分别为Pb和Pc,在过程ab和ac中吸收的热量分别为Qab,Qac,则______(填入选项前的字母,有填错的不得分)
A.Pb>Pc,Qab>Qac B.Pb>Pc,Qab<Qac
C.Pb<Pc,Qab>Qac D.Pb<Pc,Qab<Qac
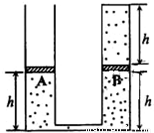
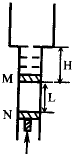
(2)图中系统由左右两个侧壁绝热、底部导热、截面均为左容器足够高,上端敞开,右容器上端由导热材料封闭.两容器的下端由可忽略容积的细管连通.
容器内两个绝热的活塞A、B下方封有氮气,B上方封有氢气.大气的压强为P,温度为T=273K,两活塞因自身重量对下方气体产生的附加压强均为0.1P.系统平衡时,各气柱的高度如下图所示.现将系统底部浸入恒温热水槽中,再次平衡时A上升了一定高度.用外力将A缓慢推回第一次固定,第三次达到平衡后,氢气柱高度为0.8h.氮气和氢气均可视为理想气体
(ⅰ)第二次平衡时氮气的体积;
(ⅱ)水的温度.
【答案】分析:(1)根据理想气体状态方程,整理后可得V-T图象,判断斜率的意义,得到压强的变化,再根据热力学第一定律判断做功和吸热;
(2)第一个过程是等温过程,应用玻意耳定理可解得,第二步为等压变化,用盖-吕萨克定理可以解得.
解答:解:(1)A、B、根据理想气体状态方程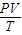 =C,
=C,
整理可得:V=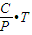
所以斜率越大,压强越小,即b点的压强小于c点,故AB错误.
C、D、由热力学第一定律△U=W+Q
经过过程ab到达状态b或经过过程ac到状态c,b、c状态温度相同,所以△U相等,
又因经过过程ab到达状态b,体积增大,对外做功,W为负值,
而经过过程ac到状态c,体积不变,对外不做功,W为零,所以第一个过程吸收的热量多,故C正确,D错误;
故选C;
(2)(ⅰ)考虑氢气的等温过程,该过程的初态压强为P,体积为hS,末态体积为0.8hS,
设末态的压强为P,由玻意耳定理得:
P=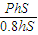 =1.25P
=1.25P
活塞A从最高点被第一次推回平衡位置的过程是等温过程,该过程的初态压强为1.1P,体积为V,末态压强为P′,末态压强V′
则:P′=P+0.1P=1.35P
V′=2.2hS
由玻意耳定理得:V= ×2.2hS=2.7hS
×2.2hS=2.7hS
(ⅰⅰ)活塞A从从最初位置升到最高位置过程为等压过程,该过程的初态体积和温度分别为2hS和T=273K,末态体积为2.7hS,
设末态温度为T,由该吕萨克定律得:T=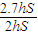 T=368.55K
T=368.55K
答:(ⅰ)第二次平衡时氮气的体积为2.75hS;
(ⅰⅰ)水的温度为368.55K.
点评:本题第一小题关键根据理想气体状态方程,结合热力学第一定律判断各物理量体积、压强、温度的变化;第二小题解题的关键点是找准变化过程属于等温过程、等压过程、还是等容过程,然后列出相应的关系式.
(2)第一个过程是等温过程,应用玻意耳定理可解得,第二步为等压变化,用盖-吕萨克定理可以解得.
解答:解:(1)A、B、根据理想气体状态方程
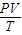 =C,
=C,整理可得:V=
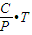
所以斜率越大,压强越小,即b点的压强小于c点,故AB错误.
C、D、由热力学第一定律△U=W+Q
经过过程ab到达状态b或经过过程ac到状态c,b、c状态温度相同,所以△U相等,
又因经过过程ab到达状态b,体积增大,对外做功,W为负值,
而经过过程ac到状态c,体积不变,对外不做功,W为零,所以第一个过程吸收的热量多,故C正确,D错误;
故选C;
(2)(ⅰ)考虑氢气的等温过程,该过程的初态压强为P,体积为hS,末态体积为0.8hS,
设末态的压强为P,由玻意耳定理得:
P=
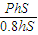 =1.25P
=1.25P 活塞A从最高点被第一次推回平衡位置的过程是等温过程,该过程的初态压强为1.1P,体积为V,末态压强为P′,末态压强V′
则:P′=P+0.1P=1.35P
V′=2.2hS
由玻意耳定理得:V=
 ×2.2hS=2.7hS
×2.2hS=2.7hS(ⅰⅰ)活塞A从从最初位置升到最高位置过程为等压过程,该过程的初态体积和温度分别为2hS和T=273K,末态体积为2.7hS,
设末态温度为T,由该吕萨克定律得:T=
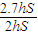 T=368.55K
T=368.55K答:(ⅰ)第二次平衡时氮气的体积为2.75hS;
(ⅰⅰ)水的温度为368.55K.
点评:本题第一小题关键根据理想气体状态方程,结合热力学第一定律判断各物理量体积、压强、温度的变化;第二小题解题的关键点是找准变化过程属于等温过程、等压过程、还是等容过程,然后列出相应的关系式.

练习册系列答案
相关题目
 物理--选修3-3
物理--选修3-3 [物理-选修3-3]
[物理-选修3-3]