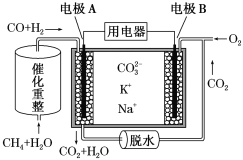
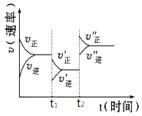
【题目】I.在锌与某浓度的盐酸反应的实验中,实验员得到下面的结果:
锌的质量(g) | 锌的形状 | 温度(℃) | 溶解于酸花的时间(s) | |
A | 2 | 薄片 | 5 | 400 |
B | 2 | 薄片 | 15 | 200 |
C | 2 | 薄片 | 25 | 100 |
D | 2 | 薄片 | 35 | 50 |
E | 2 | 薄片 | 45 | 25 |
F | 2 | 粉末 | 15 | 5 |
(1)写出基态Zn2+的核外电子排布式:_____,该反应是_____反应(填“放热”或“吸热”);
(2)仔细观察A~F的实验数据对比,你可以得到关于温度影响反应速率结论,用此结论,计算:55℃时,2g锌薄片溶解于酸中需花 _____s。
II.某可逆反应在某体积为5 L的密闭容器中进行,在从0~4分钟各物质的量的变化情况如图所示(X

(3)该反应的的化学方程式为__________________;
(4)反应开始至2分钟时,X的平均反应速率为__;
(5)能说明该反应已达到平衡状态的是_________;
a.每消耗1molX,同时生成1.33molZ b.容器内压强保持不变
c.Z的浓度不再变化 d.容器内混合气体的密度保持不变
(6)由下图求得平衡时Y的转化率为__________________。
(7)若保持容器体积不变,充入He,容器内反应速率将_______。(填“增大”“减小”或“不变”)