0 175464 175472 175478 175482 175488 175490 175494 175500 175502 175508 175514 175518 175520 175524 175530 175532 175538 175542 175544 175548 175550 175554 175556 175558 175559 175560 175562 175563 175564 175566 175568 175572 175574 175578 175580 175584 175590 175592 175598 175602 175604 175608 175614 175620 175622 175628 175632 175634 175640 175644 175650 175658 203614
 2CO2(g)+3H2O(g) ΔH1=-1366kJ·mol-1
2CO2(g)+3H2O(g) ΔH1=-1366kJ·mol-1
 CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。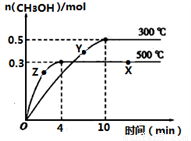
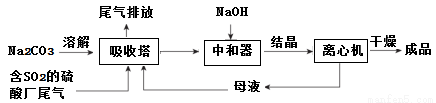
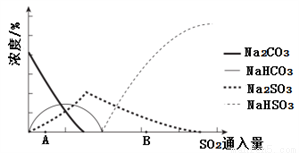



 g/cm3,阿伏加德罗常数为NA,则该晶胞的边长为______________cm。
g/cm3,阿伏加德罗常数为NA,则该晶胞的边长为______________cm。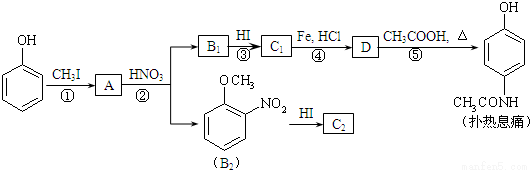
 ,请按要求填空:
,请按要求填空: 和
和 ,写出另3种同分异构体的结构简式____________、____________、____________。
,写出另3种同分异构体的结构简式____________、____________、____________。 2HI(g) ΔH=-QkJ·mol-1表示常温常压下,在恒温密闭容器中当有1mol H2和1mol I2(g)反应生成2 mol HI时放出QkJ的热量
2HI(g) ΔH=-QkJ·mol-1表示常温常压下,在恒温密闭容器中当有1mol H2和1mol I2(g)反应生成2 mol HI时放出QkJ的热量
 NH3•H2O+H+
NH3•H2O+H+ 2C(g)在定容密闭容器中达到平衡的标志的是
2C(g)在定容密闭容器中达到平衡的标志的是