0 175115 175123 175129 175133 175139 175141 175145 175151 175153 175159 175165 175169 175171 175175 175181 175183 175189 175193 175195 175199 175201 175205 175207 175209 175210 175211 175213 175214 175215 175217 175219 175223 175225 175229 175231 175235 175241 175243 175249 175253 175255 175259 175265 175271 175273 175279 175283 175285 175291 175295 175301 175309 203614

 是( )
是( )


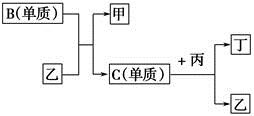
 O2(g)=4CO2(g)+5H2O(l)的ΔH ﹦
O2(g)=4CO2(g)+5H2O(l)的ΔH ﹦ 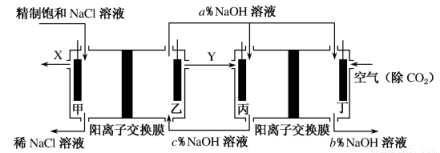
 装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________mol电子。
装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________mol电子。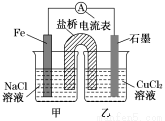

 FeO42?+3H2↑,工作原理如下图1所示。装置通电后,铁电极附近生成紫红色的FeO42?,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
FeO42?+3H2↑,工作原理如下图1所示。装置通电后,铁电极附近生成紫红色的FeO42?,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
 壤、水体污染等环境问题。
壤、水体污染等环境问题。


 S
S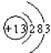

 解质
解质 的值不变
的值不变