硫酸工业中SO2转化为SO3是重要的反应之一,在一定压强和催化剂作用下在2L密闭容器中充入0.8molSO2和2molO2发生反应:2SO2(g)+O2(g) 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:
温度℃ | 450 | 475 | 500 | 525 | 550 | 575 | 600 | 650 |
SO2的转化率% | 97.5 | 95.8 | 95.8 | 93.5 | 90.50 | 85.6 | 80.0 | 73.7 |
(1)能判断该反应是否达到平衡状态的是
A.容器的压强不变
B.混合气体的密度不变
C.混合气体中SO3的浓度不变
D.C(SO2)=C(SO3)
E.v正(SO2)=v正(SO3)
F.v正(SO3)=2v逆(O2)
(2)某温度下经2min反应达到平衡后C(SO2)=0.08mol·L-1,
①此时的温度为 ℃
②若将平衡反应混合物的压强增大1倍(假如体积可变),此时Qc为 (可用分数表示),平衡将 向移动。
在温度T℃下,某Ba(OH)2稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,向该溶液中逐滴加入pH=b的盐酸,测得混合溶液的部分pH如下表所示:
序号 | 氢氧化钡的体积/mL | 盐酸的体积/mL | 溶液的pH |
① | 22.00 | 0.00 | 8 |
② | 22.00 | 18.00 | 7 |
③ | 22.00 | 22.00 | 6 |
(1)依据题意判断,T ℃________25 ℃(填“大于”、“小于”或“等于”),该温度下水的离子积Kw=__________。
(2)b=__________,原Ba(OH)2稀溶液的物质的量浓度为_____________。
(3)该温度下,向1 L硫酸与硫酸钠的混合溶液中加入3 L该Ba(OH)2的稀溶液时,沉淀量正好达最大值,从所得溶液中取出4 mL并加水稀释至20 mL,测得溶液的pH为7,则原硫酸与硫酸钠混合溶液的pH为__________。
 2 NH3(g)+CO2(g) △H >0。该反应的化学平衡常数的表达式K= 。
2 NH3(g)+CO2(g) △H >0。该反应的化学平衡常数的表达式K= 。 CO (NH2)2 (s) +H2O(g),混合气体中NH3的体积分数[φ(NH3)]随时间变化关系如图所示。
CO (NH2)2 (s) +H2O(g),混合气体中NH3的体积分数[φ(NH3)]随时间变化关系如图所示。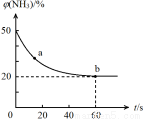
 )2↓+O2↑
)2↓+O2↑ 其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体。某温度下,部分含
其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体。某温度下,部分含 氯组分含量随pH变化情况如图所示,下列说法不正确的是
氯组分含量随pH变化情况如图所示,下列说法不正确的是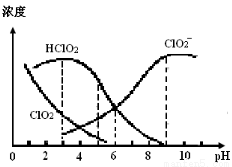
 空气中,容器内酸液的质量都减轻
空气中,容器内酸液的质量都减轻