硅孔雀石是一种含铜矿石,含铜形态为CuCO3·Cu(OH)2和CuSiO3·2H2O,同时含有SiO2、FeCO3、Fe2O3、Al2O3等杂质。以其为原料制取硫酸铜的工艺流程如图:

(1) 完成步骤①中稀硫酸与CuSiO3·2H2O反应的化学方程式:
CuSiO3·2H2O+H2SO4=CuSO4 +__________+H2O;双氧水的作用是 。
(2)有关氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 |
步骤②中,调节pH=4时,所得滤渣B的成分的化学式为 ,滤液B中除Cu2+外, 还含有的金属阳离子是 。
(3)将滤液B通过 、 ,过滤,洗涤等操作可得到硫酸铜晶体。
(4)硫酸铜也可以用硫化铜和氧气在高温 条件下化合制得,该反应的化学方程式 。
条件下化合制得,该反应的化学方程式 。
化学在生活中有着广泛的应用,下列对应关系正确的是( )
化学性质 | 实际应用 | |
A | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
B | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板.Com] |
C | 碳酸钠、Al(OH)3均可与酸反应 | 均可用于治疗胃酸过多 |
D | AlCl3在水溶液中有自由移动的Al3+和Cl- | 电解熔融状态的AlCl3制备Al |
 0.1 mol
0.1 mol


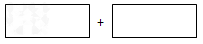
 H3OH(l)+3O2(g)=2CO2(g)+4
H3OH(l)+3O2(g)=2CO2(g)+4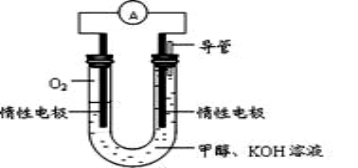
 将在___________(填电极名称)生成
将在___________(填电极名称)生成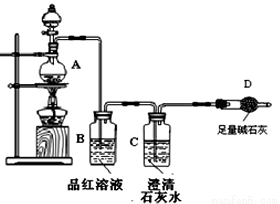

 观察到装置F中的现象是 。
观察到装置F中的现象是 。 Ⅱ中,将滤液B稀释为250 mL需要用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须要用到的是 ;
Ⅱ中,将滤液B稀释为250 mL需要用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须要用到的是 ;