5.下列反应的离子方程式中正确的是( )
| A. | 铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag | |
| B. | 氢氧化钡溶液与稀硫酸混合:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| C. | 碳酸钙溶于稀醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O |
4.若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在0℃、101 kPa时,22.4L氢气中含有NA个氢原子 | |
| B. | NA个CO分子和0.5mol CH4的质量比为7:4 | |
| C. | 16gCH4与18gNH${\;}_{4}^{+}$所含质子数相等 | |
| D. | 常温常压下,92g的NO2和N2O4混合气体中含有的原子数为6NA |
3.下列实验能达到目的是( )
| A. | 加入试剂按①SO42- ②Cl- ③OH-的正确顺序可以将混合液中Cu2+、Ba2+、Ag+逐一沉淀出来加以分离 | |
| B. | 配制480mL 1.0mol•L-1的NaOH溶液时,用托盘天平称取19.2gNaOH固体 | |
| C. | 用萃取分液的方法除去酒精中的水 | |
| D. | 用可见光束照射以区别溶液和胶体 |
2.下列说法正确的是( )
| A. | 对于相同浓度的弱酸HX和HY(前者的Ka较小)溶液,加水稀释相同倍数时,HY溶液的pH改变值小于HX溶液的pH改变值 | |
| B. | 在NH3•H2O和NH4Cl浓度均为0.1 mol•L-1的体系中,外加少量酸或碱时,溶液的pH可保持基本不变 | |
| C. | 在NaH2PO4水溶液中存在关系:c(H3PO4)+c(H+)=c(HPO42-)+c(PO43-)+c(OH-) | |
| D. | 沉淀溶解平衡AgI?Ag++I- 的平衡常数为8.5×10-17,说明难溶盐AgI是弱电解质 |
1.下列说法不正确的是( )
| A. | CH3CH2CHCH3CH2CH(CH3)2的系统命名为3,5-二甲基己烷 | |
| B. | 正丁烷的二氯代物有6种(不考虑立体异构) | |
| C. | 乙醇在铜催化下加热可脱氢生成乙醛,该反应属于氧化反应 | |
| D. | 淀粉、纤维素属于糖类化合物,在一定条件下都可以水解得到葡萄糖 |
20.下表为元素周期表的一部分.X、Y、Z、W为短周期元素,其中X元素的原子最外层电子数是其内层电子数的2倍.下列说法正确的是( )
| X | Y | ||
| Z | W | ||
| T |
| A. | X氢化物的沸点一定比Y氢化物的沸点高 | |
| B. | Z的最高价氧化物的水化物酸性一定比W的强 | |
| C. | XZ2、XW4与Na2O的化学键类型相同 | |
| D. | 根据元素周期律,可以推测存在T3Y4、TZ2和TW4 |
19.下列说法正确的是( )
| A. | 用分液漏斗分液时,先打开旋塞,待下层液体完全分出后,关闭旋塞,再从上口倒出上层液体 | |
| B. | 准确量取25.00 mL的液体可选用移液管、量筒或滴定管等量具 | |
| C. | 在中和热测定实验中,盐酸和NaOH溶液的总质量m g,反应前后体系温度变化,反应液的比热容为c J•g-1•℃-1,则生成1 mol水放出的热量为kJ | |
| D. | 在抽滤装置中洗涤晶体时,为减少晶体溶解损失,应使洗涤剂快速通过滤纸 |
18.下列说法不正确的是( )
0 173734 173742 173748 173752 173758 173760 173764 173770 173772 173778 173784 173788 173790 173794 173800 173802 173808 173812 173814 173818 173820 173824 173826 173828 173829 173830 173832 173833 173834 173836 173838 173842 173844 173848 173850 173854 173860 173862 173868 173872 173874 173878 173884 173890 173892 173898 173902 173904 173910 173914 173920 173928 203614
| A. | 质谱和核磁共振不仅可用于有机小分子结构的分析,还可用于蛋白质结构的研究 | |
| B. | 储氢金属吸氢形成金属氢化物,改变条件释放吸收的氢气,是氢气贮存的重要途径 | |
| C. | 牺牲阳极的阴极保护法、外加电源的阳极保护法和改变金属组成或结构的方法都是 防止金属腐蚀的方法 | |
| D. | 乙醇与水互溶,这与乙醇和水分子之间能形成氢键有关 |
 如图所示为实验室制取少量溴苯的装置,回答下列问题:
如图所示为实验室制取少量溴苯的装置,回答下列问题: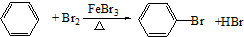
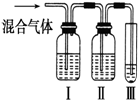 为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯,将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应.乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量有还原性的杂质气体,由此他提出必须先把杂质气体除去,再与溴水反应.
为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯,将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应.乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量有还原性的杂质气体,由此他提出必须先把杂质气体除去,再与溴水反应.