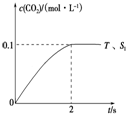
6.铅蓄电池的电极材料是Pb和PbO2,电解液是硫酸溶液.现用铅蓄电池电解饱和硫酸钠溶液一段时间.已知蓄电池放电时发生的反应为PbO2+Pb+2H2SO4═2PbSO4+2H2O,假设电解时温度不变且用惰性电极,下列说法不正确的是( )
| A. | 电解后,c(Na2SO4)不变,且溶液中有晶体析出 | |
| B. | 电解池的阳极反应式为:4OH--4e-═2H2O+O2↑ | |
| C. | 蓄电池放电时,每消耗0.1molPb,共生成0.1molPbSO4 | |
| D. | 蓄电池中每生成2molH2O,电解池中就消耗1molH2O |
5.对于化学反应Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g);△H=a mol/L,下列叙述不正确的是( )
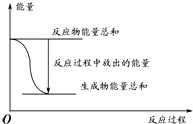

| A. | 反应过程中能量关系如上图表示,则该反应为放热反应 | |
| B. | 若将该反应设计成原电池,锌为负极 | |
| C. | 化学反应的焓变与反应方程式的计量数有关 | |
| D. | 若将其设计为原电池,当有32.5g锌溶解时,正极放出气体一定为11.2 L |
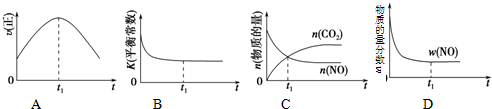
4.在平衡体系2NO+O2?2NO2中通入18O组成的氧气,重新达到平衡后,则18O( )
| A. | 只存在于O2中 | B. | 只存在于NO2中 | ||
| C. | 只存在于O2和NO2中 | D. | 存在于NO、O2、NO2 |
3.以下实验操作正确的是( )
| A. | 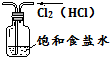 除去Cl2中的HCl气体 | B. |  淡化海水 | ||
| C. | 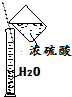 稀释浓硫酸 | D. | 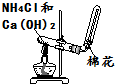 实验室制取氨气 |
2.下列说法正确的是( )
| A. | 硝酸钾制备实验中,将NaNO3和KCl的混合液加热并浓缩至有晶体析出,趁热过滤时,可以分离出硝酸钾 | |
| B. | 重结晶时,溶液冷却速度越慢得到的晶体颗粒越大 | |
| C. | 减压过滤操作时,应将滤纸放入布氏漏斗内,滤纸大小应略大于漏斗内径才能将全部小孔盖住 | |
| D. | 在两支试管中分别加1ml无水乙醇和1.5g苯酚固体,再加等量的钠,比较乙醇、苯酚羟基上氢原子的活泼性 |
1.下列有关厨房铝制品的使用中,你认为合理的是( )
| A. | 烧煮开水 | B. | 盛放食醋 | ||
| C. | 用金属丝擦表面的污垢 | D. | 用碱水洗涤 |
19.下列说法不正确的是( )
| A. | 甲苯和二甲苯互为同系物 | B. | 乙酸和甲酸甲酯互为同分异构体 | ||
| C. | H2和D2互为同位素 | D. | 石墨和金刚石互为同素异形体 |
18.下列说法正确的是( )
| A. | 电解稀硫酸或氢氧化钠溶液的产物不同 | |
| B. | 常温下,pH=6的溶液一定是酸溶液 | |
| C. | c(H+)>c(OH-)的溶液一定显酸性 | |
| D. | 水电解生成氢气和氧气,证明水是弱电解质 |
17.下列有关化学反应原理的应用叙述中,正确的是( )
0 173586 173594 173600 173604 173610 173612 173616 173622 173624 173630 173636 173640 173642 173646 173652 173654 173660 173664 173666 173670 173672 173676 173678 173680 173681 173682 173684 173685 173686 173688 173690 173694 173696 173700 173702 173706 173712 173714 173720 173724 173726 173730 173736 173742 173744 173750 173754 173756 173762 173766 173772 173780 203614
| A. | 电解饱和食盐水制烧碱,NaOH在阳极区域产生 | |
| B. | 合成氨生成过程中,采用高温高压都是为了提高N2、H2的转化率 | |
| C. | 给铁钉镀铜时,用铜做阴极 | |
| D. | 用明矾净水是因为Al3+水解生成的Al(OH)3胶粒具有很强的吸附性 |